Nitrik asit
| |||
| |||
| Adlandırmalar | |||
|---|---|---|---|
Nitrik asit | |||
Diğer adlar Aqua fortis, Kezzap, Hidrojen nitrat | |||
| Tanımlayıcılar | |||
3D model (JSmol)
|
|||
| 3DMet | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| ECHA InfoCard | 100.028.832 | ||
| EC Numarası |
| ||
| 1576 | |||
| KEGG | |||
| MeSH | Nitric+acid | ||
PubChem CID
|
|||
| RTECS numarası |
| ||
| UNII | |||
| UN numarası | 2031 | ||
CompTox Bilgi Panosu (EPA)
|
|||
| |||
| |||
| Özellikler | |||
| Kimyasal formül | HNO3 | ||
| Molekül kütlesi | 63,01 g mol−1 | ||
| Görünüm | Renksiz, sarı veya kırmızı dumanlı sıvı | ||
| Koku | keskin, boğucu[1] | ||
| Yoğunluk | 1.51 g cm−3, 1.41 g cm−3 [%68 w/w] | ||
| Erime noktası | −42 °C | ||
| Kaynama noktası | 83 °C %68 saflıktaki çözelti 121 °C'de kaynar. | ||
| Çözünürlük (su içinde) | Tamamen karışabilir | ||
| Buhar basıncı | 48 mmHg (20 °C) | ||
| Asitlik (pKa) | -1.4[2] | ||
| Termokimya | |||
Standart molar entropi (S⦵298)
|
146 J•mol−1•K−1[3] | ||
Standart formasyon entalpisi (ΔfH⦵298)
|
−207 kJ•mol−1[3] | ||
| Tehlikeler | |||
| GHS etiketleme sistemi: | |||
| Piktogramlar |  
| ||
| İşaret sözcüğü | TEHLİKE | ||
| Tehlike ifadeleri | H272, H300, H310, H330, H373, H411 | ||
| Önlem ifadeleri | P210, P220, P260, P305+P351+P338, P310, P370+P378 | ||
| NFPA 704 (yangın karosu) |
|||
| Parlama noktası | Yanıcı değildir | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LC50 (medyan konsantrasyon)
|
138 ppm (sıçan, 30 dak.)[1] | ||
| NIOSH ABD maruz kalma limitleri: | |||
| PEL (izin verilen) | TWA 2 ppm (5 mg/m3)[1] | ||
| REL (tavsiye edilen) | TWA 2 ppm (5 mg/m3) ST 4 ppm (10 mg/m3)[1] | ||
| IDLH (anında tehlike) | 25 ppm[1] | ||
| Güvenlik bilgi formu (SDS) | ICSC 0183 | ||
| Benzeyen bileşikler | |||
Diğer anyonlar
|
Nitröz asit | ||
Diğer katyonlar
|
Sodyum nitrat Potasyum nitrat Amonyum nitrat | ||
Benzeyen bileşikler
|
Azot pentaoksit | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |||
| Bilgi kutusu kaynakları | |||
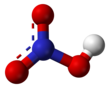
Nitrik asit HNO3 kimyasal formülüne sahip oldukça aşındırıcı bir inorganik asittir. Kezzap olarak da bilinir. Saf hâldeki bileşik renksizdir. Ancak uzun süre bekleyen eski asitler azot oksitleri ve suya ayrışması nedeniyle sarı renge dönebilme özelliğindedirler. Piyasada bulunan nitrik asitlerin çoğu % 68'lik bir konsantrasyona sahiptir. Çözelti, %86'dan fazla HNO3 içerdiğinde, dumanlı nitrik asit olarak adlandırılır. Mevcut azot dioksit miktarına bağlı olarak, dumanlı nitrik asit ayrıca %86’nın üzerindeki konsantrasyonlarda kırmızı dumanlı nitrik asit veya %95’in üzerindeki konsantrasyonlarda beyaz dumanlı nitrik asit olarak tanımlanır.
Nitrik asit, tipik olarak bir organik moleküle nitro grubunun eklenmesi olan nitrasyon için kullanılan ana reaksiyon maddesidir. Ortaya çıkan bazı nitro bileşikleri şok ve termik olarak hassas patlayıcı maddeler olsa da, bazıları mühimmat ve yıkımlarda kullanılacak kadar kararlıdır. Diğerleri ise daha kararlıdır ve mürekkep ve boyar maddelerde pigment olarak kullanılır. Nitrik asit, ayrıca kuvvetli bir oksitleyici madde olarak da yaygın şekilde kullanılmaktadır.
Fiziksel ve kimyasal özellikleri[değiştir | kaynağı değiştir]
Ticari olarak bulunan nitrik asit %68 HNO3 konsantrasyonunda bir azeotroptur. Bu çözelti, 1 atm’de 120.5 °C’lik bir kaynama sıcaklığına sahiptir. "Derişik nitrik asit" olarak bilinir. Saf derişik nitrik asit oda sıcaklığında renksiz bir sıvıdır.
İki katı hidratı bilinmektedir; monohidrat (HNO3•H2O veya [H3O]NO3) ve trihidrat (HNO3•3H2O).
Daha eski yoğunluk ölçeği olarak, bazen 42° Baumé derişik nitrik asit olarak da tanımlanır.[4]
Azot dioksit nedeniyle olan safsızlık[değiştir | kaynağı değiştir]

Nitrik asit, ısı veya ışık ayrışmasına maruz kalır ve bu nedenle genellikle kahverengi cam şişelerde saklanır:
- 4 HNO3 → 2 H2O + 4 NO2 + 2 O2
Bu reaksiyon sonucu üretilen azot oksitler, asit içinde kısmen veya tamamen çözündüğü için sıvının üzerindeki buhar basıncında göz ardı edilemeyecek bazı değişikliklere neden olabilir.
Azot dioksit (NO2) yüksek sıcaklıklarda nitrik asit içinde çözünerek, asidi sarı veya hatta kırmızı renge dönüştürür. Saf asit, havaya maruz kaldığında beyaz duman çıkarmaya meyilliyken, azot dioksit çözünmüş asit kırmızımsı kahverengi buharlar verir ve bu da "kırmızı dumanlı nitrik asit" ve "beyaz dumanlı nitrik asit" adlarına yol açar. Azot oksitler (NOx) nitrik asit içinde çözünür.
Dumanlı nitrik asit[değiştir | kaynağı değiştir]
Ticari kalitede dumanlı bir nitrik asit %98 HNO3 içerir ve yoğunluğu 1.50 g/cm3’tür. Bu kalitedeki asit patlayıcı madde endüstrisinde sıklıkla kullanılır. Susuz asit kadar uçucu veya aşındırıcı değildir ve yaklaşık 21.4 M konsantrasyonuna sahiptir.
Kırmızı dumanlı nitrik asit, çözeltiyi kırmızımsı kahverengi bir renkle terk eden önemli miktarlarda çözünmüş azot dioksit (NO2) içerir. Çözünmüş azot dioksit nedeniyle, kırmızı dumanlı nitrik asidin yoğunluğu 1.490 g/cm3’ten daha düşüktür.
Katkılı dumanlı nitrik asit, %0.6 - 0.7 hidrojen florür (HF) ilave edilerek yapılabilir. Bu florür metal tanklarda korozyon direnci için eklenir. Florür, metali koruyan bir metal florür tabakası oluşturur.
Susuz nitrik asit[değiştir | kaynağı değiştir]
Beyaz dumanlı nitrik asit, saf nitrik asit, susuz nitrik asite çok yakındır. Analiz derecesi olarak %99.9 nitrik asit şeklinde bulunmaktadır. Beyaz dumanlı nitrik asit için bir spesifikasyon, maksimum %2 suya ve maksimum %0.5 çözünmüş NO2'e sahip olmasıdır. Susuz nitrik asit, 1.513 g/cm3 yoğunluğa ve yaklaşık 24 molar konsantrasyona sahiptir. Susuz nitrik asit, −42 °C’de katılaşıp beyaz kristaller oluşturan 1.512 g/cm3 yoğunluğa sahip renksiz bir akışkan sıvıdır. NO2 ve suya ayrıştığında, sarı bir renk alır. 83 °C’de kaynar. Genellikle basınç oluşumuna izin vermek için tepe boşluğunun iki katı hacmine sahip kırılmaz bir amber cam şişede saklanır. Ancak bu önlemler bile yeterli olmaz ve basıncı azaltmak için şişenin aylık olarak havalandırılması gerekir.
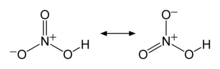
Yapı ve bağlanma[değiştir | kaynağı değiştir]

N–O bağlarından ikisi eşdeğer olup nispeten kısadır (bu rezonans teorileri ile açıklanabilir; doğal biçimler bu iki bağda çift bağ karakteri gösterir, bu da tipik N–O bağlarından daha kısa olmalarına neden olur). O atomu da bir protona bağlandığı için üçüncü N–O bağı uzamaktadır.[5][6]
Reaksiyonları[değiştir | kaynağı değiştir]
Asit-baz özellikleri[değiştir | kaynağı değiştir]
Nitrik asit, normal olarak oda sıcaklığında kuvvetli asit olarak kabul edilir. Asit ayrışma sabitinin değeri konusunda bazı anlaşmazlıklar olsa da, pKa değeri genellikle −1’den düşük olarak bildirilmektedir. Bu, seyreltilmiş çözeltideki nitrik asidin aşırı asidik çözeltiler dışında tamamen ayrıldığı anlamına gelir. pKa değeri 250 °C’de 1’e yükselir.[7]
Nitrik asit, sülfürik asit gibi daha kuvvetli bir asidin karşısında bir baz görevi görebilir:
- HNO3 + 2 H2SO4 ⇌ NO+2 + H3O+ + 2 HSO-4; Denge sabiti: K ≈ 22
Nitronyum iyonu, NO+2, aromatik nitrolama reaksiyonlarında aktif bir reaksiyon maddesidir. Nitrik asit hem asidik hem de bazik özelliklere sahip olduğundan, suyun kendiliğinden iyonlaşmasına benzer bir otoprotoliz reaksiyonuna uğrayabilir:
- 2 HNO3 ⇌ NO+2 + NO-3 + H2O
Metallerle olan reaksiyonları[değiştir | kaynağı değiştir]
Nitrik asit çoğu metalle reaksiyona girer. Ancak reaksiyonun ayrıntısı, asit konsantrasyonuna ve metalin doğasına bağlıdır. Seyreltik nitrik asit, çoğu metalle olan reaksiyonunda tipik bir asit gibi davranır. Magnezyum, mangan ve çinko H2 serbest bırakır:
- Mg + 2 HNO3 → Mg(NO3)2 + H2 (Magnezyum nitrat)
- Mn + 2 HNO3 → Mn(NO3)2 + H2 (Mangan(II) nitrat)
Nitrik asit, bakır ve gümüş gibi aktif olmayan metalleri oksitleyebilir. Aktif olmayan veya daha az elektropozitif metaller ile olan bu reaksiyon ürünleri sıcaklığa ve asit konsantrasyonuna bağlıdır. Örneğin, bakır, 3: 8 stokiyometri oranı ile oda sıcaklığında seyreltik nitrik asit ile reaksiyona girer:
- 3 Cu + 8 HNO3 → 3 Cu2+ + 2 NO + 4 H2O + 6 NO-3
Ortaya çıkan azot monoksit, azot dioksit vermek üzere atmosferik oksijen ile reaksiyona girebilir. Daha derişik nitrik asit ile, azot dioksit doğrudan 1: 4 stokiyometri oranındaki bir reaksiyonda oluşur:
- Cu + 4 H+ + 2 NO-3 → Cu2+ + 2 NO2 + 2 H2O
Nitrik asit ile olan reaksiyonlarında metallerin çoğu, karşılığı olan nitratları verir. Bazı yarı metaller ve metaller oksitleri verir; örneğin, Sn, As, Sb ve Ti sırasıyla SnO2, As2O5, Sb2O5 ve TiO2 olarak oksitlenir.[8]
Saf altın ve platin grubu metaller gibi bazı değerli metaller nitrik asit ile reaksiyona girmez. Ancak, saf altın derişik nitrik asit ve hidroklorik asit karışımı olan kral suyu ile reaksiyona girer. Bununla birlikte, renkli altın gibi altın bakımından nispeten düşük bazı altın alaşımlarında bulunan daha az soy metaller (Ag, Cu, ...) nitrik asit tarafından kolayca oksitlenebilir ve çözülebilir. Bu da altın alaşımlı yüzeyin renk değişikliklerine yol açar. Nitrik asit, kuyumcu dükkanlarında düşük altın alaşımlarını (< 14 ayar) hızlı bir şekilde tespit etmek ve altın saflığını hızla değerlendirmek için ucuz bir araç olarak kullanılır.
Kuvvetli bir oksitleyici madde olan nitrik asit birçok ametal bileşiklerle şiddetle reaksiyona girer ve reaksiyonlar patlayıcı olabilir. Asit konsantrasyonuna, sıcaklığa ve ilgili indirgeyici maddeye bağlı olarak, son ürünler değişken olabilir. Reaksiyon, soy metal serileri ve bazı alaşımlar hariç tüm metallerle gerçekleşir. Genel bir kural olarak, oksitleyici reaksiyonlar öncelikle derişik asit ile meydana gelir ve azot dioksit (NO2) oluşturur. Bununla birlikte, nitrik asidin güçlü oksitleyici özellikleri doğası gereği termodinamiktir. Ancak, bazen yükseltgenme reaksiyonları kinetik olarak tercih edilmez. Küçük miktarlarda nitröz asit (HNO2) varlığı reaksiyon hızını büyük ölçüde artırır.[8]
Krom (Cr), demir (Fe) ve alüminyum (Al) seyreltik nitrik asit içerisinde kolayca çözünmesine rağmen, derişik asit, metal kütlesini daha fazla oksidasyondan koruyan bir metal oksit tabakası oluşturur. Bu koruyucu tabakanın oluşumuna pasifleştirme denir. Tipik pasifleştirme konsantrasyonları hacimce %20 - 50 arasında değişir (bkz. ASTM A967-05). Derişik nitrik asit tarafından pasifleştirilen metaller demir, kobalt, krom, nikel ve alüminyum’dur.[8]
Ametallerle olan reaksiyonları[değiştir | kaynağı değiştir]
Kuvvetli bir oksitleyici asit olan nitrik asit, birçok ametal bileşiklerle şiddetle reaksiyona girer ve reaksiyonlar patlayıcı olabilir. Hidroksil grubu tipik olarak su oluşturmak için organik molekülden bir hidrojeni çıkarır ve geri kalan nitro grubu hidrojenin yerini alır. Organik bileşiklerin nitrik asit ile nitrolanması, nitrogliserin, nitroselüloz ve trinitrotoluen (TNT) gibi birçok yaygın patlayıcı maddelerin sentezinin birincil yöntemidir. Çok daha az kararlı yan ürünler mümkün olduğundan, bu reaksiyonlar dikkatlice termal olarak kontrol edilmeli ve yan ürünler istenen ürünü izole etmek için uzaklaştırılmalıdır.
Azot, oksijen, soy gazlar, silisyum ve iyot dışındaki halojenler hariç ametal elementlerle olan reaksiyon, genellikle seyreltik asit için azot monoksit ve derişik asit için azot dioksit oluşumu ile, onları asit olarak en yüksek yükseltgenme seviyelerine yükseltger.
- Cgrafit + 4 HNO3 → CO2 + 4 NO2 + 2 H2O
ya da
- 3 Cgrafit + 4 HNO3 → 3 CO2 + 4 NO + 2 H2O
Derişik nitrik asit I2, P4 ve S8’I sırasıyla HIO3, H3PO4 ve H2SO4’e yükseltger.[8] Grafit ve amorf karbon ile reaksiyona girmesine rağmen, elmas ile reaksiyona girmez; elması oksitlediği grafitten ayırabilir.[9]
Ksantoproteik test[değiştir | kaynağı değiştir]
Nitrik asit proteinlerle reaksiyona girerek, sarı renkli nitratlanmış ürünler oluşturur. Bu reaksiyon ksantoproteik reaksiyonu olarak bilinir. Bu test, test edilen maddeye derişik nitrik asit ilave edilerek ve daha sonra karışımın ısıtılmasıyla gerçekleştirilir. Aromatik halkalara sahip amino asitler içeren proteinler varsa, karışım sararır. Amonyak gibi bir baz eklendikten sonra renk turuncuya döner. Bu renk değişikliklerine proteindeki nitratlı aromatik halkalar neden olur.[10][11] Asit, epitel hücrelerine temas ettiğinde ksantoproteik asit oluşur. Kişisel lokal cilt rengi değişiklikleri, nitrik asitle çalışırken yetersiz güvenlik önlemlerinin bir göstergesidir.
Üretimi[değiştir | kaynağı değiştir]
Nitrik asit, azot dioksit (NO2)’in suyla olan reaksiyonu ile yapılır.
- 4 NO2 + 2 H2O → 2 HNO3 + NO + NO2 + H2O
Veya, sadeleşmiş formülü:
- 3 NO2 + H2O → 2 HNO3 + NO
Genellikle, reaksiyon tarafından üretilen azot monoksit, ilave azot dioksit üretmek üzere havadaki oksijen tarafından yeniden oksitlenir.
Hidrojen peroksit içinden azot dioksit geçirilmesi, asit verimini artırmaya yardımcı olabilir.
- 2 NO2 + H2O2 → 2 HNO3
Ticari kalitedeki nitrik asit çözeltileri genellikle %52 - 68 arasında nitrik asit içerir. Nitrik asit üretimi, Alman kimyager Wilhelm Ostwald'ın adını taşıyan Ostwald işlemi ile gerçekleşir. Bu işlemde, susuz amonyak, yaklaşık 250 °C’lik yüksek sıcaklıkta ve 9 atmosfer basınçta platin ya da rodyum tel örgü katalizör eşliğinde azot monoksit’e yükseltgenir.
- 4 NH3 (g) + 5 O2 (g) → 4 NO (g) + 6 H2O (g) (ΔH = −905.2 kJ/mol)
Azot monoksit daha sonra azot dioksit oluşturmak için havadaki oksijen ile reaksiyona sokulur.
- 2 NO (g) + O2 (g) → 2 NO2 (g) (ΔH = −114 kJ/mol)
Bu daha sonra nitrik asit ve azot monoksit oluşturmak için su içinde soğurulur.
- 3 NO2 (g) + H2O (l) → 2 HNO3 (aq) + NO (g) (ΔH = −117 kJ/mol)
Azot monoksit yeniden oksidasyon için döngüye ilave edilir. Alternatif olarak, son adım havada gerçekleştirilirse:
- 4 NO2 (g) + O2 (g) + 2 H2O (l) → 4 HNO3 (aq)
Elde edilen sulu HNO3 damıtma yapılarak, kütlece yaklaşık %68’e kadar derişik hale getirilebilir. Derişik H2SO4 ile yapılan dehidrasyonla %98’e kadar daha fazla derişim elde edilebilir. Haber işleminden elde edilen amonyak kullanılarak, nihai ürün tek hammadde olarak hava ve doğal gazdan üretilen azot, hidrojen ve oksijenden üretilebilir.[12]
Laboratuvar sentezi[değiştir | kaynağı değiştir]
Laboratuvarda nitrik asit, daha sonra nitrik asit vermek üzere sudan geçirilen azot dioksit ve oksijen gazları üreterek bakır(II) nitratın termal ayrışmasıyla yapılabilir.
- 2 Cu(NO3)2 → 2 CuO + 4 NO2 + O2
Ardından, Ostwald işlemini takip ederek:
- 2 NO2 + H2O → HNO2 + HNO3
Alternatif olarak, sodyum nitrat gibi herhangi bir nitrat tuzunun eşit kütlelerinin sülfürik asit (H2SO4) ile reaksiyonu ve bu karışımın nitrik asidin 83 °C kaynama noktasında damıtılmasıdır. Damıtma kabında uçucu olmayan metal hidrojen sülfat kalıntısı kalır. Elde edilen kırmızı dumanlı nitrik asit, beyaz nitrik asite dönüştürülebilir.[6]
- NaNO3 + H2SO4 → HNO3 + NaHSO4
Çözünmüş NOx, beyaz dumanlı nitrik asit vermek üzere oda sıcaklığında (200 mmHg veya 27 kPa’da 10–30 dakika) düşük basınç kullanılarak kolayca uzaklaştırılır. Bu işlem, daha az azot dioksit gazı üretmek için tek adımda düşük basınç ve sıcaklık altında da gerçekleştirilebilir.
Seyreltik nitrik asit, maksimum kaynama azeotropu olan %68 asit derişimine kadar damıtılarak derişik hale getirilebilir. Laboratuvarda, daha fazla konsantrasyon, su çekici madde olarak işlev gören sülfürik asit veya magnezyum nitrat ile damıtmayı içerir. Bu gibi damıtmalar, asidin ayrışmasını önlemek için tamamen cam aygıt ile düşük basınçta yapılmalıdır. Endüstriyel olarak, yüksek derişimli nitrik asit, fazladan ilave edilen azot dioksitin bir soğurma kulesinde %68 nitrik asit içinde çözündürülmesiyle üretilir.[13] Çözünmüş azot oksitler ya çözelti içinden ayrılıp beyaz dumanlı nitrik asidi oluştururlar veya kırmızı dumanlı nitrik asit oluşturmak için çözelti içinde kalırlar. Yakın zamanda, derişik nitrik asit hammaddesinden susuz asit üretmek için elektrokimyasal araçlar geliştirilmiştir.[14]
Kullanımı[değiştir | kaynağı değiştir]

Nitrik asidin ana endüstriyel kullanımı gübre üretimidir. Nitrik asit, amonyum nitrat vermek üzere amonyak ile nötralize edilir. Bu uygulama, yıllık (1987) üretilen 26 milyon tonun %75-80’ini tüketmektedir. Diğer ana uygulamalar patlayıcı maddeler, naylon öncül maddeleri ve özel organik bileşiklerin üretimi içindir.[15]
Organik azot bileşiklerinde öncül madde olarak[değiştir | kaynağı değiştir]
Organik sentezde, endüstriyel ve diğer şekilde, nitro grubu çok yönlü bir fonksiyonel gruptur. Nitrik ve sülfürik asitlerin bir karışımı, elektrofilik aromatik sübstitüsyon yoluyla çeşitli aromatik bileşikler üzerine etki ederek bir nitro ornatığı sokar. TNT gibi birçok patlayıcı madde bu şekilde hazırlanır:
- C6H5CH3 + 3 HNO3 → C6H2(NO2)3CH3 + 3 H2O
Derişik sülfürik asit ya da oleum fazla suyu absorbe eder.
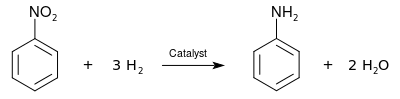
Nitro grubu, çeşitli nitrobenzenlerden anilin bileşiklerinin sentezine izin vererek bir amin grubu verecek şekilde indirgenebilir:
Oksitleyici madde olarak kulanımı[değiştir | kaynağı değiştir]
Naylonun öncül maddesi olan adipik asit, büyük ölçüde— siklohekzanon ve siklohekzanol’ün bir karışımı— olan "KA yağının nitrik asitle yükseltgenmesi yoluyla üretilir.[15]
Roket itici yakıtı[değiştir | kaynağı değiştir]
Nitrik asit, sıvı itici yakıtlı roketlerde oksitleyici olarak çeşitli formlarda kullanılmıştır. Bu formlar arasında kırmızı dumanlı nitrik asit, beyaz dumanlı nitrik asit, sülfürik asit ile karışımlar ve bu formlar HF katkılı bu formlar bulunur.[16] IRFNA (katkılı kırmızı dumanlı nitrik asit) BOMARC füzesi için 3 sıvı yakıt bileşeninden biriydi.[17]
Özel kullanımları[değiştir | kaynağı değiştir]
Analitik ayıraç[değiştir | kaynağı değiştir]
ICP-MS, ICP-AES, GFAA ve Alevli AA kullanılan element analizinde, çözeltilerdeki metal izlerini belirlemek için bir matris bileşiği olarak seyreltik nitrik asit (%0.5–5.0) kullanılır.[18] Bu tür bir belirleme için ultra saf iz metal kalitesinde asit gereklidir. Çünkü az miktarda metal iyonu analiz sonucunu etkileyebilir.
Aynı zamanda, bulanık su numunelerinin, çamur örneklerinin, katı numunelerin yanı sıra ICP-MS, ICP-OES, ICP-AES, GFAA ve alevli atomik absorpsiyon spektroskopisi yoluyla element analizi gerektiren diğer benzersiz örneklerin parçalama işleminde de kullanılır. Tipik olarak bu parçalanmalarda satın alınan Tip 1(Ultra saf) deiyonize su ile karıştırılmış HNO3’in %50’lik bir çözeltisi kullanılır.
Elektrokimyada, nitrik asit, organik yarı iletkenler için ve ham karbon nanotüpler için saflaştırma işlemlerinde kimyasal bir katkı maddesi olarak kullanılır.
Ağaç işleme[değiştir | kaynağı değiştir]
Düşük bir derişimde (yaklaşık %10), nitrik asit genellikle çam ve akçaağaçın yapay olarak eskitilmesi için kullanılır. Üretilen renk, cilalı veya yağlı çok eski bir ağaç görünümünde olup çok fazla grimsi altın rengindedir (ağaç yüzey işlemleri).[19]
Aşındırma ve temizleme maddesi[değiştir | kaynağı değiştir]
Nitrik asidin aşındırıcı etkileri, baskı yapımında gravür, paslanmaz çeliklerin dekapajı veya elektronikte silikon gofretlerin temizlenmesi gibi bazı özel uygulamalar için kullanılır.[20]
Bir nitrik asit, su ve alkol çözeltisi Nital, mikroyapıyı ortaya çıkarmak için metalleri aşındırmak için kullanılır. ISO 14104, bu iyi bilinen işlemi, detaylandıran standartlardan biridir.
Nitrik asit, hidroklorik asit ile birlikte veya tek başına, üst düzey mikroskopi uygulamaları için lam ve lamelleri temizlemek için kullanılır.[21] Gümüş aynalar yaparken gümüş kaplamadan önce camı temizlemek için de kullanılır.[22]
Ticari olarak temin edilebilen %5–30 nitrik asit ve %15–40 fosforik asit sulu karışımları, genellikle çökelmiş kalsiyum ve magnezyum bileşiklerini uzaklaştırmak için gıda ve mandıra ekipmanlarını temizlemek için yaygın olarak kullanılır (işlem akışından biriken veya üretim ve temizlik sırasında sert su kullanımından kaynaklanan). Fosforik asit içeriği, demir alaşımlarını seyreltik nitrik asit tarafından korozyona karşı pasifleştirmeye yardımcı olur.
Nitrik asit, LSD gibi alkaloidler için bir nokta testi olarak kullanılabilir ve alkaloide bağlı olarak çeşitli renkler verir.[23]
Güvenlik[değiştir | kaynağı değiştir]
Nitrik asit aşındırıcı bir asit ve kuvvetli bir yükseltgen maddedir. Bunun çıkardığı en büyük tehlike kimyasal yanıklardır. Çünkü, nitrik asit proteinler (amid) ve yağlarla (ester) asit hidrolizi gerçekleştirir. Bu durum, canlı dokuyu (örneğin deri ve vücut eti) ayrıştırır. Derişik nitrik asit, keratin ile reaksiyonu nedeniyle insan derisinde sarı lekeler bırakır. Bu sarı lekeler nötralleştirildiğinde turuncuya döner.[24] Bununla birlikte, sistemik etkiler olası değildir ve madde kanserojen veya mutajen olarak kabul edilmez.[25]
Cilde asit dökülmeleri için standart ilk yardım tedavisi, diğer aşındırıcı maddelerde olduğu gibi, büyük miktarlarda su ile yıkamaktır. Asit yanmasını çevreleyen dokuyu soğutmak ve ikincil hasarı önlemek için yıkama en az 10-15 dakika sürdürülür. Asitle bulaşmış giysiler hemen çıkarılır ve alttaki cilt iyice yıkanır.
Kuvvetli bir yükseltgen madde olan nitrik asit, siyanürler, karbürler veya metalik tozlar gibi bileşiklerle patlayıcı bir şekilde ve terebentin gibi birçok organik bileşiklerle, şiddetli ve hipergolik olarak (yani kendi kendine tutuşabilir) reaksiyona girebilir. Bu nedenle bazlardan ve organik maddelerden uzak tutulmalıdır.
Tarihçe[değiştir | kaynağı değiştir]
Nitrik asitten ilk kez, Ebû Bekir Muhammed bin Zekeriyyâ er-Râzî (854–925) gibi Arap simyacılarının[26] ve daha sonra Pseudo-Geber'in De Inventione Veritatis adlı eserlerinde bahsedilmiştir. Bu eserlerde, güherçile, şap ve mavi vitriyol karışımının kalsine edilerek elde edildiği yazılmaktadır. Yine 13. yüzyılda Albertus Magnus tarafından ve nitrik asidi güherçile ve kil ile ısıtarak hazırlayan ve "eau forte" (aqua fortis) olarak adlandırılan Ramon Lull tarafından tanımlanmıştır.[27]
Glauber, potasyum nitratı sülfürik asit ile damıtarak nitrik asit elde etmek için bir işlem tasarladı. 1776’da Lavoisier oksijen içerdiğini gösterdi ve 1785'te Henry Cavendish kesin bileşimini belirledi ve nemli havadan bir elektrik kıvılcımı akışı geçirerek sentezlenebileceğini gösterdi.[27] 1806’da, Humphry Davy, anotta çözünmüş atmosferik azot gazından nitrik asidin üretildiğine dair kapsamlı damıtılmış su elektroliz deneylerinin sonuçlarını bildirdi. Yüksek voltajlı bir batarya ve reaktif olmayan elektrotlar ile nemli asbestle köprülenen kaplar olarak iki katına çıkan altından yapılmış elektrot konileri gibi kaplar kullandı.[28]
Atmosferik havadan nitrik asidin endüstriyel üretimi, ark işlemi olarak da bilinen Birkeland–Eyde işlemi ile 1905'te başladı.[29] Bu işlem, atmosferik azotun atmosferik oksijen tarafından çok yüksek sıcaklıkta bir elektrik arkı ile azot monoksite yükseltgenmesine dayanır. 3000 °C'de yaklaşık %4-5'e kadar azot monoksit verimi, daha düşük sıcaklıklarda daha az verim elde edildi.[29][30] Azot monoksit soğutuldu ve geri kalan atmosferik oksijen tarafından azot dioksite yükseltgendi. Elde edilen azot dioksit seyreltik nitrik asit üretmek için bir seri dolgulu kolon veya plakalı kolon absorsorpsiyon kulesinde su içinde absorbe edildi. İlk kulelerde dolgu maddesi olarak reaktif olmayan kuvars parçaları dolu olup azot dioksit su ile birlikte bu kulelerde reaksiyona sokulmakta idi. Üretilen azot oksitlerin yaklaşık %20'si reaksiyona girmediğinden dolayı son kuleler geri kalanını nötralize etmek için bir alkali çözeltisi içeriyordu.[31] İşlem çok enerji harcıyordu ve ucuz amonyak elde edildikten sonra Ostwald işlemi tarafından hızla yer değiştirdi.
Başka bir erken üretim yöntemi 1913'te Fransız mühendis Albert Nodon tarafından icat edildi. Onun yönteminde, turba bataklıklarındaki azotlu maddeden bakteriler tarafından dönüştürülen kalsiyum nitratın elektrolizinden nitrik asit üretti. Kireçle çevrelenmiş toprak bir kap turbaya gömüldü ve nitrik asidin oluştuğu karbon anot için bir bölme yapmak için katranlı ağaç kazık ile bağlandı. Nitrik asit, kabın dibine batırılmış cam bir borudan[32] dışarıya pompalandı. Çıkarılan sıvıyı değiştirmek için başka bir cam borudan üstten temiz su pompalandı. İç kısmı kok kömürü ile dolduruldu. Döküm demir katotlar etrafındaki turbaya batırıldı. Direnç metreküp başına yaklaşık 3 ohm ve verilen güç yaklaşık 10 volt idi. Bir üretim hücresinden üretim, yılda 800 tondu.[32][33]
1913'te etkili amonyak üretimi için Haber işlemi tanıtıldıktan sonra, Ostwald işlemi kullanılarak amonyaktan nitrik asit üretimi Birkeland-Eyde işlemini geride bırakarak hakim bir üretim yöntemi oldu. Üretimin bu yöntemi bugün hâlâ kullanılmaktadır.
Kaynakça[değiştir | kaynağı değiştir]
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards. "#0447". National Institute for Occupational Safety and Health (NIOSH).
- ^ Bell, R. P. (1973), The Proton in Chemistry (2. bas.), Ithaca, NY: Cornell University Press
- ^ a b Zumdahl, Steven S. (2009). Chemical Principles 6th Ed. Houghton Mifflin Company. s. A22. ISBN 978-0-618-94690-7.
- ^ Dean, John (1992). Lange's Handbook of Chemistry (14 bas.). McGraw-Hill. ss. 2.79-2.80. ISBN 978-0-07-016194-8.
- ^ Luzzati, V. (1951). "Structure cristalline de l'acide nitrique anhydre". Acta Crystallographica (Fransızca). 4 (2): 120-131. doi:10.1107/S0365110X51000404.
- ^ a b Allan, D. R.; Marshall, W. G.; Francis, D. J.; Oswald, I. D. H.; Pulham, C. R.; Spanswick, C. (2010). "The crystal structures of the low-temperature and high-pressure polymorphs of nitric acid" (PDF). Dalton Trans. (Submitted manuscript). 39 (15): 3736-3743. doi:10.1039/B923975H. PMID 20354626. 23 Temmuz 2020 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 27 Haziran 2020.
- ^ IUPAC SC-Database 19 Haziran 2017 tarihinde Wayback Machine sitesinde arşivlendi. A comprehensive database of published data on equilibrium constants of metal complexes and ligands
- ^ a b c d Catherine E. Housecroft; Alan G. Sharpe (2008). "Chapter 15: The group 15 elements". Inorganic Chemistry (3. bas.). Pearson. ISBN 978-0-13-175553-6.
- ^ Ōsawa, Eiji (Aralık 2007). "Recent progress and perspectives in single-digit nanodiamond". Diamond and Related Materials. 16 (12): 2018-2022. Bibcode:2007DRM....16.2018O. doi:10.1016/j.diamond.2007.08.008.
- ^ Sherman, Henry Clapp (2007). Methods of organic analysis. Read Books. s. 315. ISBN 978-1-4086-2802-7.
- ^ Knowles, Frank (2007). A practical course in agricultural chemistry. Read Books. s. 76. ISBN 978-1-4067-4583-2.
- ^ Considine, Douglas M., (Ed.) (1974). Chemical and process technology encyclopedia. New York: McGraw-Hill. ss. 769-72. ISBN 978-0-07-012423-3.
- ^ Urbanski, Tadeusz (1965). Chemistry and technology of explosives. Oxford: Pergamon Press. ss. 85-86. ISBN 978-0-08-010239-9.
- ^ US 6200456, Harrar, Jackson E.; Roland Quong & Lester P. Rigdon et al., "Large-scale production of anhydrous nitric acid and nitric acid solutions of dinitrogen pentoxide", April 13, 1987 tarihinde yayımlandı, March 13, 2001 tarihinde verildi, assigned to United States Department of Energy
- ^ a b Thiemann, Michael; Scheibler, Erich; Wiegand, Karl Wilhelm (2000). "Nitric Acid, Nitrous Acid, and Nitrogen Oxides". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_293. ISBN 978-3527306732.
- ^ Clark, John D (1972). Ignition!. Rutgers University Press. ISBN 978-0-8135-0725-5.
- ^ "BOMARC Summary". BILLONY.COM. 11 Mayıs 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 28 Mayıs 2009.
- ^ Clesceri, Lenore S.; Greenberg, Arnold E.; Eaton, Andrew D., (Ed.) (1998). Standard methods for the examination of water and wastewater (20. bas.). American Public Health Association, American Water Works Association, Water Environment Federation. ISBN 978-0-87553-235-6.Şablon:Pn
- ^ Jewitt, Jeff (1997). Hand-applied finishes. Taunton Press. ISBN 978-1-56158-154-2. Erişim tarihi: 28 Mayıs 2009.
- ^ Muraoka, Hisashi (1995) "Silicon wafer cleaning fluid with HNO3, HF, HCl, surfactant, and water" ABD patent 5.635.463
- ^ Fischer, A. H.; Jacobson, K. A.; Rose, J.; Zeller, R. (1 Mayıs 2008). "Preparation of Slides and Coverslips for Microscopy". Cold Spring Harbor Protocols. 2008 (6): pdb.prot4988. doi:10.1101/pdb.prot4988. PMID 21356831.
- ^ Curtis, Heber D. (Şubat 1911). "Methods of Silvering Mirrors". Publications of the Astronomical Society of the Pacific. 23 (135): 13. Bibcode:1911PASP...23...13C. doi:10.1086/122040.
- ^ O’Neal, Carol L; Crouch, Dennis J; Fatah, Alim A (Nisan 2000). "Validation of twelve chemical spot tests for the detection of drugs of abuse". Forensic Science International. 109 (3): 189-201. doi:10.1016/S0379-0738(99)00235-2. PMID 10725655.
- ^ May, Paul (Kasım 2007). "Nitric acid". 6 Kasım 2007 tarihinde kaynağından arşivlendi. Erişim tarihi: 28 Mayıs 2009.
- ^ "Nitric acid: Toxicological overview". Health Protection Agency. 27 Temmuz 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Aralık 2011.
- ^ Ahmad Y. Al-Hassan, Cultural contacts in building a universal civilisation: Islamic contributions, published by O.I.C. Research Centre for Islamic History, Art and Culture in 2005 13 Temmuz 2020 tarihinde Wayback Machine sitesinde arşivlendi. and available online at History of Science and Technology in Islam 29 Aralık 2015 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ a b
 Chisholm, Hugh, (Ed.) (1911). "Nitric Acid". Encyclopædia Britannica. 19 (11. bas.). Cambridge University Press. ss. 711–712.
Chisholm, Hugh, (Ed.) (1911). "Nitric Acid". Encyclopædia Britannica. 19 (11. bas.). Cambridge University Press. ss. 711–712.
- ^ Davy, John, (Ed.) (1839). "On Some Chemical Agencies of Electricity". The Collected Works of Sir Humphry Davy. 5. ss. 1-12.
- ^ a b Mellor, J. W. (1918). Modern Inorganic Chemistry. Longmans, Green and Co. s. 509.
- ^ Martin, Geoffrey; Barbour, William (1915). Industrial Nitrogen Compounds and Explosives. Crosby Lockwood and Son. s. 21.
- ^ Knox, Joseph (1914). The Fixation of Atmospheric Nitrogen. D. Van Nostrand Company. ss. 45-50.
- ^ a b Dary, G. (1913). "The Production of Nitrates by the Direct Electrolysis of Peat Deposits". London Electrical Review. 73: 1020-1021.
- ^ Hale, Arthur (1919). The Manufacture of Chemicals by Electrolysis. D. Van Nostrand Co. ss. 30-32. Erişim tarihi: 15 Eylül 2019.
Dış bağlantılar[değiştir | kaynağı değiştir]
- Kimyasal Tehlikeler için NIOSH Cep Rehberi5 Ağustos 2020 tarihinde Wayback Machine sitesinde arşivlendi.
- Ulusal Kirletici Envanteri - Nitrik Asit Bilgi Formu28 Mayıs 2013 tarihinde Wayback Machine sitesinde arşivlendi.
- Hesaplayıcılar:Nitrik asit çözeltilerinin yüzey gerilimleri22 Şubat 2020 tarihinde Wayback Machine sitesinde arşivlendi. ve yoğunlukları, molariteleri ve molaliteleri22 Şubat 2020 tarihinde Wayback Machine sitesinde arşivlendi.