Kral suyu
| |
| Adlandırmalar | |
|---|---|
nitrik asit hidroklorür | |
Diğer adlar aqua regia, nitrohidroklorik asit | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
PubChem CID
|
|
CompTox Bilgi Panosu (EPA)
|
|
| |
| Özellikler | |
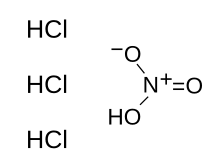
| Molekül formülü | HNO3+3 HCl |
| Görünüm | kırmızı, sarı ya da altın renginde dumanlı sıvı |
| Yoğunluk | 1.01–1.21 g/cm3 |
| Erime noktası | −42 °C |
| Kaynama noktası | 108 °C |
| Çözünürlük (su içinde) | suda çözünür |
| Buhar basıncı | 21 mbar |
| Tehlikeler | |
| NFPA 704 (yangın karosu) |
|
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |


Kral suyu (Latince: Aqua Regia), asitlerin az etki ettiği ya da etki etmediği altın ve platin gibi metallerle tepkimeye girebilen kuvvetli bir asit çözeltisidir. Hidroklorik asit ve nitrik asitin 3:1 oranında karıştırılmasıyla oluşur. Ebu Musa Câbir bin Hayyan tarafından bulunduğu tahmin edilmektedir.
3 HCl + HNO3 → NOCl (aq) + Cl2 (aq) + 2 H2O (l)
- Au (s) + 3 NO-3(aq) + 6 H+ (aq) → Au3+ (aq) + 3 NO2 (g) + 3 H2O (l) ve
- Au3+(aq) + 4 Cl- (aq) → [AuCl4]- (aq).
En güçlü oksidanlardan biri olan nitrik asit, altının çok ufak neredeyse ölçülemez bir miktarını çözüp altın iyonuna dönüştürür. Ortamdaki hidroklorik asit ise bu altın iyonlarıyla birleşir. Altın iyonları eksildiğinden denge hali bozulur, bu da daha fazla altının çözünmesine yol açar. Cabir Bin Hayyam bu karışımı kullanarak altın, platin gibi maddeleri çözmüştür.
Platinin Kral Suyunda çözünmesi[değiştir | kaynağı değiştir]
Altının Kral suyu ile verdiği reaksiyona benzer denklemler platin için de yazılabilir. Altında olduğu gibi yükseltgenme reaksiyonu sonunda ürün olarak azot dioksit veya azot oksit açığa çıkabilir.
Pt (s) + 4 NO-3 (sulu) + 8 H + (sulu) → Pt4 + (sulu) + 4 NO2 (g) + 4 H2O(s)
3Pt (s) + 4 NO-3 (sulu) + 16 H + (sulu) → 3Pt4 + (sulu) + 4 NO (g) + 8 H2O (s)
Yükseltgenen platin iyonu sonra klorür iyonları reaksiyona sokularak kloroplatinat iyonu oluşması sağlanır.
Pt4 + (sulu) + 6 CI (sulu) → PtCl2-6 (sulu)
Deneysel kanıtlar kral suyu ile platinin reaksiyonunun çok karmaşık olduğunu ortaya koymaktadır. İlk etapta sıvı haldeki platinden kloroplatinik asit (H2PtCl4) ve nitroplatin klorür ((NO) 2PtCl4) 'den oluşan bir karışım üretilir.
Üretilen nitroplatinklorür katı üründür. Platinin tam çözünmesi arzu edilirse, derişik hidroklorik asit ile katı kalıntıların tekrar ekstraksiyonu gerçekleştirilmelidir.
2Pt (k) + 2HNO3 (sulu) + 8 HCI (sulu) → (NO) 2PtCl4 (k) + H2PtCl4 (sulu) + 4 H2O (I)
(NO) 2PtCl4 (k) + 2 HCI (sulu) ⇌ H2PtCl4 (sulu) + 2 NOCl (g)
Kloroplatinik asit ısıtırken çözelti klorla doyurularak kloroplatinik asite yükseltgenebilir.[1]
Sonuç olarak;
Platinin genellikle asitlerle reaksiyon vermediği bilinir. Ancak sıcak kral suyu ile kloroplatinik asit oluşturur. Reaksiyon aşağıdaki gibidir.[2]
Pt + 4 HNO3 + 6 HCl → H2PtCl6 + 4 NO2 + 4 H2O Bakınız Resim 3.

Ayrıca bakınız[değiştir | kaynağı değiştir]
Kaynakça[değiştir | kaynağı değiştir]
- Özel
- ^ George B. Kauffman; Larry A. Teter; Rhoda, Richard N. (1963). "Recovery of Platinum from Laboratory Residues". Inorg. Synth. Inorganic Syntheses. 7: 232. doi:10.1002/9780470132388.ch61. ISBN 9780470132388
- ^ Kauffman, George B.; Thurner, Joseph J.; Zatko, David A. (1967). "Ammonium Hexachloroplatinate(IV)". Inorganic Syntheses. Inorganic Syntheses. 9: 182–185. doi:10.1002/9780470132401.ch51. ISBN 978-0-470-13240-1.
- Genel
- Chemistry Comes Alive! Aqua Regia26 Eylül 2011 tarihinde Wayback Machine sitesinde arşivlendi.
- Aqua Regia 9 Eylül 2015 tarihinde Wayback Machine sitesinde arşivlendi. Periyodik Tablo Videoları (Nottingham Üniversitesi)
- Altın Paranın Asit (Kral Suyu)te Eritilme Gösterisi 10 Temmuz 2015 tarihinde Wayback Machine sitesinde arşivlendi.

