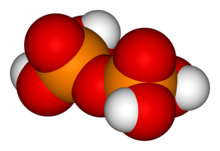
Pirofosforik asit

| |
| |
Diğer adlar Difosforik asit | |
| Tanımlayıcılar | |
|---|---|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.017.795 |
PubChem CID
|
|
CompTox Bilgi Panosu (EPA)
|
|
| Özellikler | |
| Molekül formülü | H4P2O7 |
| Molekül kütlesi | 177.97 g/mol |
| Erime noktası | 71.5 °C (160.7 °F) |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Difosforik asit olarak da bilinen pirofosforik asit, H4P2O7 formülüne sahip inorganik bir bileşik veya daha açıklayıcı olarak [(HO)2P(O)]2O'dur. Renksiz ve kokusuzdur, su, dietil eter ve etil alkolde çözünür. Susuz asit, 54.3 °C ve 71.5 °C'de eriyen iki polimorf içinde kristalleşir. Bileşik, polifosforik asit ve pirofosfat anyonunun konjugat asidinin bir bileşeni olması dışında özel olarak yararlı değildir. Pirofosforik asit anyonları, tuzları ve esterlerine pirofosfatlar denir.
Hazırlık
[değiştir | kaynağı değiştir]En iyi hazırlık, sodyum pirofosfattan iyon değişimi veya kurşun pirofosfatın hidrojen sülfür ile muamele edilmesidir. Fosforik asidin dehidrasyonu ile hazırlanmaz. Bunun yerine, pirofosforik asit ürünlerden sadece biri olarak üretilir.
Reaksiyonlar
[değiştir | kaynağı değiştir]Erimiş olduğu zaman, pirofosforik asit hızla fosforik asit, pirofosforik asit ve polifosforik asitlerin bir denge karışımını oluşturur. Pirofosforik asidin ağırlıkça yüzdesi %40 civarındadır ve eriyikten tekrar kristalleşmesi zordur. Sulu çözeltide pirofosforik asit, tüm polifosforik asitler gibi, hidrolizler ve nihayetinde fosforik asit pirofosforik asit ve polifosforik asitler arasında bir denge kurulur.[1]
- H4P2O7 + H2O ⇌ 2H3PO4
Pirofosforik asit orta güçlü bir inorganik asittir.
Güvenlik
[değiştir | kaynağı değiştir]Pirofosforik asit aşındırıcı olsa da, başka türlü toksikliği olduğu bilinmemektedir.[2]
Tarih
[değiştir | kaynağı değiştir]Pirofosforik asit adı, bir sodyum fosfat tuzunun kırmızı ısısına ısıtılmasının ardından keşfi ile tanınan bir "Glasgowlu Bay Clarke" tarafından verildi. Fosforik asidin kırmızı ısıya ısıtıldığında sıcak su ile kolayca fosforik aside dönüştürülen pirofosforik asit oluşturduğu bulunmuştur.[3]
Kaynakça
[değiştir | kaynağı değiştir]- ^ Corbridge, D. (1995). "Chapter 3: Phosphates". Studies in inorganic Chemistry vol. 20. Elsevier Science B.V. pp. 169–305. doi:10.1016/B978-0-444-89307-9.50008-8. ISBN 0-444-89307-5.
- ^ Material Safety Data Sheet: Pyrophosphoric acid MSDS 3 Mart 2016 tarihinde Wayback Machine sitesinde arşivlendi. www.sciencelab.com
- ^ Beck, Lewis Caleb (1834). A Manual of Chemistry: Containing a Condensed View of the Present State of the Science, with Copious References to More Extensive Treatises, Original Papers, Etc. E.W & C Skinner. p. 160. Retrieved January 30, 2015.
