Vanadyum: Revizyonlar arasındaki fark
| [kontrol edilmiş revizyon] | [kontrol edilmiş revizyon] |
+ |
|||
| 114. satır: | 114. satır: | ||
=== Organometalik bileşikler === |
=== Organometalik bileşikler === |
||
Vanadyumun [[Organovanadyum kimyası|organometalik bileşiklerinden]] olan [[vanadosen diklorür]], uçucu bir başlatıcı reaktiftir.<ref name="wilkinson">{{cite journal |last1=Wilkinson |first1=G. |last2=Birmingham |first2=J. M. |date=Eylül 1954 |title=Bis-cyclopentadienyl Compounds of Ti, Zr, V, Nb and Ta |journal=Journal of the American Chemical Society |volume=76 |issue=17 |pages=4281-4284 |doi=10.1021/ja01646a008 |dil=en}}</ref> [[Vanadyum karbonil]] (V(CO)<sub>6</sub>), [[paramanyetizma|paramanyetik]] bir [[metal karbonil]]dir.<ref>{{cite journal |last1=Bellard |first1=S. |last2=Rubinson |first2=K. A. |last3=Sheldrick |first3=G. M. |date=15 February 1979 |title=Crystal and molecular structure of vanadium hexacarbonyl |journal=Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry |volume=35 |issue=2 |pages=271-274 |dil=en |doi=10.1107/S0567740879003332}}</ref><ref>{{cite book |last=Elschenbroich |first=C. |title=Organometallics: A Concise Introduction |author2=Salzer A. |date=1992 |publisher=Wiley-VCH |isbn=978-3-527-28165-7 |dil=en}}</ref> |
Vanadyumun [[Organovanadyum kimyası|organometalik bileşiklerinden]] olan [[vanadosen diklorür]], uçucu bir başlatıcı reaktiftir.<ref name="wilkinson">{{cite journal |last1=Wilkinson |first1=G. |last2=Birmingham |first2=J. M. |date=Eylül 1954 |title=Bis-cyclopentadienyl Compounds of Ti, Zr, V, Nb and Ta |journal=Journal of the American Chemical Society |volume=76 |issue=17 |pages=4281-4284 |doi=10.1021/ja01646a008 |dil=en}}</ref> [[Vanadyum karbonil]] (V(CO)<sub>6</sub>), [[paramanyetizma|paramanyetik]] bir [[metal karbonil]]dir.<ref>{{cite journal |last1=Bellard |first1=S. |last2=Rubinson |first2=K. A. |last3=Sheldrick |first3=G. M. |date=15 February 1979 |title=Crystal and molecular structure of vanadium hexacarbonyl |journal=Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry |volume=35 |issue=2 |pages=271-274 |dil=en |doi=10.1107/S0567740879003332}}</ref><ref>{{cite book |last=Elschenbroich |first=C. |title=Organometallics: A Concise Introduction |author2=Salzer A. |date=1992 |publisher=Wiley-VCH |isbn=978-3-527-28165-7 |dil=en}}</ref> |
||
== Doğal oluşumu == |
|||
[[Dosya:Vanadinite - ACF mine, Mibladen, Morocco.jpg|thumb|[[Fas]]'ta bulunan bir [[vanadinit]] parçası]] |
|||
Vanadyum, [[Dünya'nın yerkabuğu|Yerkabuğu]]'ndaki [[Kimyasal elementlerin Dünya'nın yerkabuğundaki bollukları|en bol bulunan]] 20. elementtir.<ref>{{cite book |url=https://books.google.com/books?id=WV5EAAAAYAAJ&q=vanadium+20th+most+common+element+in+Earth's+crust |title=Proceedings |date=1991 |publisher=National Cotton Council of America |dil=en}}</ref><ref>{{cite journal |son1=Ostrooumov |ilk1=M. |son2=Taran |ilk2=Y. |year=2015 |title=Discovery of Native Vanadium, a New Mineral from the Colima Volcano, State of Colima (Mexico) |url=https://www.uhu.es/fexp/sem2015/arc/macla/macla_20_109-110.pdf |url-status=live |journal=Revista de la Sociedad Española de Mineralogía |volume=20 |pages=109-110 |archive-url=https://web.archive.org/web/20230207070847/https://www.uhu.es/fexp/sem2015/arc/macla/macla_20_109-110.pdf |archive-date=7 Şubat 2023 |dil=en}}</ref><ref>{{cite web |title=Vanadium: Vanadium mineral information and data |url=https://www.mindat.org/min-43604.html |dil=en |archive-url=https://web.archive.org/web/20210716205934/https://www.mindat.org/min-43604.html |archive-date=16 Temmuz 2021 |website=Mindat.org}}</ref> 20. yüzyılın başlarında; Junín, [[Cerro de Pasco]], [[Peru]] yakınlarındaki [[Ragra Madenleri]]'nde bir vanadyum cevheri keşfedildi.<ref>{{cite journal |last1=Hillebrand |first1=W. F. |year=1907 |title=The Vanadium Sulphide, Patronite, and ITS Mineral Associates from Minasragra, Peru |url=https://zenodo.org/record/1450154 |url-status=live |journal=Journal of the American Chemical Society |volume=29 |issue=7 |pages=1019-1029 |dil=en |doi=10.1021/ja01961a006 |archive-url=https://web.archive.org/web/20210911093143/https://zenodo.org/record/1450154 |archive-date=11 September 2021 |access-date=6 September 2020}}</ref><ref>{{cite journal |last1=Hewett |first1=F. |year=1906 |title=A New Occurrence of Vanadium in Peru |journal=The Engineering and Mining Journal |volume=82 |issue=9 |pages=385}}</ref><ref name="scielo">{{cite journal |last1=Steinberg |first1=W.S. |last2=Geyser |first2=W. |last3=Nell |first3=J. |year=2011 |title=The history and development of the pyrometallurgical processes at Evraz Highveld Steel & Vanadium |url=http://www.scielo.org.za/pdf/jsaimm/v111n10/v111n10a09.pdf |url-status=live |journal=The Journal of the Southern African Institute of Mining and Metallurgy |volume=111 |pages=705-710 |archive-url=https://web.archive.org/web/20210911093146/http://www.scielo.org.za/pdf/jsaimm/v111n10/v111n10a09.pdf |archive-date=11 September 2021 |access-date=17 December 2018}}</ref> Bu dönemlerde [[patronit]] (VS<sub>4</sub>), vanadyum elde ediliminde kullanılan başlıca mineraldi.<ref>{{cite web |title=mineralogical data about Patrónite |url=https://www.mindat.org/min-3131.html |url-status=live |archive-url=https://web.archive.org/web/20210430004309/https://www.mindat.org/min-3131.html |archive-date=30 April 2021 |access-date=19 January 2009 |publisher=mindata.org}}</ref> 1920 itibarıyla, dünyadaki vanadyum üretiminin yaklaşık üçte ikisi bu madende gerçekleştiriliyordu.<ref>{{cite journal |last1=Allen |first1=M. A. |last2=Butler |first2=G. M. |date=1921 |title=Vanadium |url=https://repository.arizona.edu/bitstream/handle/10150/630042/b-115_vanadium.pdf |url-status=live |journal=University of Arizona |archive-url=https://web.archive.org/web/20210427182032/https://repository.arizona.edu/bitstream/handle/10150/630042/b-115_vanadium.pdf |archive-date=27 April 2021 |access-date=20 January 2020}}</ref> 1910 ve 1920'lerde [[karnotit]]ten ({{nowrap|K<sub>2</sub>(UO<sub>2</sub>)<sub>2</sub>(VO<sub>4</sub>)<sub>2</sub>·3H<sub>2</sub>O}}) [[uranyum]] üretimi başlayınca, vanadyum da bu süreçte ortaya çıkan bir ara ürün olarak elde edilmeye başlandı. Vanadinit ve diğer vanadyum içeren mineraller, yalnızca istisnai durumlarda çıkarılmaya başlandı. Elemente olan talebin artmasıyla, günümüzde dünyadaki vanadyum üretiminin çoğu,[[Ultramafik kayaç|ultramafik]] [[gabro]] yığınlarındaki vanadyum barındıran [[magnatit]]ten elde edilir. Bu magnatit [[demir]] üretiminde kullanılırsa, vanadyumun çoğu [[cüruf]]a gider ve buradan ayrılştırılır.<ref>{{cite journal |last1=Hukkanen |first1=E. |last2=Walden |first2=H. |year=1985 |title=The production of vanadium and steel from titanomagnetites |journal=International Journal of Mineral Processing |volume=15 |issue=1-2 |pages=89-102 |dil=en |bibcode=1985IJMP...15...89H |doi=10.1016/0301-7516(85)90026-2}}</ref><ref name="scielo" /> |
|||
== Üretimi == |
== Üretimi == |
||
Sayfanın 02.27, 5 Aralık 2023 tarihindeki hâli
 Farklı dokulardaki %99 saflıktaki üç vanadyum kristal çubuğu ile %99,95 saflıktaki 1 cm3 hacmindeki bir vanadyum küpü | ||||||||||||||||||||||||||||
| Görünüş | Mavi-gümüşi-gri metal | |||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Standart atom ağırlığı Ar, std(V) | 50,9415(1) | |||||||||||||||||||||||||||
| Periyodik tablodaki yeri | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
| Atom numarası (Z) | 23 | |||||||||||||||||||||||||||
| Grup | 5. grup | |||||||||||||||||||||||||||
| Periyot | 4. periyot | |||||||||||||||||||||||||||
| Blok | d bloku | |||||||||||||||||||||||||||
| Elektron dizilimi | [Ar] 3d3 4s2 | |||||||||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 11, 2 | |||||||||||||||||||||||||||
| Fiziksel özellikler | ||||||||||||||||||||||||||||
| Faz (SSB'de) | Katı | |||||||||||||||||||||||||||
| Erime noktası | 2183 K ({{{erime_noktası_C}}} °C, {{{erime_noktası_F}}} °F) | |||||||||||||||||||||||||||
| Kaynama noktası | 3680 K (3407 °C; 6164,6 °F) | |||||||||||||||||||||||||||
| Yoğunluk (OS) | 6,11 g/cm3 | |||||||||||||||||||||||||||
| sıvıyken (en'de) | 5,5 g/cm3 | |||||||||||||||||||||||||||
| Erime entalpisi | 21,5 kJ/mol | |||||||||||||||||||||||||||
| Buharlaşma entalpisi | 444 kJ/mol | |||||||||||||||||||||||||||
| Molar ısı kapasitesi | 24,89 J/(mol·K) | |||||||||||||||||||||||||||
Buhar basıncı
| ||||||||||||||||||||||||||||
| Atom özellikleri | ||||||||||||||||||||||||||||
| Yükseltgenme durumları | -3, -1, 0, +1, +2, +3, +4, +5 (amfoter oksit) | |||||||||||||||||||||||||||
| Elektronegatiflik | Pauling ölçeği: 1,61 | |||||||||||||||||||||||||||
| İyonlaşma enerjileri |
| |||||||||||||||||||||||||||
| Atom yarıçapı | Deneysel: 134 pm | |||||||||||||||||||||||||||
| Kovalent yarıçapı | 153±8 pm | |||||||||||||||||||||||||||
| Diğer özellikleri | ||||||||||||||||||||||||||||
| Kristal yapı | Hacim merkezli kübik (hmk) | |||||||||||||||||||||||||||
| Ses hızı | 4560 m/s | |||||||||||||||||||||||||||
| Genleşme | 8,4 µm/(m·K) | |||||||||||||||||||||||||||
| Isı iletkenliği | 30,7 W/(m·K) | |||||||||||||||||||||||||||
| Elektrik direnci | 197 Ω·m | |||||||||||||||||||||||||||
| Manyetik düzen | Paramanyetik | |||||||||||||||||||||||||||
| Manyetik alınganlık | +255,0 × 10-6 cm3/mol | |||||||||||||||||||||||||||
| Young modülü | 128 GPa | |||||||||||||||||||||||||||
| Kayma modülü | 47 GPa | |||||||||||||||||||||||||||
| Hacim modülü | 160 GPa | |||||||||||||||||||||||||||
| Poisson oranı | 0,37 | |||||||||||||||||||||||||||
| Mohs sertliği | 6,7 | |||||||||||||||||||||||||||
| Vickers sertliği | 628-640 MPa | |||||||||||||||||||||||||||
| Brinell sertliği | 600-742 MPa | |||||||||||||||||||||||||||
| CAS Numarası | 7440-62-2 | |||||||||||||||||||||||||||
| Tarihi | ||||||||||||||||||||||||||||
| Adını aldığı | Vanadís | |||||||||||||||||||||||||||
| Keşif | Andrés Manuel del Río (1801) | |||||||||||||||||||||||||||
| İlk izolasyon | Henry Roscoe (1867) | |||||||||||||||||||||||||||
| Adlandıran | Nils Gabriel Sefström (1830) | |||||||||||||||||||||||||||
| Ana izotopları | ||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||
Vanadyum, simgesi V, atom numarası 23 olan bir elementtir. Bir geçiş metali olan element, doğada nadiren bulunur. Yapay olarak izole edildiğinde, oksit bir katmanın ortaya çıkmasıyla pasifleşir ve kararlı hâle gelen elementin oksitlenmesi sona erer.
Andrés Manuel del Río tarafından 1801 yılında vanadinit mineralinin (Pb5(VO4)3Cl) analizi sırasında keşfedildi ve erythronium adı verildi. Ancak bir süre sonra erythronium ile kromun aslında aynı element oldukları fikri kabul gördü. 1831 yılında Nils Gabriel Sefström, vanadyumun keşfedilmemiş bir element olduğunu ispatladı ve İskandinav güzellik ve bereket tanrıçası Vanadis'in (Freyja olarak da bilinir) adını verdi.

Element doğada 65 farklı mineralde bileşik halinde bulunur. Çin ve Rusya'da çelik üretiminde ortaya çıkan cürufun işlenmesi ile, diğer ülkelerde ise ağır yağ baca tozunun geridönüşümü ya da uranyum madenciliğinin bir yan ürünü olarak üretir. Özellikle yüksek hız çeliği benzeri yüksek alaşımlı çeliklerin üretiminde kullanılır. Vanadyum pentoksit (V2O5) bileşiği sülfürik asit üretimi için bir katalizördür. Çoğu canlıda bulunan vanadyum, bazı enzimlerin etkin bölgesi olarak kullanılır.
Tarihi
1801'de, Meksika'daki bir "kahverengi kurşun" (daha sonraları vanadinit olarak adlandırıldı) örneğinden bu elementi ayrıştıran Andrés Manuel del Río tarafından keşfedildi. Del Río, tuzlarının çeşitli renkler taşıdığını gözlemlediği elementi Yunancada "tüm renkler" anlamı taşıyan παγχρώμιο (panhromio) kelimesinden türetilen pankromyum olarak adlandırdı. Sonrasında ise, tuzların çoğunun ısıtıldığında kırmızı rengi almasından ötürü elemente, Yunancada "kırmızı" anlamına gelen ερυθρός (erutrhos) kelimesinden türettiği erithronyum adını verdi. Del Río'nun arkadaşı Alexander von Humboldt'un desteklediği Hippolyte-Victor Collet-Descotils 1805'te, hatalı bir şekilde bu elementin, saf olmayan bir krom örneği olduğunu öne sürdü. Collet-Descotils'in bu görüşünü kabul eden Del Río, elementin keşfine dair iddiasını geri çekti.[1]
1831'de Nils Gabriel Sefström, demir cevherleriyle çalışırken bulduğu yeni bir oksitte elementi tekrar keşfetti. Yılın ilerleyen dönemlerinde Friedrich Wöhler, bu elementin del Río'nun 1801'de bulduğu elementle aynı olduğunu doğruladı.[2] Daha önce hiçbir elementin ilk harfi olarak kullanılmayan V harfiyle başlayan bir isim arayışına giren Sefström, elementin meydana getirdiği "güzel renkli" bileşiklere atfen, İskandinav mitolojisideki güzellik ve bereket tanrıçası Vanadís'ten türettiği vanadyum isminde karar kıldı.[2] Wöhler'in tespitinden haberdar olan del Río, kendi çalışmasının kabulünü sağlasa da elementin adı vanadyum olarak kaldı.[3] 1831'de George William Featherstonhaugh'nun, elementin adının del Río'ya atfen "riyonyum" olması yönündeki önerisi kabul görmedi.[4]
Başka elementlerle birlikte bulunmasından ötürü, keşfinin ilk dönemlerinde vanadyumun izole edilmesi konusunda birtakım zorluklar yaşanıyordu.[5] 1831'de Jacob Berzelius elementi ürettiğini kaydetse de Henry Enfield Roscoe, Berzelius'un vanadyum nitrür (VN) elde ettiğini gösterdi. 1867'de Roscoe, vanadyum(II) klorürü (VCl2) hidrojen (H) ile indirgeyerek elementi elde etti.[6] 1927'de, vanadyum pentoksidin (V2O5) kalsiyum (Ca) ile indirgenmesi sonucunda saf vanadyum elde edildi.[7]
Vanadyumun ilk geniş çaplı endüstriyel kullanımı, Ford Model T'nin alaşımlı çelik şasisinde oldu. Vanadyumun eklenmesiyle çeliğin kütlesi azalırken çekme mukavemeti artmıştı.[8] 1900'lerde elde edilen vanadyumun çoğu, American Vanadium Company tarafından Peru'daki Ragra Madeni'nden çıkarılıyordu. İlerleyen dönemde uranyuma olan talebin artması, elde edilen vanadyumum da artmasına yol açtı. Uranyumun elde edildiği başlıca minerallerden karnotit (K2(UO2)2(VO4)2), vanadyum da içeriyordu ve uranyum elde edilirken vanadyum da yan ürün olarak elde ediliyordu.[9][10]
1911'de Martin Henze, Ascidiacea üyelerinin kan hücrelerinde (ya da sölom hücrelerinde), vanadyum içeren hemovanadin proteinlerini keşfetti.[11][12]
Özellikleri
Sünek bir geçiş metali olan vanadyumun mavi-gümüşi-gri renkli, metalik bir görünümü vardır. Elektriksel açıdan iletken, ısıl açıdan yalıtkandır.[13][14] 6,7 Mohs sertliği değerine sahip olup korozyona karşı dirençli, alkaliler ile sülfürik ve hidroklorik asitlere karşı kararlıdır.[15] 933 K (660 °C; 1220 °F) kadar sıcaklıktaki havada oksitlenirken oda sıcaklığında dahi oksit bir katmanın ortaya çıkmasıyla pasifleşerek kararlı hâle gelir.[16]
İzotopları
Doğada vanadyum, kararlı bir izotop olan 51V ya da radyoizotop olan 50V şeklinde bulunur. 2,71 × 1017 yıllık yarı ömre sahip 50V izotopunun doğal bolluğu %0,25'tir. Doğal bolluğu %99,75 olan 51V izotopunun çekirdek spini 7⁄2'dir. Elementin, kütle numarası 40 ilâ 65 arasında değişen 24 yapay radyoizotopu sentezlentir. 330 günlük yarı ömre sahip 49V ile 16 günlük yarı ömre sahip 48V en kararlı iki yapay radyoizotopu iken kalan radyoizotopların yarı ömürleri bir saatten kısadır. En az dört izotopunun yarı kararlı uyarılmış durumları vardır.[17] 51V'den daha hafif izotopların ana bozunma türü elektron yakalanması, daha ağır izotopların ise beta bozunmasıdır.[18] Elektron yakalanma reaksiyonları, titanyum (Ti) izotoplarının, beta bozunmaları ise krom (Cr) izotoplarının oluşmasıyla sonuçlanır.
Bileşikleri

Vanadyum, -2 hariç olmak üzere -3 ile +5 arasındaki yükseltgenme durumlarının tamamında bulunabilir. Sulu bir çözeltide element; pH değerine göre [V(H2O)6]2+ formülüyle lila, [V(H2O)6]3+ formülüyle yeşil, [VO(H2O)5]2+ formülüyle mavi ya da [VO(H2O)5]3+ formülüyle sarı-turuncu renkli bir metal-su bileşiği oluşturur. Vanadyum(II) bileşikleri indirgen, vanadyum(V) bileşikleri ise yükseltgendir. Vanadyum(IV) bileşikleri genellikle, merkezinde VO2+ bulunan vanadil türevleri şeklindedir.[15]
Amonyum vanadat(V) (NH4VO3), çinko (Zn) ile indirgenilerek vanadyumun +2 ile +5 arasındaki yükseltgenme durumlarındaki farklı renkleri almasını sağlayabilir. Daha düşük yükseltgenme durumları, V(CO)6, [V(CO)6]- ya da benzer bileşiklerde görülür.[15] Vanadyum pentoksit, sülfürik asit üretimi için ticari değeri olan bir katalizördür.[15]
Vanadyum redoks pilinin bir elektrodu vanadyumun +5/+4 yükseltgenme durumu çiftini, diğer elektrodu ise +3/+2 çiftini kullanır. Bu yükseltgenme durumları arasındaki dönüşüm, çinko tozu ya da amalgam içeren bir vanadyum(V) bileşiğinin güçlü bir asidik çözeltisinin indirgenmesiyle gözlemlenir. Pervanadilin [VO2(H2O)4]+ neden olduğu başlangıçtaki sarı renk, sonrasında sırasıyla [VO(H2O)5]2+ bileşiğinin mavi, [V(H2O)6]3+ bileşiğinin yeşil ve [V(H2O)6]2+ bileşiğinin mor rengine dönüşür.[15]
Oksianyonlar
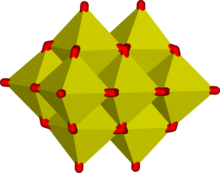
Sulu bir çözeltide vanadyum(V), pH ve yoğunluğa bağlı olmak üzere en az 11 tür oksianyon oluşturur.[19] Dört yüzlü ortovanadat iyonu VO3-4, pH değerinin 12-14 arasında olduğu çözeltilerdeki birincil türdür. Tetratiovanadat [VS4]3-, ortovanadat ile analogdur.[20]
Daha düşük pH değerlerinde, ağırlıklı olarak, vanadyum yoğunluğu 10-2M (toplam vanadyum yoğunluğunun logaritması/M oranının negatif değeri olan pV > 2 olmak kaydıyla) civarından düşük olan monomer [HVO4]2- ile dimer [V2O7]4- barındıran çözeltiler ortaya çıkar.[21][22] pH değeri düştükçe, polivanadatlar oluşturacak şekilde protonlanma ve yoğunlaşma görülür. pH 4-6 aralığındayken pV değerinin 4 civarından yüksek olduğu durumlarda [H2VO4]- baskınken daha yüksek yoğunluklarda trimer ve tetramerler meydana gelir.[23] pH 2-4 arasındayken, ortovanadatın aşağıdaki yoğunlaşma reaksiyonu sonucu oluşturduğu dekavanadat baskındır:
- 10 [VO4]3- + 24 H+ → [V10O28]6- + 12 H2O
Dekavanadattaki her V(V) merkezi, altışar oksit ligandla çevrilidir.[15] Vanadik asit H3VO4, tetrahedral [H2VO4]- bileşiğinin protonlanması sonucunda, öncelikli olarak oktahedral [VO2(H2O)4]+ bileşiğinin oluşmasından ötürü yalnızca çok düşük yoğunluklarda var olur.[24] 2'den düşük pH değerine sahip asidik çözeltilerde, [VO2(H2O)4]+ bileşiği baskınken, yüksek yoğunluklarda çözeltiye dahil olan V2O5, vanadik asidin asit anhidratıdır. Vanadat bileşiklerinin çoğunun yaısı, X ışını kristalografisiyle belirlenir.
Vanadyum(V), bromoperoksidaz enzimlerinin vanadyum içeren etkin alanındakiler gibi çeşitli perokso bileşikler oluşturur. VO(O2)(H2O)4+ bileşiği, asidik çözeltilerde kararlıdır. Alkali çözeltilerde ise 2, 3 ya da 4 peroksit gruplular bilinirken 4 peroksit gruplular; M3V(O2)4 nH2O (M= Li, Na vs) formüllü, mor renkli ve vanadyumun 8 koordinatlı dodekahedron yapıda olduğu tuzlar oluşturur.[25][26]
Halojenür türevleri
Vanadyumun bilinen, VXn (n=2..5) formüllü on iki çift halojenürü mevcuttur.[27] VI4, VCl5, VBr5 ve VI5 var değildir ya da son derece kararsızdır. Diğer reaktiflerle birlikte VCl4, dialkenlerin polimerizasyonunda katalizör olarak kullanılır. Tüm çift halojenürler gibi vanadyum halojenürler de Lewis asididir.[27] Vanadyum halojenürlerin çoğu, VXnL6-n (X=halojenür, L=diğer ligant) formülüyle oktahedral yapılar meydana getirir.
VOmXn formüllü birçok vanadyum oksihalojenür vardır.[28] Vanadyum oksitriklorür (VOCl3) ile vanadyum(V) oksitriflorür (VOF3) uçucu,[29] gazken tetrahedral yapılı ve Lewis asididir.[30]
Koordinasyon bileşikleri

Vanadyum(II) ve (III) bileşikleri indirgen, V(IV) ve V(V) bileşikleri ise yükseltgendir. Vanadyum iyonunun bazı bileşikleri, [V(CN)7]4- örneğindeki gibi 6'dan yüksek koordinasyon sayısına ulaşırlar. Oksovanadyum(V), yükseltgen bromlaşma ve tiyoeter yükseltgenmelerinde kullanılan tetradentat ligandlar ve peroksitlerle birlikte 7 koordinatlı koordinasyon bileşikleri oluştururlar. V4+'ün koordinasyon kimyasında, kendisine güçlü bağlanan dört ligand ile zayıf bağlanan bir ligand olan VO2+ merkezi baskındır. Bu duruma bir örnek teşkil eden vanadil asetilasetonat (V(O)(O2C5H7)2) bileşiğinde vanadyum, 5 koordinatlı ve bozuk bir kare piramit şeklinde olduğundan, piridin gibi altıncı bir ligand bağlanabilse de bu sürecin bağlanma sabiti düşük olur. VOCl2(NMe3)2 gibi 5 koordinatlı vanadil bileşiklerinin çoğu have trigonal bipiramidal yapıdadır.[31] V5+'in koordinasyon kimyasında; genellikle vanadyum(IV) öncüllerinin hava oksitlenmesi sonucu oluşan, +5 yükseltgenme durumunun kararlı hâle gelmesini ve +4 ile +5 yükseltgenme durumları arasındaki dönüşümün kolaylaşmasını sağlayan görece kararlı dioksovanadyum koordinasyon bileşikleri baskındır.[32][33]
Organometalik bileşikler
Vanadyumun organometalik bileşiklerinden olan vanadosen diklorür, uçucu bir başlatıcı reaktiftir.[34] Vanadyum karbonil (V(CO)6), paramanyetik bir metal karbonildir.[35][36]
Doğal oluşumu

Vanadyum, Yerkabuğu'ndaki en bol bulunan 20. elementtir.[37][38][39] 20. yüzyılın başlarında; Junín, Cerro de Pasco, Peru yakınlarındaki Ragra Madenleri'nde bir vanadyum cevheri keşfedildi.[40][41][42] Bu dönemlerde patronit (VS4), vanadyum elde ediliminde kullanılan başlıca mineraldi.[43] 1920 itibarıyla, dünyadaki vanadyum üretiminin yaklaşık üçte ikisi bu madende gerçekleştiriliyordu.[44] 1910 ve 1920'lerde karnotitten (K2(UO2)2(VO4)2·3H2O) uranyum üretimi başlayınca, vanadyum da bu süreçte ortaya çıkan bir ara ürün olarak elde edilmeye başlandı. Vanadinit ve diğer vanadyum içeren mineraller, yalnızca istisnai durumlarda çıkarılmaya başlandı. Elemente olan talebin artmasıyla, günümüzde dünyadaki vanadyum üretiminin çoğu,ultramafik gabro yığınlarındaki vanadyum barındıran magnatitten elde edilir. Bu magnatit demir üretiminde kullanılırsa, vanadyumun çoğu cürufa gider ve buradan ayrılştırılır.[45][42]
Üretimi
Vanadyumun temel mineralleri potasyum uaranil vanadat 2 K(UO2)VO4.3 H2O ve vanadyum sülfürdür. Niobyum ve tantal içerikli mineraller de yüksek miktarda vanadyum bulundurur. Vanadyum mineralinin NaCl veya Na2CO3 ile 850 °C’de reaksiyonu sonucunda elde edilen NaVO3 bileşiği su içerisinde çözülmesi ve çözeltinin kırmızı çökelek verene kadar asitlendirilmesi ile V2O5 oksidi elde edilir. Bu oksidin kalsiyum ile indirgenmesi ile element saf olarak elde edilir. Elementin sentezinde kullanılan diğer bir yöntem ise VCl5 bileşiğinin hidrojen gazı veya magnezyum ile indirgenmesidir.
Kaynakça
- ^ Cintas, Pedro (12 Kasım 2004). "The Road to Chemical Names and Eponyms: Discovery, Priority, and Credit". Angewandte Chemie International Edition (İngilizce). 43 (44): 5888-5894. doi:10.1002/anie.200330074. PMID 15376297.
- ^ a b Sefström, N. G. (1831). "Ueber das Vanadin, ein neues Metall, gefunden im Stangeneisen von Eckersholm, einer Eisenhütte, die ihr Erz von Taberg in Småland bezieht". Annalen der Physik und Chemie (Almanca). 97 (1): 43-49. Bibcode:1831AnP....97...43S. doi:10.1002/andp.18310970103. 10 Eylül 2021 tarihinde kaynağından arşivlendi.
- ^ Marshall, James L.; Marshall, Virginia R. (2004). "Rediscovery of the Elements: The "Undiscovery" of Vanadium" (PDF) (İngilizce). The Hexagon. s. 45. 30 Mart 2023 tarihinde kaynağından (PDF) arşivlendi.
- ^ Featherstonhaugh, George William (1831). "New Metal, provisionally called Vanadium". The Monthly American Journal of Geology and Natural Science (İngilizce): 69.
- ^ Habashi, Fathi (Ocak 2001). "Historical Introduction to Refractory Metals". Mineral Processing and Extractive Metallurgy Review (İngilizce). 22 (1): 25-53. Bibcode:2001MPEMR..22...25H. doi:10.1080/08827509808962488.
- ^ "XIX. Researches on vanadium". Proceedings of the Royal Society of London (İngilizce). 18 (114-122): 37-42. 31 Ocak 1870. doi:10.1098/rspl.1869.0012. 9 Eylül 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Kasım 2023.
- ^ Marden, J. W.; Rich, M. N. (Temmuz 1927). "Vanadium 1". Industrial & Engineering Chemistry (İngilizce). 19 (7): 786-788. doi:10.1021/ie50211a012.
- ^ Betz, Frederick (2003). Managing Technological Innovation: Competitive Advantage from Change (İngilizce). Wiley-IEEE. ss. 158-159. ISBN 978-0-471-22563-8.
- ^ Busch, Phillip Maxwell (1961). Vanadium: A Materials Survey (İngilizce). U.S. Department of the Interior, Bureau of Mines. s. 65. OCLC 934517147. 23 Nisan 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Kasım 2023.
- ^ Wise, James M. (Mayıs 2018). "Remarkable folded dacitic dikes at Mina Ragra, Peru" (İngilizce). 10 Eylül 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Kasım 2018.
- ^ Henze, M. (1911). "Untersuchungen über das Blut der Ascidien. I. Mitteilung". Z. Physiol. Chem. (İngilizce). 72 (5-6): 494-50. doi:10.1515/bchm2.1911.72.5-6.494.
- ^ Michibata, H.; Uyama, T.; Ueki, T.; Kanamori, K. (2002). "Vanadocytes, cells hold the key to resolving the highly selective accumulation and reduction of vanadium in ascidians" (PDF). Microscopy Research and Technique (İngilizce). 56 (6): 421-434. doi:10.1002/jemt.10042. PMID 11921344. 17 Mart 2020 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 23 Kasım 2023.
- ^ Vander Voort, George F. (1984). Metallography, Principles and Practice (İngilizce). ASM International. s. 137. ISBN 978-0-87170-672-0.
- ^ Cardarelli, François (2008). Materials Handbook (İngilizce). Springer. s. 338. ISBN 978-1-84628-668-1.
- ^ a b c d e f Holleman, Arnold F.; Wiberg, Egon; Wiberg, Nils (1985). "Vanadium". Lehrbuch der Anorganischen Chemie (Almanca) (91-100 bas.). Walter de Gruyter. ss. 1071-1075. ISBN 978-3-11-007511-3.
- ^ Nisbett, Edward G. (1986). Steel Forgings: A Symposium Sponsored by ASTM Committee A-1 on Steel, Stainless Steel, and Related Alloys, Williamsburg, VA, 28-30 Nov., 1984 (İngilizce). ASTM International. ISBN 978-0-8031-0465-5.
- ^ Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik (2003). "The NUBASE evaluation of nuclear and decay properties". Nuclear Physics A (İngilizce). 729: 3-128. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S.; Audi, G. (2021). "The NUBASE2020 evaluation of nuclear properties". Chinese Physics C (İngilizce). 45 (3): 030001. doi:10.1088/1674-1137/abddae.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. bas.). Butterworth-Heinemann. s. 984. ISBN 0080379419.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. bas.). Butterworth-Heinemann. s. 988. ISBN 0080379419.
- ^ Crans, Debbie C. (18 December 2015). "Antidiabetic, Chemical, and Physical Properties of Organic Vanadates as Presumed Transition-State Inhibitors for Phosphatases". The Journal of Organic Chemistry (İngilizce). 80 (24): 11899-11915. doi:10.1021/acs.joc.5b02229. PMID 26544762.
- ^ Jung, Sabrina (2018). Speciation of molybdenum- and vanadium-based polyoxometalate species in aqueous medium and gas-phase and its consequences for M1 structured MoV oxide synthesis (Tez) (İngilizce). doi:10.14279/depositonce-7254.
- ^ Cruywagen, J. J. (1999), Sykes, A. G. (Ed.), Protonation, Oligomerization, and Condensation Reactions of Vanadate(V), Molybdate(vi), and Tungstate(vi), Advances in Inorganic Chemistry (İngilizce), 49, Academic Press, ss. 127–182, doi:10.1016/S0898-8838(08)60270-6, ISBN 978-0-12-023649-7
- ^ Tracey, Alan S.; Willsky, Gail R.; Takeuchi, Esther S. (2007-03-19). Vanadium: Chemistry, Biochemistry, Pharmacology and Practical Applications (İngilizce). CRC Press. ISBN 978-1-4200-4614-4.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. bas.). Butterworth-Heinemann. ISBN 0080379419., s. 994.
- ^ Strukul, Giorgio (1992). Catalytic Oxidations with Hydrogen Peroxide as Oxidant (İngilizce). Springer. s. 128. ISBN 978-0-7923-1771-5.
- ^ a b Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. bas.). Butterworth-Heinemann. s. 989. ISBN 0080379419.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. bas.). Butterworth-Heinemann. s. 993. ISBN 0080379419.
- ^ Flesch, Gerald D.; Svec, Harry J. (1 Ağustos 1975). "Thermochemistry of vanadium oxytrichloride and vanadium oxytrifluoride by mass spectrometry". Inorganic Chemistry (İngilizce). 14 (8): 1817-1822. doi:10.1021/ic50150a015.
- ^ Iqbal, Javed; Bhatia, Beena; Nayyar, Naresh K. (March 1994). "Transition Metal-Promoted Free-Radical Reactions in Organic Synthesis: The Formation of Carbon-Carbon Bonds". Chemical Reviews (İngilizce). 94 (2): 519-564. doi:10.1021/cr00026a008.
- ^ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2. bas.). Butterworth-Heinemann. s. 995. ISBN 0080379419.
- ^ Geiser, Jan Nicholas (2019). Development of an improved state-of-charge sensor for the all-vanadium redox flow battery (Tez) (İngilizce). doi:10.22028/D291-29229.
- ^ Nica, Simona; Rudolph, Manfred; Görls, Helmar; Plass, Winfried (Nisan 2007). "Structural characterization and electrochemical behavior of oxovanadium(V) complexes with N-salicylidene hydrazides". Inorganica Chimica Acta (İngilizce). 360 (5): 1743-1752. doi:10.1016/j.ica.2006.09.018.
- ^ Wilkinson, G.; Birmingham, J. M. (Eylül 1954). "Bis-cyclopentadienyl Compounds of Ti, Zr, V, Nb and Ta". Journal of the American Chemical Society (İngilizce). 76 (17): 4281-4284. doi:10.1021/ja01646a008.
- ^ Bellard, S.; Rubinson, K. A.; Sheldrick, G. M. (15 February 1979). "Crystal and molecular structure of vanadium hexacarbonyl". Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry (İngilizce). 35 (2): 271-274. doi:10.1107/S0567740879003332.
- ^ Elschenbroich, C.; Salzer A. (1992). Organometallics: A Concise Introduction (İngilizce). Wiley-VCH. ISBN 978-3-527-28165-7.
- ^ Proceedings (İngilizce). National Cotton Council of America. 1991.
- ^ Ostrooumov, M.; Taran, Y. (2015). "Discovery of Native Vanadium, a New Mineral from the Colima Volcano, State of Colima (Mexico)" (PDF). Revista de la Sociedad Española de Mineralogía (İngilizce). 20: 109-110. 7 Şubat 2023 tarihinde kaynağından (PDF) arşivlendi.
- ^ "Vanadium: Vanadium mineral information and data". Mindat.org (İngilizce). 16 Temmuz 2021 tarihinde kaynağından arşivlendi.
- ^ Hillebrand, W. F. (1907). "The Vanadium Sulphide, Patronite, and ITS Mineral Associates from Minasragra, Peru". Journal of the American Chemical Society (İngilizce). 29 (7): 1019-1029. doi:10.1021/ja01961a006. 11 September 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 September 2020.
- ^ Hewett, F. (1906). "A New Occurrence of Vanadium in Peru". The Engineering and Mining Journal. 82 (9): 385.
- ^ a b Steinberg, W.S.; Geyser, W.; Nell, J. (2011). "The history and development of the pyrometallurgical processes at Evraz Highveld Steel & Vanadium" (PDF). The Journal of the Southern African Institute of Mining and Metallurgy. 111: 705-710. 11 September 2021 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 17 December 2018.
- ^ "mineralogical data about Patrónite". mindata.org. 30 April 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 19 January 2009.
- ^ Allen, M. A.; Butler, G. M. (1921). "Vanadium" (PDF). University of Arizona. 27 April 2021 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 20 January 2020.
- ^ Hukkanen, E.; Walden, H. (1985). "The production of vanadium and steel from titanomagnetites". International Journal of Mineral Processing (İngilizce). 15 (1-2): 89-102. Bibcode:1985IJMP...15...89H. doi:10.1016/0301-7516(85)90026-2.
Konuyla ilgili yayınlar
| Wikimedia Commons'ta Vanadyum ile ilgili ortam dosyaları bulunmaktadır. |
- Slebodnick, Carla; ve diğerleri. (1999). "Modeling the Biological Chemistry of Vanadium: Structural and Reactivity Studies Elucidating Biological Function". Hill, Hugh A. O.; ve diğerleri. (Ed.). Metal Sites in Proteins and Models (İngilizce). Springer. ISBN 978-3-540-65553-4.


