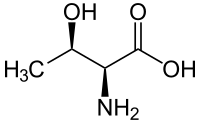
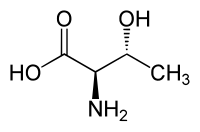
Treonin

| |
| Adlandırmalar | |
|---|---|
Treoninler L-Treonin (sol) D-Treoinin (sağ) | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| ChemSpider | |
| ECHA InfoCard | 100.000.704 |
PubChem CID
|
|
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Molekül formülü | C4H9NO3 |
| Molekül kütlesi | 119,12 g·mol−1 |
| Görünüm | Renksiz ve katı halde bulunur. Kendine has kokusu vardır. |
| Erime noktası | 255–257 °C |
| Çözünürlük (su içinde) | Suda kötü çözülür.(10 g·l−1 20 °C,) Organik çözeltilerde hiçi çözülmez. |
| Tehlikeler | |
| Güvenlik bilgi formu (SDS) | ICSC 1507 |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Treonin (Thr, T) canlıların yapısında yaygın olarak bulunan 20 aminoasitten biridir. Beslenme açısından insanların yiyecekler yoluyla dışarıdan almaları gerekli olan aminoasitlerdendir.
Yapısı
[değiştir | kaynağı değiştir]Treoninde iki optik merkez bulunur, dolayısıyla 4 farklı stereoizomeri olabilir, diğer bir deyişle L-treoninin iki diastereoizomerinin olması mümkündür . Fakat L-treonin ismi yaygın olarak sadece bir enantiomeri için kullanılmaktadır, (2S, 3R)-2-amino-3-hidroksibütanoik asit. Doğada çok nadir olarak bulunan ikinci diastereoizomeri (2S, 3S), L-allo-treonin olarak adlandırılmaktadır.
| Treonin'in çeşitli isomerleri | |
|---|---|
Hücre içi modifikasyonlarla treoninin yan zincirine O-glikozilasyon ile şeker grupları eklenebilir. Treonin, treonin kinaz adlı enzimler vasıtasiyle hidroksil grubundan fosforile (Pi eklenmesi) edilebilir. Fosforile edilmiş haline fosfotreonin de denilmektedir.
Zengin treonin içeriğine sahip olan yiyecekler peynir, et ve balık ürünleri, mercimek ve susamdır. Yetişkin bir insan günlük Treonin ihtiyacı vücut ağırlığının kg başına ortalaması 16 mg'dır.[1]
Bu yazıda ya da bilimsel makalelerde Treonin L- ya da D- olarak hiçbir ön ek almayarak sadece Treonin diye bahsedilmişse, burada bahsi geçen L-Treonin’dir.
Biyosentezi
[değiştir | kaynağı değiştir]Treonin insan vücudu tarafından sentezlenemediği için dışarıdan beslenme yoluyla alınması hayati önem taşımaktadır. Fakat bitkiler ve mikroorganizmaların çoğu aspartik asitten yola çıkarak treonin sentezleyebilme yetisine sahiptirler. Treoninin sentezlenişi sırasındaki kritik aşamalar aşağıdaki şemada özetlenmiştir.
Kaynakça
[değiştir | kaynağı değiştir]- ^ D. H. Baker: "Tolerance for branched-chain amino acids in experimental animals and humans", in: J. Nutr., 2005, 135 (6), S. 1585S–1590S