Bor
Bor simgesi B ve atom numarası 5 olan kimyasal elementtir. Kristal formunda kırılgan, koyu, parlak bir metaloid; amorf formunda kahverengi bir tozdur. Bor grubunun en hafif elementidir, kovalent bağlar oluşturan üç değerlik elektronuna sahiptir, bu da borik asit, mineral sodyum borat, bor karbür ve bor nitrür gibi ultra sert bor kristallerini açıklar.
Bor yıldız nükleosentezi ile değil, tamamen kozmik ışın parçalanması ve süpernovalar tarafından sentezlenir, bu nedenle Güneş Sistemi ve Dünya'nın kabuğunda düşük miktarda bulunan bir elementtir.[1] Yerkabuğunun ağırlıkça yaklaşık yüzde 0,001'ini oluşturur.[2] Doğal olarak, suda çözünür boratların çökelmesi ile yer kabuğunda yoğunlaşmıştır. Bunlar endüstriyel olarak boraks ve kernit gibi evaporitler olarak çıkarılır. Bilinen en büyük yataklar, bor minerallerinin en büyük üreticisi olan Türkiye'de bulunmaktadır.
Elemental bor göktaşlarında küçük miktarlarda bulunan bir metaloiddir, ancak Dünya'da doğal olarak bulunmaz. Endüstriyel olarak, çok saf element karbon veya uzaklaştırılmaya dirençli diğer elementlerle kontaminasyon nedeniyle zorlukla üretilir.[3] Birkaç allotrop mevcuttur: amorf bor, kahverengi bir tozdur; kristalli bor, gümüş rengi ila siyah renktedir, son derece serttir (Mohs ölçeğinde yaklaşık 9,5) ve oda sıcaklığında zayıf bir elektrik iletkenidir. Birincil kullanımı, bazı yüksek mukavemetli malzemelerde karbon elyaflarına benzer uygulamalarla bor filamentleridir.
Bor kimyasal bileşiklerde öncelikli kullanıma sahiptir. Küresel üretimin yaklaşık yarısı, yalıtım ve yapısal malzemeler için cam elyafı katkı maddesi olarak kullanılıyor. Bir sonraki kullanım, yüksek mukavemetli, hafif yapısal ve ısıya dayanıklı malzemelerdeki polimerler ve seramiklerdir. Borosilikat cam, sıradan soda kireç camına göre daha yüksek mukavemet ve termal şok direnci için arzu edilir. Sodyum perborat ağartıcı olarak kullanılır. Küçük bir miktar yarı iletkenlerde katkı maddesi olarak ve organik ince kimyasalların sentezinde reaktif ara madde olarak kullanılır. Bor içeren birkaç organik farmasötik kullanımdadır. Doğal bor, biri (bor-10) nötron yakalama ajanı olarak çeşitli kullanımlara sahip olan iki kararlı izotoptan oluşur.
Borun biyoloji ile kesişimi çok azdır. Memeli yaşamı için gerekli olduğu konusunda fikir birliği yoktur. Boratlar, memelilerde düşük, ancak eklembacaklılarda yüksek toksisite gösterir ve insektisit olarak kullanılabilir. Bor içeren organik antibiyotikler bilinmektedir. Sadece eser miktarda gerekli olmasına rağmen, temel bir bitki besin maddesidir.
Tarih[değiştir | kaynağı değiştir]
Bor kelimesi, izole edildiği mineral olan borakstan, borun kimyasal olarak boraksın karbona benzeliği ile türetilmiştir.

Tinkal olarak bilinen Mineral boraks, MS 300 dolaylarında Çinde sır olarak kullanılmaya başlandı. Bir miktar ham boraks batıya doğru gitti ve MS 700 civarında simyacı Cabir bin Hayyan tarafından ondan bahsedildi. Marco Polo, 13. yüzyılda İtalya'ya bazı sırlar getirdi. Georgius Agricola, MS 1600 civarında, boraksın metalurjide bir akış olarak kullanıldığını bildirdi. Borik asit, İtalya'nın Floransa yakınlarındaki kaplıcalarda (soffioni) 1777'de fark edildi ve tıbbi faydaları olan sal sedativum olarak bilinmeye başlandı. Mineral, İtalya'daki Sasso Pisano'dan sonra sassolit olarak adlandırıldı. Sasso, Amerikan kaynaklarının yerini aldığı 1827'den 1872'ye kadar Avrupa boraksın ana kaynağıydı.[4][5] Bor bileşikleri, 1800'lerin sonlarına kadar, Francis Marion Smith'in Pacific Coast Borax Company'nin bunları ilk kez popüler hale getirip düşük maliyetle hacimli olarak üretmesine kadar nispeten nadiren kullanılıyordu.[6]
Humphry Davy, Gay-Lussac ve Louis Jacques Thénard tarafından izole edilene kadar bor element olarak tanınmadı. 1808'de Davy, bir borat çözeltisinden gönderilen elektrik akımının elektrotlardan birinde kahverengi bir çökelti ürettiğini gözlemledi. Daha sonraki deneylerinde borik asidi azaltmak için elektroliz yerine potasyum kullandı. Yeni elementi doğrulamaya yetecek kadar bor üretti ve buna borakyum adını verdi. Gay-Lussac ve Thénard, borik asidi indirgemek için yüksek sıcaklıklarda demir kullandı. Bor'u hava ile oksitleyerek borik asidin oksidasyon ürünü olduğunu gösterdiler.[7] Jöns Jacob Berzelius, 1824'te onu bir element olarak tanımladı.[8] Saf bor ilk kez 1909'da tartışmasız Amerikalı kimyager Ezekiel Weintraub tarafından üretildi.[9][10][11]
Laboratuarda elemental borun hazırlanması[değiştir | kaynağı değiştir]
Borun eldesi borik oksidin magnezyum veya alüminyum gibi metallerle indirgenmesini içeriyordu. Bununla birlikte, ürün neredeyse her zaman bu metallerin boritleri ile kontamine olur. Saf bor, uçucu bor halojenürlerin yüksek sıcaklıklarda hidrojen ile indirgenmesiyle hazırlanabilir. Yarı iletken endüstrisinde kullanım için ultra saf bor, diboranın yüksek sıcaklıklarda ayrışmasıyla üretilir ve ardından bölge eritme veya Czochralski işlemleriyle saflaştırılır.[12]
Bileşiklerin üretimi boratlar üzerinden yapılabilir.
Özellikler[değiştir | kaynağı değiştir]
Allotroplar[değiştir | kaynağı değiştir]

Bor, kararlı kovalent bağlı moleküler ağlar oluşturma kabiliyeti açısından karbona benzer. Nominal olarakamorf bor bile rastgele birbirine bağlanmış düzenli bor icosahedra içerir.[13][14] Kristalin bor, erime noktası 2000 °C 'in üzerinde olan çok sert, siyah bir malzemedir. Dört ana allotrop oluşturur: α-eşkenar dörtgen ve β-eşkenar dörtgen (α-R ve β-R), γ-ortorombik (γ) ve β-tetragonal (β-T). Dört fazın tümü ortam koşullarında kararlı, β-eşkenar dörtgen en yaygınıdır. Bir α-tetragonal faz da mevcuttur (α-T), ancak önemli bir kontaminasyon olmadan üretilmesi çok zordur. Fazların çoğu B12 ikosahedraya dayalıdır, ancak y fazı, ikosahedra ve B2 atomik çiftlerinin kaya tuzu tipi düzenlemesi olarak tanımlanabilir.[15] Diğer bor fazlarını 1500–1800'°C ye ısıtma ve 12–20'GPa'ya sıkıştırarak üretilebilir. Sıcaklık ve basıncı serbest bıraktıktan sonra sabit kalır. β-T fazı benzer basınçlarda üretilir, ancak daha yüksek 1800–2200 °C sıcaklıklarda üretilebilir, α-T ve β-T fazları ortam koşullarında bir arada bulunabilir, β-T fazı daha kararlıdır.[15][16][17]
Borun 160' GPa üzerinde sıkıştırılması, henüz bilinmeyen bir yapıya sahip bir bor fazı üretir ve bu faz, 6–12 K'nin altındaki sıcaklıklarda bir süper iletkendir.[18] Borosfer (fulleren benzeri B40 molekülleri) ve borofen (önerilen grafen benzeri yapı), 2014 te tanımlandı.
| Bor fazı | α-R | β-R | γ | β-T |
|---|---|---|---|---|
| Simetri | eşkenar dörtgen | eşkenar dörtgen | ortorombik | dörtgen |
| Atomlar/birim hücre [15] | 12 | ~105 | 28 | |
| Yoğunluk (g/cm3) [19][20][21][22] | 2,46 | 2.35 | 2.52 | 2.36 |
| Vickers sertliği (GPa) [23][24] | 42 | 45 | 50–58 | |
| Bulk modülü (GPa)[24][25] | 185 | 224 | 227 | |
| Bant aralığı (eV) [24][26] | 2 | 1.6 | 2.1 |
Elementin kimyası[değiştir | kaynağı değiştir]
Elemental bor nadirdir ve saf malzemenin hazırlanması son derece zor olması sebebiyle yeterince çalışılmamıştır. "Bor" ile ilgili çoğu çalışma, az miktarda karbon içeren numuneleri içerir. Borun kimyasal davranışı alüminyumdan çok silisyuma benzer. Kristal bor, kimyasal olarak inerttir ve hidroflorik veya hidroklorik asitle kaynatılmaya dirençlidir. İnce bir şekilde bölündüğünde, sıcak konsantre hidrojen peroksit, sıcak konsantre nitrik asit, sıcak sülfürik asit veya sıcak sülfürik ve kromik asit karışımı tarafından yavaşça saldırıya uğrar.[10]
Borun oksidasyon hızı kristallik, partikül boyutu, saflık ve sıcaklığa bağlıdır. Bor, oda sıcaklığında hava ile reaksiyona girmez, ancak daha yüksek sıcaklıklarda yanarak bor trioksit oluşturur:[27]
- 4 B + 3 O 2 → 2 B2O3

Bor, trihalidler vermek için halojenlemeye tabi tutulur; Örneğin,
- 2 B + 3 Br2 → 2 BBr3
Pratikte triklorür genellikle oksitten yapılır.[27]
Atomik yapı[değiştir | kaynağı değiştir]
Bor, temel halde p-orbitalinde bir elektrona sahip olan en hafif elementtir. Ancak, diğer pek çok p-elementin aksine, oktet kuralına nadiren uyar ve genellikle valans kabuğuna yalnızca altı elektron[28] (üç moleküler orbitalde ) yerleştirir. Bor, bor grubu (IUPAC grubu,13) için prototiptir, ancak bu grubun diğer üyeleri metaller ve daha tipik p elementleridir.
Kimyasal bileşikler[değiştir | kaynağı değiştir]

En bilinen bileşiklerde bor, formal oksidasyon durumu III'e sahiptir. Bunlar oksit, sülfit, nitrit ve halojenürleri içerir.[27]
Trihalid'ler, düzlemsel bir üçgen yapı benimser. Bu bileşikler, Lewis bazları olarak adlandırılan elektron çifti donörleri ile kolayca adüktler oluşturdukları için Lewis asitleridir. Örneğin, florür (F -) ve bor triflorür (BF3) birleşerek tetrafloroborat anyonu, BF4- verir. Bor triflorür petrokimya endüstrisinde katalizör olarak kullanılmaktadır. Halojenler, borik asit oluşturmak için su ile reaksiyona girer.[27]
Doğada çeşitli B(III) oksitleri olarak bulunur ve genellikle diğer elementlerle birliktedirler. Yüzün üzerinde borat minerali +3 bor içerir. Bu mineraller bazı açılardan silikatlara benzer, ancak oksijenle genellikle sadece dört yüzlü bir koordinasyonda değil, aynı zamanda üçgen düzlemsel bir konfigürasyonda da bulunur. Silikatlardan farklı olarak, bor mineralleri onu asla dörtten büyük koordinasyon sayısı ile içermezler. Tipik bir motif, solda gösterilen ortak mineral boraksın tetraborat anyonlarıdır. Tetrahedral borat merkezinin formal negatif yükü, borakstaki sodyum (Na +) gibi minerallerdeki metal katyonları ile dengelenir.[27] Borat-silikatların turmalin grubu da bor içeren çok önemli bir mineral grubudur ve bir dizi borosilikatın da doğal olarak var olduğu bilinmektedir.[29]
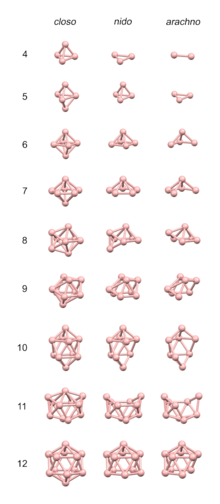
Boranlar genel formülleri BxHy olan bor ve hidrojen bileşikleridir. Bu bileşikler doğada oluşmaz. Boranların birçoğu hava ile temas ettiğinde kolayca oksitlenir, bazıları şiddetli bir şekilde. Ana üye BH3'e boran denir, ancak yalnızca gaz halinde bilinir ve diboran B2H6 oluşturmak için dimerize olur. Daha büyük boranların tümü, bazıları izomerler olarak var olan çok yüzlü bor kümelerinden oluşur. Örneğin, B20H26'nın izomerleri, iki 10 atomlu kümenin füzyonuna dayanır.
En önemli boranlar diboran B2H6 ve piroliz ürünlerinden ikisi, pentaboran B5H9 ve dekaboran B10H14'tür. Çok sayıda anyonik bor hidrit bilinmektedir, örneğin [B12H12]2−.
Boranlarda şekli oksidasyon sayısı pozitiftir ve aktif metal hidritlerde olduğu gibi hidrojen -1 olarak varsayılır. Boronlar için ortalama oksidasyon sayısı, basitçe moleküldeki hidrojenin bora oranıdır. Örneğin, diboran B2H6'da bor oksidasyon durumu +3'tür, ancak dekaboran B10H14'te +1.4'tür. Bu bileşiklerde borun oksidasyon durumu genellikle bir tam sayı değildir.
Bor nitrürler dikkate değer yapılardır. Grafit, elmas ve nanotüpler gibi karbon allotroplarına benzer yapılar sergilerler. Kübik bor nitrür (ticari adı Borazon) olarak adlandırılan elmas benzeri yapıdadır; bor atomları elmastaki karbon atomlarının tetrahedral yapısında bulunur, ancak her dört BN bağından biri, iki elektronun Lewis asidik bor (III) merkezine bağ için Lewis bazı gibi davranan nitrojen atomu tarafından bağışlandığı bir koordine kovalent bağ olarak görülebilir. Diğer uygulamaların yanı sıra kübik bor nitrür, elmasla karşılaştırılabilir bir sertliğe sahip olduğundan (iki madde birbirinin üzerinde çizikler oluşturabilir) aşındırıcı olarak kullanılır. Grafitin BN bileşik analoğunda, altıgen bor nitrür (h-BN), her bir düzlemde pozitif yüklü bor ve negatif yüklü nitrojen atomları, bir sonraki düzlemde zıt yüklü atoma bitişiktir. Sonuç olarak, grafit ve h-BN çok farklı özelliklere sahiptir, ancak her ikisi de yağlayıcıdır, çünkü bu düzlemler kolayca birbirinin yanından geçer. Bununla birlikte, h-BN, düzlemsel yönlerde nispeten zayıf bir elektrik ve termal iletkendir.[31][32]
Organobor kimyası[değiştir | kaynağı değiştir]
Çok sayıda organobor bileşiği bilinmektedir ve birçoğu organik sentezde faydalıdır. Çoğu basit bir boran kimyasalı olan diboran B2H6 kullanan hidroborasyondan üretilir. Organoboron(III) bileşikleri genellikle tetrahedral veya trigonal düzlemseldir, örneğin tetrafenilborat, [B(C6H5)4]- ve trifenilboran, B(C6H5)3. Bununla birlikte, birbiriyle reaksiyona giren çoklu bor atomları, tamamen bor atomlarından veya değişen sayıda karbon heteroatomlarından oluşan yeni on iki yüzlü (12 kenarlı) ve ikosahedral (20 kenarlı) yapılar oluşturma eğilimindedir.
Organoboron kimyasalları, bor karbürden karboranlara, bir süper asit olan karboran asit dahil reaktif yapılar oluşturmak üzere halojenlenebilen karbon-bor küme kimyası bileşiklerine kadar çok çeşitli kullanımlarda kullanılmıştır.
Bir örnek olarak, karboranlar, kanser için bor nötron yakalama tedavisi için bor içeren bileşikleri sentezlemek amacıyla diğer biyokimyasallara önemli miktarlarda bor ekleyen faydalı moleküler parçalar oluşturur.
B(I) ve B(II) Bileşikleri[değiştir | kaynağı değiştir]
Hidrit kümelerinden beklendiği gibi bor, formal oksidasyon durumu üçten az olan kararlı bileşikler oluşturur. B2F4 ve B4Cl4 iyi karakterize edilmiştir.

Metal-bor bileşikleri, negatif oksidasyon durumlarında bor içerir. Örnek, magnezyum diborittir (MgB2). Bileşikte bor atomuna -1, magnezyuma +2 formal yük atanır. Bu malzemede bor merkezleri, grafitteki karbona benzer tabakalar oluşturan her bir bor için ekstra bir çift bağ ile üçgen düzlemseldir. Bununla birlikte, kovalent atomların düzleminde elektronlardan yoksun olan altıgen bor nitrürün aksine, magnezyum diborürdeki delokalize elektronlar, izoelektronik grafite benzer elektrik iletmesine izin verir. 2001 yılında, bu malzemenin yüksek sıcaklıklı bir süper iletken olduğu bulundu.[33][34] Aktif geliştirme aşamasında olan bir süper iletkendir. CERN'de MgB2 kabloları yapmaya yönelik bir proje, büyük hadron çarpıştırıcısının tasarlanan yüksek parlaklık versiyonu gibi son derece yüksek akım dağıtım uygulamaları için 20.000 amper taşıyabilen süper iletken test kabloları ile sonuçlandı.[35]
Bazı diğer metal borürler, kesici takımlar için sert malzemeler olarak özel uygulamalar bulur.[36] Genellikle borürlerdeki bor, kalsiyum hekzaboritte (CaB6) olduğu gibi 1/3 fraksiyonel oksidasyon durumlarına sahiptir.
Yapısal açıdan borun en belirgin kimyasal bileşikleri hidritlerdir. Bu seriye dahil olan küme bileşikleri dodecaborate (B12H2-12), dekaboran (B10H14) ve C2B10H12 gibi karboranlardır. Karakteristik olarak bu tür bileşikler, koordinasyon sayıları dörtten büyük olan bor içerir.[27]
İzotoplar[değiştir | kaynağı değiştir]
Borun doğal olarak oluşan ve kararlı iki izotopu vardır, 11B (%80.1) ve 10B (%19.9). Kütle farkı, -16 ile +59 arasında değişen 11B ile 10B arasındaki kesirli bir fark olarak tanımlanan ve geleneksel olarak binde bir olarak ifade edilen geniş bir δ11B değerleri aralığıyla sonuçlanır. Borun bilinen 13 izotopu vardır; en kısa ömürlü izotop 7B'dir ve proton emisyonu ve alfa bozunması yoluyla 3,5 × 10 −22 s'lik bir yarı ömürle bozunur. Borun izotopik fraksiyonlanması, bor türleri B(OH)3 ve [B(OH)4]-' nin değişim reaksiyonları tarafından kontrol edilir. Bor izotopları ayrıca hidrotermal sistemlerde H2O faz değişimlerinde mineral kristalleşmesi sırasında ve kayanın hidrotermal alterasyonu sırasında fraksiyonlara ayrılır. İkinci etki, [10B(OH)4]− iyonunun killer üzerinde tercihli olarak çıkarılmasıyla sonuçlanır. 11B(OH)3 açısından zenginleştirilmiş çözeltilerle sonuçlanır ve bu nedenle hem okyanus kabuğuna hem de kıtasal kabuğa göre deniz suyundaki büyük 11B zenginleşmesinden sorumlu olabilir; bu fark, izotopik bir imza görevi görebilir.[37]
Egzotik 17B bir nükleer hale sergiliyor, yani yarıçapı sıvı damla modeli tarafından tahmin edilenden önemli ölçüde daha büyük.[38]
10B izotopu, termal nötronları yakalamak için kullanışlıdır (bkz. nötron kesiti#Tipik kesitler). Nükleer endüstri, doğal bor'u neredeyse saf 10B'ye kadar zenginleştirir. Daha az değerli yan ürün, tükenmiş bor, neredeyse saf 11B'dir.
Ticari izotop zenginleştirme[değiştir | kaynağı değiştir]
Bor-10, yüksek nötron kesiti nedeniyle sıklıkla nükleer reaktörlerde nötron tutucu bir madde olarak fisyonu kontrol etmek için kullanılır.[39] Çeşitli endüstriyel ölçekli zenginleştirme süreçleri geliştirilmiştir; bununla birlikte, yalnızca boron triflorürün (DME-BF3) dimetil eter eklentisinin fraksiyonlara ayrılmış vakumla damıtılması ve boratların kolon kromatografisi kullanılmaktadır.[40][41]
Zenginleştirilmiş bor (bor-10)[değiştir | kaynağı değiştir]

Zenginleştirilmiş bor (veya 10B) hem radyasyon kalkanı, hem de kanserin nötron yakalama tedavisinde kullanılan birincil nükliddir. İkincisinde ("bor nötron yakalama tedavisi" veya BNCT), 10B içeren bir bileşik, habis bir tümör ve yakınındaki dokular tarafından seçici olarak alınan bir farmasötik maddeye dahil edilir. Hasta daha sonra nispeten düşük bir nötron radyasyon dozunda bir düşük enerjili nötron ışını ile tedavi edilir. Ancak nötronlar, bor + nötron nükleer reaksiyonunun ürünleri olan enerjik ve kısa menzilli ikincil alfa parçacığı ve lityum-7 ağır iyon radyasyonunu tetikler ve bu iyon radyasyonu ayrıca, özellikle tümör hücrelerinin içinden tümörü bombalar.[42][43][44][45]
Nükleer reaktörlerde 10B reaktivite kontrolü ve acil kapatma sistemlerinde kullanılmaktadır. Borosilikat çubukları veya borik asit olarak işlev görebilir. Basınçlı su reaktörlerinde, tesis yakıt ikmali için kapatıldığında reaktör soğutucusuna 10B borik asit eklenir. Daha sonra, bölünebilir malzeme tükendikçe ve yakıt daha az reaktif hale geldikçe, aylar boyunca yavaşça filtrelenir.[46]
10B yapısal malzeme (bor fiber veya BN nanotüp malzemesi olarak) olarak gelecekteki mürettebatlı gezegenler arası uzay aracının radyasyon kalkanında özel bir rol oynayabilir. Çoğunlukla yüksek enerjili protonlar olan kozmik ışınlarla uğraşmanın zorluklarından biri, kozmik ışınlar ve uzay aracı malzemelerinin etkileşiminden kaynaklanan bazı ikincil radyasyonun yüksek enerjili parçalanma nötronları olmasıdır. Bu tür nötronlar, polietilen gibi yüksek oranda hafif elementler içeren malzemelerle yumuşatılabilir, ancak yumuşatılmış nötronlar, kalkanda aktif olarak soğurulmadıkça radyasyon tehlikesi olmaya devam eder. Termal nötronları emen hafif elementler arasında 6Li ve 10B, hem mekanik takviye hem de radyasyondan korunma görevi gören potansiyel uzay aracı yapısal malzemeleri olarak görünmektedir.[47]
Tükenmiş bor (bor-11)[değiştir | kaynağı değiştir]
Radyasyonla sertleştirilmiş yarı iletkenler[değiştir | kaynağı değiştir]
Kozmik radyasyon, uzay aracı yapılarına çarparsa ikincil nötronlar üretecektir. Bu nötronlar, eğer uzay aracının yarı iletkenlerinde bulunuyorsa, bir gama ışını, bir alfa parçacığı ve bir lityum iyonu üretiyorsa, 10B'de yakalanacaktır. Ortaya çıkan bu bozunma ürünleri daha sonra yakındaki yarı iletken "çip" yapılarını ışınlayarak veri kaybına (bit çevirme veya tek olay bozulması) neden olabilir. Radyasyonla sertleştirilmiş yarı iletken tasarımlarında, bir karşı önlem, 11B açısından büyük ölçüde zenginleştirilmiş ve neredeyse hiç 10B içermeyen tükenmiş bor kullanmaktır. Bu yararlıdır çünkü 11B büyük ölçüde radyasyon hasarına karşı bağışıktır. Tükenmiş bor, nükleer endüstrinin bir yan ürünüdür (yukarıya bakın).[46]
Nükleer yakıt olarak[değiştir | kaynağı değiştir]
11B anötronik füzyon için bir yakıt adayıdır. Enerjisi yaklaşık 500 k eV olan bir proton çarptığında üç alfa parçacığı ve 8.7 MeV enerji üretir. Hidrojen ve helyum içeren diğer füzyon reaksiyonlarının çoğu, reaktör yapılarını zayıflatan ve uzun vadeli radyoaktiviteye neden olan ve dolayısıyla işletme personelini tehlikeye atan nüfuz edici nötron radyasyonu üretirken 11B füzyonunda oluşan alfa parçacıkları doğrudan elektrik enerjisine dönüştürülebilir ve reaktör kapatılır-kapatılmaz tüm radyasyon durur.[48]
Prof. Dr. Doğan Aydal Veryansın Tv. adlı bir youtube programında teorik olarak Bor-11 izotobuna laser ve plazma etkisiyle bir H+ eklenmesiyle izotobun kararasız hale geleceğini ve parçalanarak 3 adet helyuma dönüşeceğini, sonuçta büyük bir enerji üretecek bu reaksiyonun küçük miktarlarda deneysel olarak başarıldığını ifade ediyor.[49]
NMR spektroskopisi[değiştir | kaynağı değiştir]
Hem 10B hem de 11B nükleer dönüşe sahiptir. 10B'nin nükleer spini 3'tür ve 11B'ninki ise 32 dir. Bu izotoplar, bu nedenle, nükleer manyetik rezonans spektroskopisinde kullanıma uygundur; ve boron-11 çekirdeklerini saptamak için özel olarak uyarlanmış spektrometreler ticari olarak mevcuttur. 10B ve 11B çekirdekleri de bağlı çekirdeklerin rezonanslarında bölünmeye neden olur.[50]
Meydana gelişi[değiştir | kaynağı değiştir]


Big Bang ve yıldızlarda eser oluşumu nedeniyle Bor evren ve güneş sisteminde nadirdir. Kozmik ışın parçalanması nükleosentezinde küçük miktarlarda oluşur ve kozmik toz ve meteoroid materyallerde bulunabilir.
Dünyanın yüksek oksijen ortamında, bor element olarak değil borata oksitlenmiş olarak bulunur Ay regolitinde son derece küçük elementel bor izleri tespit edilmiştir.[51]
Bor, yer kabuğunda kabuk kütlesinin sadece %0.001'ini temsil eden oldukça nadir bir element olmasına rağmen suyun çözücü etkisiyle yüksek oranda konsantre olabilir. Boraks ve borik asit olarak volkanik kaynak sularında doğal bileşik halinde bulunabilir. Yüze yakın borat minerali bilinmektedir.
Bilim adamları, 5 Eylül 2017'de Curiositynin Mars gezegeninde yaşam için temel bir bileşen olan boru tespit ettiğini bildirdi. Böyle bir bulgu, antik Mars'ta suyun mevcut olabileceğine dair önceki keşiflerle birlikte, Gale Krateri'nin Mars'taki olası erken yaşanabilirliğini daha da destekler.[52][53]
Üretim[değiştir | kaynağı değiştir]
Ekonomik açıdan önemli kaynaklar kolemanit, rasorit (kernit), üleksit ve tinkal mineralleridir. Bunlar birlikte, çıkarılan bor içeren cevherin %90'ını oluşturur. Bilinen en büyük küresel boraks yatakları, çoğu hala kullanılmamış olup, Eskişehir, Kütahya ve Balıkesir illeri de dahil olmak üzere Orta ve Batı Türkiye'de bulunmaktadır.[54][55][56] Küresel kanıtlanmış bor madeni rezervleri, yıllık yaklaşık dört milyon ton üretime karşılık bir milyar metrik tonu aşıyor.
Türkiye ve Amerika Birleşik Devletleri en büyük bor üreticileridir. Türkiye, küresel talebin yaklaşık yarısını bir Türk devlet madencilik ve kimya şirketi olan Eti Maden İşletmeleri aracılığıyla üretiyor. Dünyadaki bilinen yatakların %72'sine sahip olan Türkiye'de borat madenciliği konusunda devlet tekeline sahiptir.[57] 2012 yılında, ana rakibi Rio Tinto Group'un önünde, küresel borat mineralleri üretiminde %47'lik bir paya sahip olmuştur.[58]
Küresel bor üretiminin neredeyse dörtte biri (%23)
35°2′34.447″K 117°40′45.412″B / 35.04290194°K 117.67928111°B California yakınları ndaki tek Rio Tinto Boraks Madeninden (ABD Boraks Bor Madeni olarak da bilinir) gelmektedir.[59][60]
Piyasa[değiştir | kaynağı değiştir]
Kristal borun ortalama maliyeti 5 ABD Doları /g'dır.[61] Elemental bor, bir tungsten çekirdeği üzerinde kimyasal buhar biriktirme yöntemiyle bor liflerinin yapımında kullanılır. Bor lifleri, yüksek mukavemetli hafif kompozit eldesinde kullanılır. Bu kullanım, toplam bor kullanımının çok küçük bir kısmıdır. Bor, yarı iletkenlere bor bileşikleri olarak iyon implantasyonu ile verilir.
2012'de Tahmini küresel bor tüketimi yaklaşık 4 milyon ton B2O3 idi. Boraks ve kernit gibi bileşikler olarak maliyeti 2019'da 377 ABD Doları / ton idi.[62] Bor madenciliği ve rafinaj kapasitelerinin önümüzdeki on yıl boyunca beklenen büyüme seviyelerini karşılamak için yeterli olduğu düşünülmektedir.
Borun tüketimi Kolemanit gibi cevherlerin arsenik içeriğiyle ilgili endişelerin ardından değişmiş, tüketiciler, daha düşük kirletici içeriğine sahip rafine boratlar ve borik asit kullanımına yönelmişlerdir.
Borik asidin talep artışı, bazı üreticilerin ek yatırım yapmasına neden olmuştur. Türkiye'nin devlete ait Maden İşletmeleri, 2003 yılında Emet'te yıllık 100.000 ton üretim kapasiteli yeni bir borik asit tesisi açtı. Rio Tinto Group, bor tesisinin kapasitesini 2003 yılında yıllık 260.000 tondan Mayıs 2005'e kadar yıllık 310.000 tona çıkardı ve bunu 2006 yılında yıllık 366.000 tona çıkarmayı planlıyor.Çinli bor üreticileri, hızla artan yüksek kaliteli borat talebini karşılayamadı. Bu, sodyum tetraborat (boraks) ithalatının 2000 ile 2005 yılları arasında yüz kat ve borik asit ithalatının aynı dönemde yılda% 28 artmasına neden olmuştur.[1]
Küresel talep cam elyafı ve borosilikat cam eşya üretimindeki yüksek büyüme oranlarından kaynaklanmıştır. Asya'da donatı sınıfı bor içeren cam elyafı üretimindeki artış, Avrupa ve ABD'de bor içermeyen donatı sınıfı cam elyaf gelişimini dengelemiştir. Enerji fiyatlarındaki son artışlar, yalıtım sınıfı fiberglasa bağlı bor tüketiminde artışa neden olabilir. Roskill Consulting Group, dünya bor talebinin yılda% 3,4 artarak 2010 yılına kadar 21 milyon tona ulaşacağını tahmin ediyor. Talepteki en yüksek büyümenin, talebin yılda ortalama % 5,7 artabileceği Asya'da olması bekleniyor.[63][64]
Uygulamalar[değiştir | kaynağı değiştir]
Yerden çıkarın cevherin tamamına yakını borik asit ve sodyum tetraborat pentahidrat olarak arıtılmaya gider. Amerika Birleşik Devletleri'nde borun % 70'i cam ve seramik üretiminde kullanılmaktadır.[65][66]
Bor bileşiklerinin başlıca küresel endüstriyel ölçekli kullanımı, yüzde % 46 ile özellikle Asya'da bor içeren yalıtım ve yapısal fiberglaslar için cam elyaf üretimindedir. Bor, cama boraks pentahidrat veya bor oksit olarak cam elyaflarının mukavemet veya akışkanlık özelliklerini etkilemek için eklenir. Küresel bor üretiminin % 10'u, yüksek mukavemetli cam eşyalarda kullanılan borosilikat cam içindir. Küresel borun yaklaşık % 15'i, aşağıda tartışılan süper sert malzemeler de dahil olmak üzere bor seramiklerinde kullanılmaktadır. Tarım, küresel bor üretiminin % 11'ini, ağartıcı ve deterjanlar ise yaklaşık % 6'sını tüketmektedir.
Elemental bor lifi[değiştir | kaynağı değiştir]
Bor lifleri havacılık, golf sopaları ve oltalar gibi sınırlı alanlarda kullanılan gelişmiş, yüksek mukavemetli, hafif malzemelerdir.[67][68] Lifler, bir tungsten filamenti üzerinde borun kimyasal buhar birikimi ile üretilebilir.[3]
Bor lifleri ve milimetre altı boyutunda kristal bor yayları, lazer destekli kimyasal buhar biriktirme ile üretilir. Odaklanmış lazer ışınının çevrilmesi, karmaşık sarmal yapıların bile üretilmesini sağlar. Bu tür yapılar iyi mekanik özellikler gösterir (elastik modül 450 GPa, kırılma gerilimi % 3.7, kırılma basıncı 17 GPa) ve seramik takviyesi olarak veya mikromekanik sistemlerde uygulanabilir.[1]
Borlu fiberglas[değiştir | kaynağı değiştir]
Fiberglas, genellikle bir paspas içine dokunmuş, cam elyaflarla güçlendirilmiş plastikten yapılmış, elyaf takviyeli bir polimerdir. Fiberglas kullanıma bağlı olarak çeşitli cam türlerinden yapılır. Bu camların tümü, değişen miktarlarda kalsiyum, magnezyum ve bazen bor oksitleri içeren silika veya silikat içerir. Bor, borosilikat, boraks veya bor oksit olarak bulunur ve camın mukavemetini arttırmak veya saf haliyle kolayca işlenemeyecek kadar yüksek olan silikanın erime sıcaklığını düşürmek için bir akıtma maddesi olarak eklenir.
Fiberglasta kullanılan yüksek oranda borlu camlar E-cam olarak adlandırılmıştır. E-cam, esas olarak cam takviyeli plastikler için kullanılan, ağırlıkça % 1'den az alkali oksitli alümino-borosilikat camdır. Diğer yaygın yüksek borlu camlar arasında, cam kesikli lifler ve yalıtım için kullanılan yüksek bor oksit içeriğine sahip bir alkali-kireç camı olan C-cam ve düşük dielektrik sabiti ile adlandırılan bir borosilikat cam olan D-cam bulunur.
Küresel ölçekte kullanılan fiberglasın hepsi olmasa da çoğu bor içerir. Fiberglasın inşaat ve yalıtımda her yerde kullanılması nedeniyle, bor içeren fiberglaslar küresel üretimin yarısını tüketir ve en büyük bor pazarıdır.
Borosilikat cam[değiştir | kaynağı değiştir]

Tipik olarak % 12-15 B2O3,% 80 SiO 2 ve % 2 Al2O3 olan borosilikat cam, düşük bir termal genleşme katsayısına sahiptir ve bu da termal şoka karşı iyi bir direnç sağlar. Schott AG'nin "Duran" ve Owens-Corning'in markalı Pyrex'i, bu cam için hem laboratuvar cam eşyalarında hem de tüketici tencere ve bakeware ürünlerinde, özellikle bu direnç için kullanılan iki ana markadır.
Bor karbür seramik[değiştir | kaynağı değiştir]

Bazı bor bileşikleri, aşırı sertlikleri ve toklukları ile bilinir. Bor karbür, bir elektrikli fırında B2O3 karbonla ayrıştırılmasıyla elde edilen seramik bir malzemedir:
- 2 B2O3 + 7 C → B4C + 6 CO
Bor karbürün yapısı yaklaşık olarak B4C dir. Bu çok karmaşık yapısından kaynaklanmaktadır.Tekrarlanan polimer artı bor karbürün yarı kristal yapısı, ağırlık başına büyük yapısal mukavemet sağlar. Tank zırhında, kurşun geçirmez yeleklerde ve diğer birçok yapısal uygulamada kullanılır.
Bor karbürün uzun ömürlü radyonüklidler oluşturmadan nötronları emme yeteneği (özellikle ekstra bor-10 ile), malzemeyi nükleer santrallerde ortaya çıkan nötron radyasyonu için bir emici olarak çekici kılar.[69] Bor karbürün nükleer uygulamaları arasında ekranlama, kontrol çubukları ve kapatma peletleri bulunur. Kontrol çubukları içinde, yüzey alanını artırmak için bor karbür genellikle toz haline getirilir.[70]
Yüksek sertlikte ve aşındırıcı bileşikler[değiştir | kaynağı değiştir]
| Elmas | kübik-MÖ 2 N | kübik-MÖ 5 | kübik milyar | B4C | ReB2 | Vickers sertliği (GPa) |
|---|---|---|---|---|---|---|
| 115 | 76 | 71 | 62 | 38 | 22 | Kırılma tokluğu (MPa m 1⁄2) |
| 5.3 | 4.5 | 9.5 | 6.8 | 3.5 |
Aşındırıcı olarak bor karbür ve kübik bor nitrür tozları yaygın olarak kullanılmaktadır. Bor nitrür, karbona izoelektronik bir malzemedir. Karbona benzer şekilde, hem altıgen (yumuşak grafit benzeri h-BN) hem de kübik (sert, elmas benzeri c-BN) formlara sahiptir. h-BN, yüksek sıcaklık bileşeni ve yağlayıcı olarak kullanılır. borazon ticari adıyla da bilinen c-BN,[73] üstün bir aşındırıcıdır. Sertliği elmastan sadece biraz daha küçüktür, ancak kimyasal stabilitesi elmastan daha üstündür. Heterodiamond (BCN olarak da adlandırılır) başka bir elmas benzeri bor bileşiğidir.
Metalurji[değiştir | kaynağı değiştir]
Sertliği arttırmak için bor çeliklerine milyonda birkaç parça düzeyinde bor eklenir. Borun nötron emme kabiliyeti nedeniyle nükleer endüstride kullanılan çeliklere daha yüksek yüzdeler eklenir.
Bor, borlama yoluyla çelik ve alaşımların yüzey sertliğini de artırabilir. Ek olarak, aletleri kimyasal buhar biriktirme veya fiziksel buhar biriktirme yoluyla kaplamak için metal borürler kullanılır. İyon implantasyonu veya iyon ışını birikimi yoluyla bor iyonlarının metallere ve alaşımlara implantasyonu, yüzey direncinde ve mikro sertlikte muhteşem bir artışa neden olur. Lazer alaşımlama da aynı amaç için başarıyla kullanılmıştır. Bu borürler, elmas kaplı aletlere bir alternatiftir ve (işlenmiş) yüzeyleri, dökme borürünkilere benzer özelliklere sahiptir.[74]
Örneğin, renyum diborür ortam basınçlarında üretilebilir, ancak oldukça pahalıdır. ReB2'nin sertliği, altıgen katmanlı yapısı nedeniyle önemli ölçüde anizotropi sergiler. Değeri tungsten karbür, silisyum karbür, titanyum diborür veya zirkonyum diborür ile karşılaştırılabilir.[1] Benzer şekilde, AlMgB14+ TıB2 kompozitleri yüksek sertliğe ve aşınma direncine sahiptir ve dökme halde veya yüksek sıcaklıklara ve aşınma yüklerine maruz kalan bileşenler için kaplama olarak kullanılır.
Deterjan formülasyonları ve ağartma maddeleri[değiştir | kaynağı değiştir]
Boraks, " 20 Mule Team Borax " çamaşır güçlendirici ve " Boraxo " toz el sabunu dahil olmak üzere çeşitli ev tipi çamaşır ve temizlik ürünlerinde kullanılır. Bazı diş beyazlatma formüllerinde de bulunur.[66]
Sodyum perborat birçok deterjanda, çamaşır deterjanlarında, temizlik ürünlerinde ve çamaşır ağartıcılarında aktif oksijen kaynağı olarak görev yapar. Bununla birlikte, "Borateem" çamaşır suyu, ismine rağmen artık herhangi bir bor bileşiği içermez, bunun yerine ağartma maddesi olarak sodyum perkarbonat kullanılır.[75]
Böcek öldürücüler[değiştir | kaynağı değiştir]
Borik asit, özellikle karınca, pire ve hamamböceklerine karşı böcek ilacı olarak kullanılır.[76]
Yarı iletkenler[değiştir | kaynağı değiştir]
Bor, silikon, germanyum ve silisyum karbür gibi yarı iletkenler için faydalı bir katkı maddesidir. Konak atomdan bir eksik değerlik elektronuna sahip olarak, p tipi iletkenlikle sonuçlanan bir delik açar. Borun yarı iletkenlere sokulmasının geleneksel yöntemi, yüksek sıcaklıklarda atomik difüzyonudur. Bu işlem katı (B2O3), sıvı (BBr3) veya gaz (B2H6 veya BF3) halindeki bor kaynaklarını kullanır. (1970'lerden sonra, çoğunlukla bor kaynağı olarak BF 3'e dayanan iyon implantasyonu ile değiştirildi.[1]) Bor triklorür, yarı iletken endüstrisinde de önemli bir kimyasaldır, ancak doping için değil, metallerin ve oksitlerinin plazma aşındırmasında,[77][78] ayrıca bir bor kaynağı olarak buhar biriktirme reaktörlerine enjekte edilir.Örnekler, bor içeren sert karbon filmlerin, silikon nitrür-bor nitrür filmlerin plazma birikimi ve[79] filmin borla katkılanmasıdır.[4]
Mıknatıslar[değiştir | kaynağı değiştir]
Bor, en güçlü kalıcı mıknatıs türleri arasında yer alan neodim mıknatısların (Nd2Fe14B) bileşenlerindendir. Bu mıknatıslar, kompakt ve nispeten küçük motor ve aktüatörlerde manyetik rezonans görüntüleme (MRI) sistemleri gibi çeşitli elektromekanik ve elektronik cihazlarda bulunur. Örnek olarak, bilgisayar sabit diskleri (sabit disk sürücüleri), CD (kompakt disk) ve DVD (dijital çok yönlü disk) oynatıcılar, kompakt bir pakette yoğun dönüş gücü sağlamak için neodim mıknatıslı motorlara güvenir. Cep telefonlarında 'Neo' mıknatıslar, küçük hoparlörlerin yüksek ses gücü sağlamasına olanak sağlar.[80]
Nükleer reaktörlerde koruyucu ve nötron soğurucu[değiştir | kaynağı değiştir]
Bor koruyucu, nötron yakalama için yüksek kesitinden yararlanarak nükleer reaktörler için bir kontrol olarak kullanılır.[81]
Basınçlı su reaktörlerinde, yakıtın değişken reaktivitesini telafi etmek için bir nötron zehri olarak soğutma suyundaki değişken bir boronik asit konsantrasyonu kullanılır. Yeni çubuklar yerleştirildiğinde, boronik asit konsantrasyonu maksimumdur ve kullanım ömrü boyunca azalır.[82]
Diğer tıbbi olmayan kullanımlar[değiştir | kaynağı değiştir]
- Kendine özgü yeşil alevi nedeniyle, piroteknik işaret fişeklerinde amorf bor kullanılır.[83]
- 1950'li yıllarda jet yakıtı için enerji artırıcı "Zip yakıtı" katkı maddesi olarak boranların kullanımına ilişkin çeşitli çalışmalar yapılmıştır.
- Nişasta ve kazein bazlı yapıştırıcılar sodyum tetraborat dekahidrat (Na2B4 O7 ·10 H2O) içerir.
- Bazı korozyon önleyici sistemler boraks içerir.[84]
- Sodyum boratlar, gümüş ve altını lehimlemek için eritken olarak ve demirli metalleri kaynaklamak için amonyum klorür ile birlikte kullanılır.[85] Ayrıca plastik ve kauçuk ürünler için yangın geciktirici katkı maddeleridir.[86]
- Borik asit (ortoborik asit olarak da bilinir) H3BO3 tekstil cam elyafı ve düz panel ekranların[66][87] üretiminde ve birçok PVAc ve PVOH bazlı yapıştırıcıda kullanılır.
- Trietilboran, Lockheed SR-71 Blackbird'e güç sağlayan Pratt & Whitney J58 turbojet / ramjet motorlarının JP-7 yakıtını ateşleyen bir maddedir.[88] Ayrıca 1967'den 1973'e kadar NASA'nın Apollo ve Skylab programları tarafından kullanılan Saturn V Roketindeki F-1 Motorlarını ateşlemek için kullanıldı. Bugün SpaceX, bunu Falcon 9 roketindeki motorları ateşlemek için kullanıyor. Trietilboran, piroforik özellikleri nedeniyle, özellikle çok yüksek bir sıcaklıkta yanması nedeniyle bunun için uygundur.[89] Trietilboran, düşük sıcaklıklarda bile etkili olduğu radikal reaksiyonlarda endüstriyel bir başlatıcıdır.
- Boratlar, çevreye zarar vermeyen ahşap koruyucular olarak kullanılır.[90]
Farmasötik ve biyolojik uygulamalar[değiştir | kaynağı değiştir]
Borik asit antiseptik, antifungal ve antiviral özelliklere sahiptir ve bu nedenlerle yüzme havuzlarında su arıtıcı olarak uygulanır.[91] Göz antiseptikleri olarak hafif borik asit çözeltileri kullanılmıştır.
Bortezomib (Velcade ve Cytomib olarak pazarlanmaktadır). Bor, miyelom ve bir lenfoma formunun tedavisi için proteazom inhibitörü olarak adlandırılan yeni bir ilaç sınıfı olan organik farmasötik bortezomib'de aktif bir element olarak görünmektedir (şu anda diğer lenfoma tiplerine karşı deneysel denemelerdedir). Bortezomib içindeki bor atomu, 26S proteazomunun[92] katalitik bölgesine yüksek afinite ve özgüllükle bağlanır.
- Bor nötron yakalama tedavisinde (BNCT) kullanılmak üzere boron-10 kullanan bir dizi potansiyel borlanmış farmasötik hazırlanmıştır.[93]
- Bazı bor bileşikleri, artrit tedavisinde umut vadediyor, ancak henüz hiçbiri bu amaç için genel olarak onaylanmadı.[94]
Tavaborole (Kerydin olarak pazarlanmaktadır), ayak tırnağı mantarını tedavi etmek için kullanılan bir Aminoasil tRNA sentetaz inhibitörüdür. Temmuz 2014'te FDA onayı aldı.[95]
Dioksaborolan kimyası, sırasıyla kanser [96] ve kanamaların[97] pozitron emisyon tomografisi (PET) ile görüntülenmesine izin veren antikorların veya kırmızı kan hücrelerinin radyoaktif florür (<sup id="mwBHY">18F</sup> ) ile işaretlenmesini sağlar. İnsan Kaynaklı, Genetik, Pozitron yayan ve Floresan (HD-GPF) raportör sistemi, bir insan proteini, PSMA ve immünojenik olmayan ve pozitron yayan küçük molekül (bor bağlı 18F) kullanır. ve genomu modifiye edilmiş hücrelerin, örneğin kanser, CRISPR/Cas9 veya CAR T -hücrelerinin tüm bir farede dual modalite PET ve floresan görüntülemesi için floresans.[98] PSMA'yı hedefleyen çift modaliteli küçük molekül, insanlarda test edildi ve birincil ve metastatik prostat kanserinin yerini, kanserin flüoresan kılavuzlu çıkarılmasını buldu ve doku marjlarında tek kanser hücrelerini tespit etti.[99]
Araştırma bölgeleri[değiştir | kaynağı değiştir]
Magnezyum diborür, geçiş sıcaklığı 39 K olan önemli bir süper iletken malzemedir. MgB 2 telleri, tüp içinde toz işlemiyle üretilir ve süper iletken mıknatıslara uygulanır.[100][101]
Amorf bor, nikel-krom sert-lehim alaşımlarında erime noktası düşürücü olarak kullanılır.[102]
Altıgen bor nitrür, grafen cihazlarında elektron hareketliliğini arttırmak için kullanılmış olan atomik olarak ince tabakalar oluşturur.[103][104] Aynı zamanda, istenen özellikler listesi arasında yüksek mukavemet, yüksek kimyasal kararlılık ve yüksek termal iletkenliğe sahip nanotübüler yapılar (BNNT'ler) oluşturur.[105]
Biyolojik rol[değiştir | kaynağı değiştir]
Bor, öncelikle hücre duvarlarının bütünlüğünü korumak için gerekli olan temel bir bitki besin maddesidir . Ancak, 1.0'ppm dan büyük olan yüksek toprak konsantrasyonları, yapraklarda marjinal ve uç nekrozunun yanı sıra zayıf genel büyüme performansına yol açar. 0,8 ppm kadar düşük seviyeler, topraktaki bora özellikle duyarlı olan bitkilerde aynı semptomları üretir. Neredeyse tüm bitkiler, hatta toprak boruna bir şekilde toleranslı olanlar bile, toprak bor içeriği 1.8'ppmden fazla olduğunda en azından bazı boron toksisitesi belirtileri gösterecektir. Bu içerik 2.0'ppm'i geçtiğinde, birkaç bitki iyi performans gösterecek ve bazıları hayatta kalamayabilir.[106][107][108]
Borun, insanlar da dahil olmak üzere hayvanlarda birkaç temel rol oynadığı düşünülmektedir, ancak kesin fizyolojik rolü tam olarak anlaşılamamıştır.[109][110] 1987'de yayınlanan küçük bir insan denemesi, menopoz sonrası kadınlarda önce bor eksikliğini giderdiğini ve ardından 3 mg/gün ile tamamlandığını bildirdi. Bor takviyesi üriner kalsiyum atılımını önemli ölçüde azalttı ve 17 beta-estradiol ve testosteronun serum konsantrasyonlarını yükseltti.[111]
ABD Tıp Enstitüsü, borun insanlar için temel bir besin maddesi olduğunu doğrulamamıştır, bu nedenle ne bir Tavsiye Edilen Diyet Ödeneği (RDA) ne de Yeterli Alım belirlenmemiştir. Yetişkin diyet alımının 0,9 ila 1,4 mg/gün olduğu tahmin edilmektedir. Yaklaşık %90'ı emilir. Emilenler çoğunlukla idrarla atılır. Yetişkinler için Tolere Edilebilir Üst Alım Seviyesi 20'mg/gündür.[112]
2013 yılında bir hipotez, bor ve molibdenin Mars'ta RNA üretimini katalize etmesinin ve yaşamın yaklaşık 3 milyar yıl önce bir göktaşı aracılığıyla Dünya'ya taşınmasının mümkün olduğunu ileri sürdü.[113]
Bilinen birkaç boron içeren doğal antibiyotik vardır.[114] Streptomiçeslerden ilk izole edilen boromisin idi.[115][116]
Korneal distrofinin nadir bir formu olan konjenital endotelyal distrofi tip 2, boronun hücre içi konsantrasyonunu düzenlediği bildirilen bir taşıyıcıyı kodlayan SLC4A11 genindeki mutasyonlarla bağlantılıdır.[117]
Analitik ölçüm[değiştir | kaynağı değiştir]
Gıda veya malzemelerdeki bor içeriğinin belirlenmesi için kolorimetrik kurkumin yöntemi kullanılır. Bor, borik asit veya boratlara dönüştürülür ve kurkumin ile asidik çözeltide reaksiyona girerek kırmızı renkli bir borşelat kompleksi olan rososiyanin oluşur.[118]
Sağlık sorunları ve toksisite[değiştir | kaynağı değiştir]
Elemental bor, bor oksit, borik asit, boratlar ve birçok organoboron bileşiği, insanlar ve hayvanlar için nispeten toksik değildir (toksisitesi sofra tuzuna benzer). Hayvanlar için LD50 (%50 mortalitenin olduğu doz) yaklaşık vücut ağırlığının kg'ı başına 6g. LD 50'si 2'nin üzerinde olan maddeler toksik olmayan olarak kabul edilir. 4 g/gün borik asit olaysız rapor edildi, ancak bundan fazla birkaç dozdan fazla toksik olarak kabul edildi. 0,5'dan fazla alımlar (50 gün boyunca) küçük sindirim sorunlarına ve toksisiteyi düşündüren diğer sorunlara neden olur.[119] Borun diyete eklenmesi kemik büyümesi, yara iyileşmesi ve antioksidan aktivite için yararlı olabilir[120] ve diyette yetersiz bor, bor eksikliğine neden olabilir.
Nötron yakalama tedavisi için 20'g.lık tek doz borik asit aşırı toksisite olmaksızın kullanılmıştır.
Borik asit, böcekler için memelilerden daha zehirlidir ve rutin olarak bir böcek ilacı olarak kullanılır.[76]
Boranlar (bor hidrojen) ve benzeri gaz bileşikleri oldukça zehirlidir. Her zamanki gibi, bor özünde zehirli bir element değildir, ancak bu bileşiklerin toksisitesi yapıya bağlıdır (olgunun başka bir örneği için bkz . fosfin ).[4][5] Boranlar ayrıca oldukça yanıcı ve diğer bileşiklerin bazı kombinasyonları oldukça patlayıcıdır. Sodyum borohidrit, indirgeyici doğası ve asitle temas ettiğinde hidrojenin serbest kalması nedeniyle yangın tehlikesi arz eder. Bor halojenürler aşındırıcıdır.[121]

Bor, bitki büyümesi için gereklidir, ancak bor fazlalığı bitkiler için toksiktir ve özellikle asidik toprakta görülür.[122][123] En yaşlı yaprakların uçtan içe doğru sararması ve arpa yapraklarında siyah noktalar şeklinde kendini gösterir ancak diğer bitkilerde magnezyum noksanlığı gibi diğer streslerle karıştırılabilir.[124]
Ayrıca bakınız[değiştir | kaynağı değiştir]
Kaynakça[değiştir | kaynağı değiştir]
- ^ "Q & A: Where does the element Boron come from?". physics.illinois.edu. 29 Mayıs 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Aralık 2011.
- ^ "Boron". Britannica encyclopedia. 4 Ağustos 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Ağustos 2020.
- ^ Methods Used in Preparing Boron (İngilizce). U.S. Department of the Interior, Bureau of Mines. 1964. s. 14. 8 Mart 2024 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Nisan 2023.
- ^ a b Garrett, Donald E. (1998). Borates: handbook of deposits, processing, properties, and use. Academic Press. ss. 102; 385-386. ISBN 978-0-12-276060-0.
- ^ a b Calvert, J. B. "Boron". University of Denver. 24 Eylül 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2009.
- ^ Hildebrand, G. H. (1982) "Borax Pioneer: Francis Marion Smith."
- ^ Elvira, Mary (1933). "XII. Other Elements Isolated with the Aid of Potassium and Sodium: Beryllium, Boron, Silicon and Aluminum". The Discovery of the Elements. Easton, PA: Journal of Chemical Education. s. 156. ISBN 978-0-7661-3872-8. 20 Eylül 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Ocak 2016.
- ^ Berzelius produced boron by reducing a borofluoride salt; specifically, by heating potassium borofluoride with potassium metal.
- ^ Weintraub, Ezekiel (1910). "Preparation and properties of pure boron". Transactions of the American Electrochemical Society. 16: 165-184. 9 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Ocak 2016.
- ^ a b Laubengayer (1943). "Boron. I. Preparation and Properties of Pure Crystalline Boron". Journal of the American Chemical Society. 65 (10): 1924-1931. doi:10.1021/ja01250a036.
- ^ Borchert, W. (1970). "Crystal Growth of Beta–Rhombohedrical Boron". Zeitschrift für Angewandte Physik. 29: 277.
- ^ Berger, L. I. (1996). Semiconductor materials. CRC Press. ss. 37-43. ISBN 978-0-8493-8912-2.
- ^ Delaplane, R.G. (1988). "A neutron diffraction study of amorphous boron". Journal of Non-Crystalline Solids. 104 (2–3): 249-252. doi:10.1016/0022-3093(88)90395-X.
- ^ R.G. Delaplane (1988). "A neutron diffraction study of amorphous boron using a pulsed source". Journal of Non-Crystalline Solids. 106 (1–3): 66-69. doi:10.1016/0022-3093(88)90229-3.
- ^ a b c Oganov, A.R. (2009). "Ionic high-pressure form of elemental boron" (PDF). Nature. 457 (7231): 863-867. arXiv:0911.3192 $2. doi:10.1038/nature07736. PMID 19182772. 28 Temmuz 2018 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 9 Mayıs 2009.
- ^ van Setten M.J. (2007). "Thermodynamic stability of boron: The role of defects and zero point motion" (PDF). J. Am. Chem. Soc. 129 (9): 2458-2465. doi:10.1021/ja0631246. PMID 17295480. 15 Nisan 2021 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 14 Temmuz 2019.
- ^ Widom M. (2008). "Symmetry-broken crystal structure of elemental boron at low temperature". Phys. Rev. B. 77 (6): 064113. arXiv:0712.0530 $2. doi:10.1103/PhysRevB.77.064113.
- ^ Eremets, M. I. (2001). "Superconductivity in Boron". Science. 293 (5528): 272-4. doi:10.1126/science.1062286. PMID 11452118.
- ^ Wentorf, R. H. (Ocak 1965). "Boron: Another Form". Science (İngilizce). 147 (3653): 49-50. doi:10.1126/science.147.3653.49. ISSN 0036-8075. 9 Şubat 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Mayıs 2023.
- ^ Hoard, J. L. (1970). "The structure analysis of β-rhombohedral boron". J. Solid State Chem. 1 (2): 268-277. doi:10.1016/0022-4596(70)90022-8.
- ^ Will, G. (2001). "Electron Deformation Density in Rhombohedral a-Boron". Zeitschrift für Anorganische und Allgemeine Chemie. 627 (9): 2100. doi:10.1002/1521-3749(200109)627:9<2100::AID-ZAAC2100>3.0.CO;2-G.
- ^ Talley, C. P.; La Placa, S.; Post, B. (10 Mart 1960). "A new polymorph of boron". Acta Crystallographica (İngilizce). 13 (3): 271-272. doi:10.1107/S0365110X60000613. ISSN 0365-110X. 28 Mayıs 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Mayıs 2023.
- ^ Solozhenko (2008). "On the hardness of a new boron phase, orthorhombic γ-B28". Journal of Superhard Materials. 30 (6): 428-429. arXiv:1101.2959 $2. doi:10.3103/S1063457608060117.
- ^ a b c Zarechnaya (2009). "Superhard Semiconducting Optically Transparent High Pressure Phase of Boron". Phys. Rev. Lett. 102 (18): 185501. doi:10.1103/PhysRevLett.102.185501. PMID 19518885.
- ^ Nelmes, R. J. (1993). "Neutron- and x-ray-diffraction measurements of the bulk modulus of boron". Phys. Rev. B. 47 (13): 7668-7673. doi:10.1103/PhysRevB.47.7668. PMID 10004773.
- ^ Madelung, O. (1983). Landolt-Bornstein, New Series. 17e. Berlin: Springer-Verlag.
- ^ a b c d e f "Bor". Lehrbuch der Anorganischen Chemie. 91–100 (Almanca). Walter de Gruyter. 1985. ss. 814-864. ISBN 978-3-11-007511-3.
- ^ "Violations of the Octet Rule". Introductory Chemistry. 14 Eylül 2014. 17 Mayıs 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Ağustos 2019. Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Mindat.org - Mines, Minerals and More". mindat.org. 22 Nisan 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Ağustos 2019.
- ^ "The significance and impact of Wade's rules". Chem. Commun. 49 (35): 3615-3616. 2013. doi:10.1039/C3CC00069A. PMID 23535980. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Engler, M. (2007). "Hexagonal Boron Nitride (hBN) – Applications from Metallurgy to Cosmetics" (PDF). Cfi/Ber. DKG. 84: D25. ISSN 0173-9913. 13 Haziran 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 8 Ocak 2012.
- ^ Greim, Jochen; Schwetz, Karl A. (2005). "Boron Carbide, Boron Nitride, and Metal Borides". Boron Carbide, Boron Nitride, and Metal Borides, in Ullmann's Encyclopedia of Industrial Chemistry. Wiley-VCH: Weinheim. doi:10.1002/14356007.a04_295.pub2. ISBN 978-3527306732. Yazar eksik
|soyadı2=(yardım) - ^ Jones, Morton E. (1954). "The Preparation and Structure of Magnesium Boride, MgB2". Journal of the American Chemical Society. 76 (5): 1434-1436. doi:10.1021/ja01634a089.
- ^ Canfield (2003). "Magnesium Diboride: Better Late than Never" (PDF). Physics Today. 56 (3): 34-40. doi:10.1063/1.1570770. 26 Şubat 2012 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 8 Ocak 2012.
- ^ "Category "News+Articles" not found - CERN Document Server". cds.cern.ch. 20 Şubat 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 9 Ekim 2020.
- ^ Cardarelli, François (2008). "Titanium Diboride". Materials handbook: A concise desktop reference. ss. 638-639. ISBN 978-1-84628-668-1. 8 Ocak 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Ocak 2016.
- ^ "Boron isotopic analysis of natural fresh and saline waters by negative thermal ionization mass spectrometry". Chemical Geology. 143 (3–4): 255-261. 1997. doi:10.1016/S0009-2541(97)00107-1. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Two-body and three-body halo nuclei". Science China Physics, Mechanics & Astronomy. 46 (4): 441. 2003. doi:10.1360/03yw0027. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Steinbrück, Martin (2004). "Results of the B4C Control Rod Test QUENCH-07" (PDF). Forschungszentrum Karlsruhe in der Helmholtz-Gemeinschaft. 19 Temmuz 2011 tarihinde kaynağından (PDF) arşivlendi.
- ^ "Commissioning of Boron Enrichment Plant". Indira Gandhi Centre for Atomic Research. 8 Aralık 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Eylül 2008.
- ^ Aida (1986). "Chromatographic Enrichment of 10B by Using Weak-Base Anion-Exchange Resin". Separation Science and Technology. 21 (6): 643-654. doi:10.1080/01496398608056140.
- ^ "A Critical Assessment of Boron Neutron Capture Therapy: An Overview". Journal of Neuro-Oncology. 62 (1): 1-5. 2003. doi:10.1023/A:1023262817500. PMID 12749698. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Coderre (1999). "The Radiation Biology of Boron Neutron Capture Therapy". Radiation Research. 151 (1): 1-18. doi:10.2307/3579742. PMID 9973079.
- ^ S; F (1990). "Boron Neutron Capture Therapy of Cancer". Cancer Research. 50 (4): 1061-1070. PMID 2404588. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım); Yazar eksik|soyadı2=(yardım) - ^ "Boron Neutron Capture Therapy – An Overview". Pharmainfo.net. 22 Ağustos 2006. 23 Temmuz 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Kasım 2011.
- ^ a b Nuclear Reactor Analysis. Wiley-Interscience. 1976. s. 245. ISBN 978-0-471-22363-4.
- ^ Yu, J. (2006). "Isotopically Enriched 10BN Nanotubes" (PDF). Advanced Materials. 18 (16): 2157-2160. doi:10.1002/adma.200600231. 3 Ağustos 2008 tarihinde kaynağından (PDF) arşivlendi.
- ^ "A Review of Confinement Requirements for Advanced Fuels". Journal of Fusion Energy. 17 (1): 25-32. 1998. doi:10.1023/A:1022513215080. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Arşivlenmiş kopya". 11 Nisan 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Nisan 2023.
- ^ "Boron NMR". BRUKER Biospin. 2 Mayıs 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2009.
- ^ Mokhov, A.V., Kartashov, P.M., Gornostaeva, T.A., Asadulin, A.A., Bogatikov, O.A., 2013: Complex nanospherulites of zinc oxide and native amorphous boron in the Lunar regolith from Mare Crisium.
- ^ Gasda, Patrick J. ve diğerleri. (5 Eylül 2017). "In situ detection of boron by ChemCam on Mars" (PDF). Geophysical Research Letters. 44 (17): 8739-8748. doi:10.1002/2017GL074480. 28 Ağustos 2019 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 28 Ağustos 2019.
- ^ "Curiosity Has Discovered Something That Raises More Questions About Life on Mars". Gizmodo. 6 Eylül 2017. 4 Ağustos 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Eylül 2017. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Boron and Borates" (PDF). Industrial Minerals and Rocks. 6th: 171-186. 1994. 4 Haziran 2016 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 20 Eylül 2008. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Zbayolu, G. (1992). "Mining and Processing of Borates in Turkey". Mineral Processing and Extractive Metallurgy Review. 9 (1–4): 245-254. doi:10.1080/08827509208952709.
- ^ Kar (2006). "Boron Minerals in Turkey, Their Application Areas and Importance for the Country's Economy". Minerals & Energy – Raw Materials Report. 20 (3–4): 2-10. doi:10.1080/14041040500504293.
- ^ Ayşe Eda Biçer; Işıl Selen Denemeç (September 2013). "Are certain minerals still under state monopoly?" (PDF). Mining Turkey. 3 Mart 2016 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 21 Aralık 2013. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar eksik
|soyadı2=(yardım) - ^ "Turkey as the global leader in boron export and production" (PDF). European Association of Service Providers for Persons with Disabilities Annual Conference 2013. 3 Mart 2016 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 18 Aralık 2013.
- ^ "U.S. Borax Boron Mine". The Center for Land Use Interpretation, Ludb.clui.org. 11 Şubat 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Nisan 2013.
- ^ "Boras". Rio Tinto. 10 Nisan 2012. 18 Eylül 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Nisan 2013.
- ^ "Boron Properties". Los Alamos National Laboratory. 26 Eylül 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 18 Eylül 2008.
- ^ "BORON" (PDF). USGS. 9 Ekim 2022 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 27 Temmuz 2022.
- ^ The Economics of Boron. 11th. Roskill Information Services, Ltd. 2006. ISBN 978-0-86214-516-3.
- ^ "Roskill reports: boron". Roskill. 4 Ekim 2003 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2009.
- ^ "Boron: Statistics and Information". USGS. 16 Eylül 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2009.
- ^ a b c Hammond, C. R. (2004). The Elements, in Handbook of Chemistry and Physics. 81st. CRC press. ISBN 978-0-8493-0485-9.
- ^ "Selected Mechanical and Physical Properties of Boron Filaments" (PDF). NASA. 1966. 22 Şubat 2014 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 20 Eylül 2008. Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Fracture behaviour of boron filaments". Journal of Materials Science. 8 (11): 1581-1589. 1973. doi:10.1007/BF00754893. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Fabrication and Evaluation of Urania-Alumina Fuel Elements and Boron Carbide Burnable Poison Elements Webarşiv şablonunda hata:
|url=value. Boş., Wisnyi, L. G. and Taylor, K.M., in "ASTM Special Technical Publication No. 276: Materials in Nuclear Applications", Committee E-10 Staff, American Society for Testing Materials, 1959 - ^ Carbide, Nitride and Boride Materials Synthesis and Processing. Chapman & Hall (London, New York). 1997. ISBN 978-0-412-54060-8. Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Solozhenko (2009). "Ultimate Metastable Solubility of Boron in Diamond: Synthesis of Superhard Diamondlike BC5" (PDF). Phys. Rev. Lett. 102 (1): 015506. doi:10.1103/PhysRevLett.102.015506. PMID 19257210. 21 Eylül 2017 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 23 Ekim 2017.
- ^ Qin (2008). "Is Rhenium Diboride a Superhard Material?". Advanced Materials. 20 (24): 4780-4783. doi:10.1002/adma.200801471.
- ^ "Cubic form of boron nitride". J. Chem. Phys. 26 (4): 956. 1957. doi:10.1063/1.1745964. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Gogotsi, Y. G.; Andrievski, R.A. (1999). Materials Science of Carbides, Nitrides and Borides. Springer. ss. 270. ISBN 978-0-7923-5707-0. Yazar eksik
|soyadı2=(yardım) - ^ Thompson (1974). "Industrial applications of boron compounds". Pure and Applied Chemistry. 39 (4): 547. doi:10.1351/pac197439040547.
- ^ a b Klotz (1994). "Oral toxicity of boric acid and other boron compounds to immature cat fleas (Siphonaptera: Pulicidae)". J. Econ. Entomol. 87 (6): 1534-1536. doi:10.1093/jee/87.6.1534. PMID 7836612.
- ^ Fundamentals of semiconductor manufacturing and process control. John Wiley and Sons. 2006. ss. 51-54. ISBN 978-0-471-78406-7.
- ^ Semiconductor industry: wafer fab exhaust management. CRC Press. 2005. ss. 39-60. ISBN 978-1-57444-720-0. Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Jeong (5 Nisan 2019). "Wafer-scale and selective-area growth of high-quality hexagonal boron nitride on Ni(111) by metal-organic chemical vapor deposition". Scientific Reports (İngilizce). 9 (1): 5736. doi:10.1038/s41598-019-42236-4. ISSN 2045-2322. PMC 6450880 $2. PMID 30952939.
- ^ Permanent magnet materials and their application. Cambridge University Press. 1996. s. 45. ISBN 978-0-521-56688-9. Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Martin, James E (2008). Physics for Radiation Protection: A Handbook. ss. 660-661. ISBN 978-3-527-61880-4. 3 Haziran 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Ocak 2016.
- ^ Pastina (1999). "The influence of water chemistry on the radiolysis of the primary coolant water in pressurized water reactors". Journal of Nuclear Materials. 264 (3): 309-318. doi:10.1016/S0022-3115(98)00494-2. ISSN 0022-3115.
- ^ Kosanke, B. J.; ve diğerleri. (2004). Pyrotechnic Chemistry. Journal of Pyrotechnics. s. 419. ISBN 978-1-889526-15-7.
- ^ "Borax Decahydrate". 20 Nisan 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2009.
- ^ Davies, A. C. (1992). The Science and Practice of Welding: Welding science and technology. Cambridge University Press. s. 56. ISBN 978-0-521-43565-9.
- ^ Horrocks, A.R.; Price, D. (2001). Fire Retardant Materials. Woodhead Publishing Ltd. s. 55. ISBN 978-1-85573-419-7. Yazar eksik
|soyadı2=(yardım) - ^ Ide, F. (2003). "Information technology and polymers. Flat panel display". Engineering Materials. 51: 84. 13 Mart 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 28 Mayıs 2009.
- ^ "Lockheed SR-71 Blackbird". March Field Air Museum. 4 Mart 2000 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2009.
- ^ Young, A. (2008). The Saturn V F-1 Engine: Powering Apollo into History. Springer. s. 86. ISBN 978-0-387-09629-2.
- ^ Carr (2010). "Wood Protection Properties of Quaternary Ammonium Arylspiroborate Esters Derived from Naphthalene 2,3-Diol, 2,2'-Biphenol and 3-Hydroxy-2-naphthoic Acid". Australian Journal of Chemistry. 63 (10): 1423. doi:10.1071/CH10132.
- ^ "Boric acid". chemicalland21.com. 3 Haziran 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 28 Mayıs 2009.
- ^ Bonvini P (2007). "Bortezomib-mediated 26S proteasome inhibition causes cell-cycle arrest and induces apoptosis in CD-30+ anaplastic large cell lymphoma". Leukemia. 21 (4): 838-42. doi:10.1038/sj.leu.2404528. PMID 17268529.
- ^ "Overview of neutron capture therapy pharmaceuticals". Pharmainfo.net. 22 Ağustos 2006. 23 Temmuz 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 26 Nisan 2013.
- ^ Travers (1990). "Boron and Arthritis: The Results of a Double-blind Pilot Study". Journal of Nutritional Medicine. 1 (2): 127-132. doi:10.3109/13590849009003147.
- ^ "FDA Approves Boron-based Drug to Treat Toenail Fungal Infections". ashp. 8 Temmuz 2014. 8 Aralık 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Ekim 2015. Yazar
|ad1=eksik|soyadı1=(yardım) - ^ Rodriguez (27 Nisan 2016). "New Dioxaborolane Chemistry Enables [18F]-Positron-Emitting, Fluorescent [18F]-Multimodality Biomolecule Generation from the Solid Phase". Bioconjugate Chemistry (İngilizce). 27 (5): 1390-1399. doi:10.1021/acs.bioconjchem.6b00164. PMC 4916912 $2. PMID 27064381.
- ^ Wang (5 Ocak 2017). "18F-positron-emitting/fluorescent labeled erythrocytes allow imaging of internal hemorrhage in a murine intracranial hemorrhage model". Journal of Cerebral Blood Flow & Metabolism (İngilizce). 37 (3): 776-786. doi:10.1177/0271678x16682510. PMC 5363488 $2. PMID 28054494.
- ^ Guo (23 Mayıs 2019). "A fluorescent, [ 18 F]-positron-emitting agent for imaging PMSA allows genetic reporting in adoptively-transferred, genetically-modified cells". ACS Chemical Biology (İngilizce). 14 (7): 1449-1459. doi:10.1021/acschembio.9b00160. ISSN 1554-8929. PMC 6775626 $2. PMID 31120734.
- ^ Aras (March 2021). "Small Molecule, Multimodal [18F]-PET and Fluorescence Imaging Agent Targeting Prostate Specific Membrane Antigen: First-in-Human Study". Clinical Genitourinary Cancer (İngilizce). 19 (5): 405-416. doi:10.1016/j.clgc.2021.03.011. PMC 8449790 $2. PMID 33879400.
- ^ Canfield (2003). "Magnesium Diboride: Better Late than Never" (PDF). Physics Today. 56 (3): 34-41. doi:10.1063/1.1570770. 17 Aralık 2008 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 22 Eylül 2008.
- ^ Braccini (2007). "Development of ex situ processed MgB2 wires and their applications to magnets". Physica C: Superconductivity. 456 (1–2): 209-217. doi:10.1016/j.physc.2007.01.030.
- ^ Wu (2001). "Evaluation of transient liquid phase bonding between nickel-based superalloys". Journal of Materials Science. 36 (6): 1539-1546. doi:10.1023/A:1017513200502.
- ^ Dean (2010). "Boron nitride substrates for high-quality graphene electronics". Nature Nanotechnology. 5 (10): 722-726. arXiv:1005.4917 $2. doi:10.1038/nnano.2010.172. PMID 20729834.
- ^ Gannett (2010). "Boron nitride substrates for high mobility chemical vapor deposited graphene". Applied Physics Letters. 98 (24): 242105. arXiv:1105.4938 $2. doi:10.1063/1.3599708.
- ^ Zettl (2010). "The physics of boron nitride nanotubes". Physics Today. 63 (11): 34-38. doi:10.1063/1.3518210.
- ^ "Essential Plant Micronutrients. Boron in Idaho" (PDF). University of Idaho. 1 Ekim 2009 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 5 Mayıs 2009. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Functions of Boron in Plant Nutrition" (PDF). U.S. Borax Inc. 20 Mart 2009 tarihinde kaynağından (PDF) arşivlendi.
- ^ Blevins (1998). "Functions of Boron in Plant Nutrition". Annual Review of Plant Physiology and Plant Molecular Biology. 49: 481-500. doi:10.1146/annurev.arplant.49.1.481. PMID 15012243.
- ^ "Boron". PDRhealth. 11 Ekim 2007 tarihinde kaynağından arşivlendi. Erişim tarihi: 18 Eylül 2008.
- ^ "Ultratrace elements in nutrition: Current knowledge and speculation". The Journal of Trace Elements in Experimental Medicine. 11 (2–3): 251-274. 1998. doi:10.1002/(SICI)1520-670X(1998)11:2/3<251::AID-JTRA15>3.0.CO;2-Q. Birden fazla yazar-name-list parameters kullanıldı (yardım); Yazar
|ad1=eksik|soyadı1=(yardım) - ^ "Effect of dietary boron on mineral, estrogen, and testosterone metabolism in postmenopausal women". FASEB J. 1 (5): 394-7. 1987. doi:10.1096/fasebj.1.5.3678698. PMID 3678698.
- ^ Boron.
- ^ "Primordial broth of life was a dry Martian cup-a-soup". New Scientist. 29 Ağustos 2013. 24 Nisan 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Ağustos 2013.
- ^ "The tartrolons, new boron-containing antibiotics from a myxobacterium, Sorangium cellulosum". The Journal of Antibiotics. 48 (1): 26-30. 1995. doi:10.7164/antibiotics.48.26. PMID 7532644. 10 Mayıs 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 28 Ağustos 2019.
- ^ Hütter (1967). "Stoffwechselprodukte von Mikroorganismen. 57. Mitteilung. Boromycin". Helvetica Chimica Acta. 50 (6): 1533-1539. doi:10.1002/hlca.19670500612. PMID 6081908.
- ^ Dunitz (1971). "Structure of boromycin". Helvetica Chimica Acta. 54 (6): 1709-1713. doi:10.1002/hlca.19710540624. PMID 5131791.
- ^ Vithana, En (July 2006). "Mutations in sodium-borate cotransporter SLC4A11 cause recessive congenital hereditary endothelial dystrophy (CHED2)". Nature Genetics. 38 (7): 755-7. doi:10.1038/ng1824. ISSN 1061-4036. PMID 16767101.
- ^ Silverman (1953). "Corrections-Colorimetric Microdetermination of Boron by the Curcumin-Acetone Solution Method". Anal. Chem. 25 (11): 1639. doi:10.1021/ac60083a061.
- ^ Nielsen (1997). "Boron in human and animal nutrition". Plant and Soil. 193 (2): 199-208. doi:10.1023/A:1004276311956. 12 Mart 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Nisan 2018.
- ^ Pizzorno (Aug 2015). "Nothing boring about boron". Integrative Medicine. 14 (4): 35-48. PMC 4712861 $2. PMID 26770156.
- ^ "Environmental Health Criteria 204: Boron". the IPCS. 1998. 3 Nisan 2019 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Mayıs 2009.
- ^ "Boron (B) and Chlorine (Cl) for Citrus Trees" (PDF). IFAS Extension. University of Florida. 9 Eylül 2016 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 30 Haziran 2017.
- ^ J. Reuter, Douglas; K. I. Peverill; L. A. Sparrow (1999). Soil Analysis: An Interpretation Manual. Csiro Publishing. ss. 309-311. ISBN 978-0-643-06376-1. 12 Mart 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 30 Haziran 2017.
- ^ M. P. Reynolds (2001). Application of Physiology in Wheat Breeding. CIMMYT. s. 225. ISBN 978-970-648-077-4. 10 Mart 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 30 Haziran 2017.

