İzotop
Bu madde, Vikipedi biçem el kitabına uygun değildir. (Mayıs 2020) |
| Nükleer fizik | ||||||||||||||

| ||||||||||||||
| Radyoaktivite Fisyon Füzyon
| ||||||||||||||

İzotoplar, periyodik tabloda aynı atom numarasına ve konuma sahip olan ve farklı nötron sayıları nedeniyle nükleon sayıları bakımından farklılık gösteren iki veya daha fazla atom türüdür. Belirli bir elementin tüm izotopları neredeyse aynı kimyasal özelliklere sahipken, farklı atomik kütlelere ve fiziksel özelliklere sahiptirler.[1] İzotop terimi, "aynı yer" anlamına gelen Yunan kökenli isos (ἴσος "eşit") ve topos (τόπος "yer") 'den oluşur; isimin anlamı ise, tek bir elementin farklı izotoplarının periyodik tabloda aynı pozisyonda yer alması anlamına gelir.[2] Margaret Todd tarafından 1913 yılında Frederick Soddy'ye öneri olarak sunulmuştur.
Atom çekirdeğindeki proton sayısına atom numarası denir ve nötr (iyonize olmayan) atomdaki elektron sayısına eşittir. Her atom numarası belirli bir elementi tanımlarken, izotopu tanımlamaz; belirli bir elementin atomu, nötron sayısında geniş bir aralığa sahip olabilir. Çekirdekteki nükleonların (hem protonları hem de nötronları) atomun kütle sayısıdır ve belirli bir elementin her izotopu farklı bir kütle numarasına sahiptir.
Örneğin, karbon-12, karbon-13 ve karbon-14, sırasıyla kütle numaraları 12, 13 ve 14 olan karbon elementinin üç izotopudur. Karbonun atom numarası 6'dır, yani her karbon atomunun 6 protonu vardır, böylece bu izotopların nötron sayıları sırasıyla 6, 7 ve 8'dir.
İzotop ve Nüklid[değiştir | kaynağı değiştir]
Nüklit çekirdekte belirli sayıda proton ve nötron bulunduran bir atom türüdür, örneğin 6 protonlu ve 7 nötronlu karbon-13. Nüklid kavramı (tek tek nükleer türlere atıfta bulunarak) kimyasal özellikler üzerindeki nükleer özellikleri vurgular, izotop kavramı ise (her yılda bir defa elementin tüm atomlarını gruplandırarak) nükleer üzerindeki kimyasalları vurgular. Nötron sayısının nükleer özellikler üzerinde büyük etkisi vardır, ancak kimyasal özellikler üzerindeki etkisi çoğu element için önemsizdir. Nötron sayısının atom numarasına oranının izotoplar arasında en çok değişen en hafif elementlerdir ve (hidrojen için, en hafif element olmasına rağmen, izotop etkisi biyolojiyi güçlü bir şekilde etkileyecek kadar büyüktür). İzotoplar terimi (başlangıçta da izotopik elementlerdir.[3] Yani bazen izotopik nüklitler[4]) karşılaştırmayı (eşanlamlılar veya izomerler gibi) ima etmek için tasarlanmıştır, örneğin: nüklitler , , izotoplar (aynı atom numarasına sahip nüklidlerdir, ancak farklı kütle numaraları da vardır[5]), gibi , , izobarlardır). Bununla birlikte, izotop eski bir terimdir, çünkü nüklitten daha iyi bilinir ve bazen nüklitin nükleer teknoloji ve r nükleer tıp gibi daha uygun olabileceği bağlamlarda kullanılır.
Gösterim[değiştir | kaynağı değiştir]
Bir izotop veya nüklit, belirli elemanın adıyla belirtilir (bu atom numarasını gösterir), ardından bir tire ve kütle numarası (örneğin helyum-3,helyum-4, karbon-12, karbon-14, uranyum-235 ve uranyum-239).[6] kimyasal sembolü kullanılır, örneğin "C" karbon, standart gösterim (şimdi olarak bilinen "AZE gösterim" çünkü Bir kütle numarası, Z atom numarası ve element öğesi) olduğunu gösterir, kütle sayısı (nükleon sayısı) ile kimyasal sembolün sol alt tarafına ve sol üst tarafına yazılır (örneğin , , , ve . Atom numarası eleman sembolü tarafından verildiğinden, yalnızca üst simgedeki kütle numarasını belirtmek ve atom numarası alt simgesini (örneğin 3) dışarıda bırakmak yaygındır. (3He, 4He,12C,14C 235U ve 239U). M harfi bazen bir nükleer izomeri, metastabil veya enerjik olarak uyarılmış bir nükleer durumu (en düşük enerjili zemin durumunun aksine) belirtmek için kütle numarasından sonra eklenir, örneğin (tantal-180m). AZE gösteriminin ortak telaffuzu, asıl yazıldığından farklıdır: yaygın olarak dört-iki-helyum yerine helyum-dört ve 235 olarak telaffuz edilir (235-92-uranyum.) yerine (Amerikan İngilizcesi) ile iki-otuz beş veya (İngilizce) -iki-üç-beş olarak telaffuz edilir.
Radyoaktif, ilkel ve kararlı izotoplar[değiştir | kaynağı değiştir]
Bazı izotoplar veya nüklitler radyoaktif ve bu nedenle radyoizotoplar veya radyonüklitler olarak adlandırılır, oysa diğerleri radyoaktif olarak çürümeye hiç rastlanmamıştır ve kararlı izotoplar veya kararlı nüklitler olarak adlandırılır. Örneğin, 14C radyoaktif bir karbon şeklidir, 12C ve 13C kararlı izotoplardır. Yeryüzünde yaklaşık 339 doğal olarak meydana gelen nüklitler vardır,[7] bunların 286 tanesi ilkel nüklitlerdir, yani güneş sisteminin oluşumundan beri var oldukları anlamına gelir.
İlkel nüklitler, çok uzun yarı ömürleri (100 milyon yıldan fazla) olan 34 nüklitleri ve resmi olarak "kararlı nüklitler" olarak kabul edilen 252'leri içerir, çünkü çürümeye rastlanmamıştır. Çoğu durumda, bilinen nedenlerden dolayı, bir elementin kararlı izotopları varsa, bu izotoplar Dünya'da ve güneş sisteminde bulunan element bolluğunda baskındır. Bununla birlikte, üç element (tellür, indiyum ve renyum) durumunda, doğada bulunan en bol izotoplar, aslında bir veya daha fazla kararlı izotopa sahip olan bu elementlere rağmen, elemanın bir (veya iki) son derece uzun ömürlü radyoizotopudur.
Teori, görünüşe göre birçok "kararlı" izotop / nüklitin radyoaktif olduğunu ve son derece uzun yarı ömürlü olduğunu (tüm nüklitleri sonuçta kararsız hale getirecek proton bozulma olasılığını azaltığını) öngörür. Bazı kararlı nüklitler teorik olarak alfa bozulması veya çift beta bozulması gibi bilinen diğer bozulma biçimlerine enerjik olarak duyarlıdır, ancak henüz hiç bozulma ürünü gözlenmemiştir ve bu nedenle bu izotopların "gözlemsel olarak kararlı" olduğu söylenmektedir. Bu nüklitler için öngörülen yarılanma ömürleri genellikle evrenin tahmini yaşını büyük ölçüde aşmaktadır ve aslında yarılanma ömrü evrenin yaşından daha uzun olan 31 bilinen radyonüklid (örneğin Primordial nüklit) bulunmaktadır.
Yapay olarak oluşturulan radyonüklitlere ek olarak,[8] şu anda bilinen 3.339 nüklit vardır[9] Bunlar, kararlı olan veya 60 dakikadan daha uzun yarı ömre sahip 905 nüklidi içerir. Ayrıntılar için nüklitler listesine bakınız.
Geçmiş[değiştir | kaynağı değiştir]
Radyoaktif izotoplar[değiştir | kaynağı değiştir]
İzotopların varlığı ilk olarak 1913'te uranyum ve kurşun arasında radyo elementleri (yani radyoaktif elementler) olarak adlandırılan yaklaşık 40 farklı türün belirtildiği radyoaktif çözülme zincirleri üzerinde yapılan çalışmalara dayanır. Radyocu ve kimyacı olan Frederick Soddy tarafından önerildi, ancak periyodik tabloda sadece 11 kurşun ve uranyum elementleri dahildir.[10][11][12]
Bu yeni radyo elemanlarını kimyasal olarak ayırma girişimleri başarısız olmuştu.[13] Mesela Soddy bu durumu 1910'da göstermişti fakat mesothoriumun (daha sonra olduğu gösterilmiştir 228Ra) radyum (226Ra, uzun ömürlü bir izotop) ve toryum X (224Ra) ayırmak imkânsızdır.[14] Radyo elementleri periyodik tabloya yerleştirme girişimleri, Soddy ve Kazimierz Fajans'ın bağımsız olarak radyoaktif yer değiştirme yasalarını 1913'te, alfa bozunumu periyodik tabloda solda iki yer oluşturduğu sonucuna götürmesine neden oldu.[15] emisyon bir parça sağda bir yer üretti. Soddy, bir alfa parçacığının ve ardından iki beta parçacığının yayılmasının, başlangıç elemanı ile kimyasal olarak özdeş ancak dört birim daha hafif ve farklı radyoaktif özelliklere sahip bir elementin oluşumuna yol açtığını fark etti.
Soddy, çeşitli atom türlerinin (radyoaktif özelliklerde farklılık göstererek) tabloda aynı yeri işgal edebileceğini öne sürdü. Örneğin, uranyum-235'in alfa bozunumu toryum-231'i, aktinyum-230'un beta bozunumu toryum-230'u oluşturur. “aynı yerde” için Yunanca “izotop” terimi, fikirlerini kendisine anlattığı bir konuşma sırasında İskoç bir hekim ve aile dostu Margaret Todd tarafından Soddy'ye önerildi.[16][17][18][19][20] 1921 Nobel Kimya Ödülü'nü kısmen izotoplarla yaptığı çalışmalar nedeniyle kazandı.
1914 yılında T. W. Richards, farklı radyoaktif kökenlere bağlı olarak izotopik kompozisyondaki değişikliklere atfedilebilen, farklı mineral kaynaklarından gelen kurşunun atom ağırlığı arasında farklılıklar buldu.[21]
Kararlı izotoplar[değiştir | kaynağı değiştir]
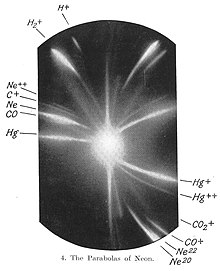
Kararlı (radyoaktif olmayan) bir elementin çoklu izotoplarına yönelik ilk kanıtlar, 1912'de J. J. Thomson tarafından kanal ışınlarının (pozitif iyonlar) bileşimine yaptığı araştırmanın bir parçası olarak bulundu.[22][23] Thomson, neon iyon akışlarını paralel manyetik ve elektrik alanlardan kanalize etti, sapmalarını yollarına bir fotoğraf plakası yerleştirerek ölçtü ve Thomson'ın parabol yöntemi olarak bilinen bir yöntem kullanarak kütlelerini yük oranına hesapladı. Her dere vurduğu noktada plaka üzerinde parlayan bir yama oluşturdu. Thomson, fotografik plaka üzerinde iki ayrı parabolik ışık yaması gözlemledi, bu da oranları yüklemek için farklı kütleye sahip iki çekirdek türü önerdi.
F. W Astonn daha sonra bir kütle spektrometrisi kullanan çok sayıda element için çoklu ve kararlı izotoplar keşfetti. 1919'da Aston, iki izotopik kütlenin 20 ve 22 tam sayılarına çok yakın olduğunu ve neon gazının bilinen molar kütlesine (20,2) eşit olmadığını göstermek için yeterli çözünürlüğe sahip neonu inceledi. Bu Aston'un izotopik kütleler için tam sayı kuralının bir örneğidir, bu da elementel molar kütlelerin tam sayılardan büyük sapmalarının temel olarak elemanın izotopların bir karışımı olması gerçeğinden kaynaklanmaktadır. Aston da benzer şekilde klorun molar kütlesinin (35,45) iki izotop için neredeyse integral kütlelerin ağırlıklı ortalaması olması 35Cl ve 37Cl.[24]
İzotoplar arasındaki özelliklerde değişiklik[değiştir | kaynağı değiştir]
Kimyasal ve moleküler özellikler[değiştir | kaynağı değiştir]
Nötr bir atom, protonlarla aynı sayıya sahiptir. Dolayısıyla, belirli bir elemanın farklı izotoplarının hepsi aynı sayıda elektrona sahiptir ve benzer bir elektronik yapıyı paylaşır. Bir atomun kimyasal davranışı büyük ölçüde elektronik yapısı ile belirlendiğinden, farklı izotoplar neredeyse aynı kimyasal davranış sergiler.
Bunun ana istisnası kinetik izotop etkisidir daha büyük kütleleri nedeniyle, daha ağır izotoplar aynı elementin daha hafif izotoplarından biraz daha yavaş reaksiyona girme eğilimindedir. Bu en protium için bugüne kadar telaffuz edilir protium (1H) döteryum (2H) ve trityum (3H), çünkü döteryumun iki kat protium kütlesi vardır ve trityum, üç kat protium kütlesine sahiptir. Bu kütle farklılıkları, atomik sistemlerin ağırlık merkezini (azaltılmış kütle) değiştirerek ilgili kimyasal bağlarının davranışlarını da etkiler. Bununla birlikte, daha ağır elementler için izotoplar arasındaki nispi kütle farkı ütleüçok daha azdır, böylece kimya üzerindeki kütle farkı etkileri genellikle ihmal edilebilir. (Ağır elementler ayrıca daha hafif elementlerden nispeten daha fazla nötrona sahiptir, bu nedenle nükleer kütlenin kolektif elektronik kütleye oranı biraz daha yüksektir.)
Benzer şekilde, sadece atomlarının izotoplarında (izotopologlar) farklılık gösteren iki molekül aynı elektronik yapıya sahiptir ve bu nedenle neredeyse ayırt edilemez fiziksel ve kimyasal özelliklere sahiptir (yine deuterium ve trityum birincil istisnalardır). Titreşim modları, bir molekülün şekli ile ve onu oluşturan atomlarının kitleler tarafından belirlenir; bu nedenle farklı izotopologlar farklı titreşim modlarına sahiptir. Titreşim modları bir molekülün karşılık gelen enerjilerin fotonlarını emmesine izin verdiğinden, izotopologlar kızılötesi aralıkta farklı optik özelliklere sahiptir.
Nükleer özellikler ve kararlılık[değiştir | kaynağı değiştir]
Ayrıca bakınız: Kararlı nüklid, Kararlı izotop oranı, Nüklid listesi ve İzotopların kararlılığına göre elementlerin listesi

Atom çekirdeği, kuvvetli bir şekilde birbirine bağlı olan protonlardan ve nötronlardan oluşur. Protonlar pozitif yüklü olduğundan, birbirlerini iterler. Elektriksel olarak nötr olan nötronlar, çekirdeği iki şekilde kararlı hale getirirler. Onların copresence protonları biraz ayrı iter ve protonlar arasındaki elektrostatik itme azaltılarak birbirlerine protonlar üzerinde, çekici nükleer kuvvet uygularlar. Bu nedenle, iki veya daha fazla protonun bir çekirdeğe bağlanması için bir veya daha fazla nötron gereklidir. Proton sayısı arttıkça, nötronların kararlı bir çekirdeği sağlamak için gerekli protonlara olan oranı da artar (sağdaki grafiğe bakınız.) Örneğin, nötron: proton oranı 1:2, nötron: proton oranı 3:2'den büyüktür. Bir dizi daha hafif element, 1:1 (Z = N) oranına sahip kararlı nüklidlere sahiptir. Nükleer (kalsiyum -40) gözlemsel olarak aynı sayıda nötron ve protona sahip en ağır kararlı nükliddir (teorik olarak, en ağır kararlı olan kükürt-32'dir.) Kalsiyum-40'tan daha ağır olan tüm kararlı nükleerler protonlardan daha fazla nötron içerir.
Element başına izotop sayısı[değiştir | kaynağı değiştir]
Kararlı bir izotopa sahip 80 elementten, herhangi bir element için gözlemlenen en fazla kararlı izotop sayısı ondur (kalay için). Hiçbir elementin dokuz kararlı izotopu yoktur. Ksenon sadece sekiz kararlı izotoplu tek elementtir. Dört element yedi kararlı izotoplar vardır, sekiz altı kararlı izotoplar vardır, on beş kararlı izotoplar vardır, dokuz dört kararlı izotoplar vardır, beş üç kararlı izotoplar vardır, 16 iki kararlı izotoplar vardır (sayım kararlı olarak) ve 26 elementin sadece tek bir kararlı izotopu vardır (bunlardan 19 tanesi mononüklidik elementlerdir, doğal elementin atom ağırlığını yüksek hassasiyete hakim ve sabitleyen tek bir ilkel kararlı izotopa sahiptir; 3 radyoaktif mononüklidik element de oluşur).[25] Toplamda, çürümeye rastlanmayan 252 nüklid vardır. Bir veya daha fazla kararlı izotopa sahip 80 element için, ortalama kararlı izotop sayısı, element başına 252/80 = 3,15 izotoptur.
Çift ve tek nükleon sayıları[değiştir | kaynağı değiştir]
Proton ve nötron oranı nükleer kararlılığı etkileyen tek faktör değildir. Atom numarası Z'nin eşit olmasına veya tuhaflığına, nötron numarası n'ye ve sonuç olarak toplamına, kütle numarası da A'ya bağlıdır. Hem Z hem de N'nin tuhaflığı, nükleer bağlanma enerjisini düşürme eğilimindedir ve garip çekirdekleri genellikle daha az kararlı hale getirir. Komşu çekirdek arasındaki nükleer bağlanma enerjisindeki bu dikkat çekici fark, özellikle bir izobarlar olan ve kendiliğinden fisyon bozunumu (pozitron emisyon dahil) Beta bozunması tarafından nötron veya proton nonoptimal sayıda kararsız izotoplar. Elektron yakalama, ya da diğer daha az yaygın çürüme modları ve küme çürümenin önemli sonuçları vardır. Kararlı nüklitlerin çoğunluğu evenprotonevenneutrondur, burada tüm sayılar Z, N ve A eşittir. Tek-A kararlı nüklitler (kabaca eşit olarak) tek-proton-hatta-nötron ve evenprotonoddneutron nüklitlerine bölünür. Kararlı tek proton-tek nötron çekirdekleri en az yaygındır. (Aşağıdaki tabloya bakınız.)
| proton
nötron |
ÇÇ | TT | ÇT | TÇ | TOPLAM |
|---|---|---|---|---|---|
| kararlı | 146 | 5 | 53 | 48 | 252 |
| uzun süreli | 22 | 4 | 3 | 5 | 34 |
| tümü ilkel | 168 | 9 | 56 | 53 | 286 |
Atom numarası[değiştir | kaynağı değiştir]
146 çift proton çift nötron (EE) nüklitleri, tüm kararlı nüklitlerin ~%58'ini içerir ve hepsinin eşleştirme nedeniyle sıfır dönüşü vardır. Ayrıca 24 ilkel uzun ömürlü nüklitler vardır. Sonuç olarak, 2'den 82'ye kadar olan 41 çift numaralı elementin, her biri en az bir kararlı izotopa sahiptir ve bu elementlerin çoğunun birkaç ilkel izotopu vardır. Bu çift sayılı elementlerin yarısı altı veya daha fazla kararlı izotopa sahiptir. 2 proton ve 2 nötronun çift eşleştirilmesi nedeniyle helyum-4'ün aşırı kararlılığı, beş ve sekiz içeren nüklitleri önler (, ). Yıldızlarda nükleer füzyon yoluyla daha ağır elementlerin birikmesi için platformlar olarak hizmet edecek kadar uzun süreli olan nükleonlar vardır (bkz. üçlü alfa süreci).
53 kararlı nüklitler çift sayıda protona ve tek sayıda nötrona sahiptir. 3 sayısı da izotoplara kıyasla bir azınlıktır. Kararlı bir nüklide sahip 41 çift-Z elementi arasında, sadece iki element (argon ve seryum) çift - tek kararlı nüklitlere sahip değildir. Bir elementin üç nüklidi (kalay) vardır. Bir çift tek nüklide sahip 24 element ve iki tek çift nüklide sahip 13 element vardır. 35 primordial radyonüklitten, bölünebilirlik dahil olmak üzere dört çift tek nüklit vardır. (aşağıdaki tabloya bakınız)
| çürüme | yarılanma süresi | |
|---|---|---|
| beta | 7.7 x a | |
| alpha | 1.06 x a | |
| alpha | 7.04 x a |
Bölünebilirlik dahil tek nötron sayıları, çift tek nüklidler nötron eşleştirme etkilerinden kaynaklanan enerji nedeniyle büyük nötron yakalama kesitlerine sahip olma eğilimindedir. Bu kararlı-garip, proton-nötron atom bile doğada bolluk tarafından nadir olarak görülür. Çünkü, kendisi de ilkel bolluk içine girmek eğilimindedir. Diğer kararlı-izotop ve nötron yakalama hem S-süreci ve R-sürecinde yıldız nükleosentezi sırasında olmalıdır. Bu nedenle, sadece ve elementlerinin en doğal bol izotoplarıdır.
Tek atom numarası[değiştir | kaynağı değiştir]
Kırk sekiz kararlı tek-proton-çift-nötron nüklitleri, eşleştirilmiş nötronlar tarafından kararlı ve tek sayılı elementlerin kararlı izotopların en önemlisidir ve tek-proton-tek-nötron nüklitlerini içermektedir. 41'in sabit izotopları olan Z = 1 ile 81 arasındaki tek sayılı elementler vardır (elementler teknekyum (43Tc) ve promethium (61Pm) kararlı izotop yok). Bu 39 tek Z elementinden 30 element (0 nötronun çift olduğu hidrojen-1 dahil) tek-çift izotop ve dokuz elemente sahiptir bunlar: klor (17Cl) potasyum (19K) bakır (29Cu) galyum (31Ga), brom (35Br), gümüş (47Ag), antimon (51Sb), iridyum (77Ir) ve talyum (81Tl). Her birinin iki tek çift kararlı izotop vardır. Bu da toplam 30 + 2(9) = 48 kararlı tek çift izotop yapar.
Beş ilkel uzun ömürlü radyoaktif tek çift izotoplar da vardır bunlar: , , , ve 'dir. Son ikisi sadece son zamanlarda çürümeye başladı ve bunların yarı ömürleri 1018 yıldan daha büyüktür.
Sadece beş kararlı nüklit, hem tek sayıda proton hem de tek sayıda nötron içerir. İlk dört "tek-tek" nüklitler düşük kütleli nüklitlerde meydana gelir, bunun için bir protonun bir nötrona değiştirilmesi veya tam tersi çok orantısız bir proton-nötron oranına yol açacaktır (, , ve çevrimi 1, 1, 3, 1). Diğerleri "kararlı" tek - tek nüklit, (9'a çevirmek) ve 252 kararlı izotopun en nadir olduğu düşünülmektedir. Ve henüz deneysel girişimlere rağmen çürüme gözlemlenmemiş olan tek ilkel nükleer izomerdir.[26]
Nispeten kısa yarı ömürleri olan birçok Garip-garip radyonüklit (tantal-180 gibi) bilinmektedir. Genellikle, eşleştirilmiş proton ve nötronlar izobarlar için beta-çürümedir. Dokuz ilkel tek-tek nüklitten (beş kararlı ve uzun yarı ömrü olan dört radyoaktif), sadece ortak bir elementin en yaygın izotopudur. Bunun nedeni, CNO döngüsünün bir parçası olduğu için olmasıdır. Nüklitler ve diğer hafif elementlere kıyasla kendilerini nadir elementlerin azınlık izotopları olarak görürler. Diğer altı izotoplar da kendi elementlerinin az da olsa doğal bolluk yüzdesini oluştururlar.
Tek nötron sayısı[değiştir | kaynağı değiştir]
Tek nötron sayısına sahip aktinitler bölünebilirler (termal nötronlarla), ancak nötron sayısı çift olanlar genellikle hızlı nötronlarla parçalanabilir olsalar da, bu bölünme tam gerçekleşemez. Gözlemsel olarak kararlı tek-tek nüklitlerin sıfır olmayan tam sayı dönüşü vardır. Bunun nedeni, tek eşlenmemiş nötron ile eşlenmemiş protonun, dönüşleri hizasında (anti-hizalanmış yerine en az 1 birim toplam spin üretiyorsa) birbirlerine daha büyük bir nükleer kuvvet çekimine sahip olmalarıdır. Bu nükleer davranışın en basit durumu için döteryuma bakınız.
Sadece, ve 'nin tek nötron numarası ve elementin en doğal bol izotopu vardır. (Aşağıdaki tabloya bakınız.)
| Nötron | even | odd |
|---|---|---|
| kararlı | 194 | 58 |
| uzun ömürlü | 27 | 7 |
| tümü ilkel | 221 | 65 |
Doğanın meydana gelişi[değiştir | kaynağı değiştir]
Elementler bir nüklitten (mononüklidik elementlerden) veya doğal olarak oluşan birden fazla izotoptan oluşur. Kararsız (radyoaktif) izotoplar ilkel veya post primordialdir. İlkel izotoplar, yıldız nükleosentezinin veya kozmik ışın spallation gibi başka bir nükleosentez türünün bir ürünüydü ve çürüme oranları çok yavaş olduğu için günümüze kadar devam etmiştir (örneğin uranyum-238 ve Potasyum-40). Post-primordial izotoplar, kozmik ışın bombardımanı tarafından kozmojenik nüklidler (örneğin, trityum, karbon-14) veya radyoaktif bir radyojenik nüklid gibi (örneğin radyum, uranyum) bir ilkel izotopun çürümesiyle yaratılmıştır. Birkaç izotop doğal nükleojenik nüklidler olarak sentezlenir, diğer bazı doğal nükleer ise reaksiyon tarafından doğal nükleer fisyon olarak sentezlenir. Örnek olarak nötronların başka bir atom tarafından emilmesi verilebilir.
Yukarıda açıklandığı gibi, sadece 80 elementin herhangi bir kararlı izotopu vardır ve bunların 26'sında sadece bir kararlı izotop bulunur. Bu nedenle, kararlı elementlerin yaklaşık üçte ikisi doğal olarak çoklu kararlı izotoplarda yer alır ve bir element için en fazla sayıda sabit izotop sayısıda kalay için ondur(50Sn). Burada, yeryüzünde doğal olarak bulunan yaklaşık 94 element (plütonyum dahil) bulunur, ancak bazıları plütonyum-244 gibi çok küçük miktarlarda tespit edilir. Bilim adamları, Dünya'da doğal olarak meydana gelen elementlerin (bazıları sadece radyoizotop olarak) toplamda 339 izotop (nüklid) olarak meydana geldiğini tahmin ediyorlar.[27] Bu doğal olarak oluşan nüklidlerin sadece 252'si, şimdiki zaman itibarıyla çürümeye hiç rastlanmadıkları görülmüştür. 34 primordial nüklid (toplam 286 primordial nüklid), gibi bilinen yarı ömürleri olan radyoaktifler, güneş sisteminin başlangıcından itibaren 100 milyon yıldan daha uzun yarı ömürleri vardır. (Ayrıntılar için nüklidlerin listesine bakınız.)
Bilinen tüm kararlı nüklidler Dünya'da doğal oluşum olarak meydana gelirler. Ve diğer doğal olarak oluşan nüklidler de radyoaktif olmakla birlikte, nispeten uzun yarı ömürleri nedeniyle ya da devam eden doğal üretimin diğer araçları nedeniyle Dünya'da meydana gelirler. Bunlar yukarıda bahsedilen kozmojenik nüklitler, nükleojenik nüklidler ve uranyum radon ve radyum gibi ilkel bir radyoaktif nüklidin devam eden çürümesiyle oluşan herhangi bir radyojenik nüklidleri içerir.
Doğada bulunmayan 3000 radyoaktif nüklid, nükleer reaktörlerde ve parçacık hızlandırıcılarında oluşturulmuştur. Dünya'da doğal olarak bulunmayan birçok kısa ömürlü nüklid, yıldızlarda veya süpernovalarda doğal olarak oluşturulan spektroskopik analizlerle de gözlemlenmiştir. Örnek olarak da, Dünya'da doğal olarak bulunmayan ancak astronomik ölçekte bolca bulunan alüminyum-26'dır.
Elementlerin tablolandırılmış atomik kütleleri, farklı kütlelere sahip çoklu izotopların varlığını hesaba katan ortalamalardır. İzotopların keşfinden önce, atomik kütlenin ampirik olarak belirlenmiş olmayan değerleri bilim insanlarını şaşırtmıştır. Çünkü, bir klor örneği %75,8 klor-35 ve %24,2 klor-37 içerir ve ortalama bir atomik kütle 35,5 atomik kütle birimi verir.
Genelgeçer kozmoloji teorisine göre, yalnızca hidrojen ve helyumun izotopları eser halde bulunan lityum, berilyum, bor gibi bazı izotopların izlerini taşır. Diğer tüm nüklit yıldızlar ve süpernovada önceden meydana gelmiş enerjik partiküller arasındaki etkileşimle sentezlenirler. Ve bunların tümü Büyük Patlama sırasında oluşmuştur. (İzotop üretiminden sorumlu olduğu düşünülen çeşitli süreçlerin detayları için nükleosenteze bakınız). Dünya üzerindeki izotopların bollukları, bu süreçlerin oluşturduğu miktarlardan, galakside yayılmasından ve kararsız olan izotopların çürüme oranlarından kaynaklanır. Güneş sisteminin ilk birleşmesinden sonra, izotoplar kütleye göre yeniden dağıtıldı ve elementlerin izotopik bileşimi gezegenden gezegene biraz değişti. Bu bazen göktaşlarını izlemeyi mümkün kılabilir.
İzotopların atomik kütlesi[değiştir | kaynağı değiştir]
Atom kütlesi () bir izotopun (nüklid) esas olarak kütle numarası (yani çekirdeğindeki nükleonların sayısı) ile belirlenir. Küçük düzeltmeler, çekirdeğin bağlanma enerjisinden (bkz. kitle hatası), proton ve nötron arasındaki kütle farkından ve atomla ilişkili elektronların kütlesinden kaynaklanır, çünkü elektron ve nükleon oranı izotoplar arasındaki farklılığı gösterir.
Kütle numarası boyutsuz bir miktardır. Öte yandan atomik kütle, karbon-12 atomunun kütlesine dayanan atomik kütle birimi kullanılarak ölçülür. "U" (Birleşik atomik kütle birimi için) veya "Da" (dalton için) sembolleri ile gösterilir. Bir elementin doğal olarak oluşan izotoplarının atomik kütleleri, elementin atomik kütlesini belirler. Element N izotopları içerdiğinde, aşağıdaki ifade ortalama atomik kütle için uygulanır :
m1, m2, ..., mN her bir izotopun atomik kütleleridir ve x1, ..., xN bu izotopların göreceli bolluklarıdır.
İzotopların uygulamaları[değiştir | kaynağı değiştir]
İzotopların saflaştırılması[değiştir | kaynağı değiştir]
Belirli bir elementin çeşitli izotoplarının özelliklerinden yararlanan uygulamalar vardır. İzotop ayrımı önemli bir teknolojik meydan okumadır, özellikle de uranyum veya plütonyum gibi ağır elementler ile bu ayrımı yapmak zordur. Lityum, karbon, azot ve oksijen gibi daha hafif elementler, CO (kobalt) ve NO (nobelyum) gibi bileşiklerinin gaz difüzyonu ile ayrılır. Hidrojen ve döteryumun ayrılması sıra dışıdır, çünkü Girdler sülfür işlemi fiziksel özelliklerden ziyade kimyasallara dayanır. Uranyum izotopları, gaz difüzyonu, gaz santrifüjü, lazer iyonizasyon ayrımı ve (Manhattan projesinde) bir tür üretim kütle spektrometresi ile toplu olarak ayrılmıştır.
Kimyasal ve biyolojik özelliklerin kullanımı[değiştir | kaynağı değiştir]
- İzotop analizi, belirli bir örnekteki gibi bir element izotopunun, izotopik imzasının, göreceli bolluğunun belirlenmesidir. İzotop analizi sıklıkla izotop oranı ile kütle spektrometresi ile yapılır. Özellikle biyojenik maddeler için, C (karbon), N (azot) ve O (oksijen) izotoplarının önemli varyasyonları meydana gelebilir. Bu tür varyasyonların analizi, gıda ürünlerinde[28] tağşiş tespiti gibi geniş bir uygulama yelpazesine veya isoscapes kullanan ürünlerin coğrafi kökenlerine sahiptir. Belirli göktaşlarının Mars kaynaklı olarak tanımlanması, kısmen içinde bulunan eser gazların izotopik imzasına dayanır.[29]
- İzotopik ikame, kinetik izotop etkisi ile bir kimyasal reaksiyon mekanizmasını belirlemek için kullanılabilir.
- Diğer bir yaygın uygulama ise izotopik etiketlemedir. Kimyasal reaksiyonlarda izleyiciler veya belirteçler olarak olağandışı izotopların kullanılmasıdır. Normal de, belirli bir elementin atomları birbirinden ayırt edilemez. Öyle ki, farklı kütlelerin izotoplarını kullanarak, farklı radyoaktif olmayan kararlı izotoplar bile kütle spektrometresi veya kızılötesi spektroskopisi ile ayırt edilebilir. Örneğin, SİLAC' da (hücre kültüründe amino asitlerle kararlı izotop etiketleme) kararlı izotopların proteinleri ölçmek için kullanılır. Radyoaktif izotoplar kullanılıyorsa, yaydıkları radyasyon ile tespit edilebilirler buna da radyoizotopik etiketleme denir.
- İzotoplar, yaygın izotop ve seyreltme yöntemi ile çeşitli elementlerin veya maddelerin konsantrasyonunu belirlemek için kullanılır. İzotopik olarak değişitirilmiş bileşiklerin bilinen miktarlarda numuneler ile karıştırılması ve elde edilen karışımların izotopik imzaları sayesinde kütle spektrometrisi belirlenir.
Nükleer özelliklerin kullanımı[değiştir | kaynağı değiştir]
- Radyoizotop etiketlemeye benzer bir teknik de, radyometrik tarihlemedir. Ayrıca kararsız bir elementin bilinen yarılanma ömrünü kullanarak, bilinen bir izotop konsantrasyonunun varlığından bu yana geçen süre hesaplanabilir. En yaygın olarak bilinen örnek ise, karbonlu malzemelerin yaşını belirlemek için kullanılan radyokarbon tarihlemesidir.
- Çeşitli spektroskopi formları, hem radyoaktif hem de kararlı olan spesifik izotopların benzersiz nükleer özelliklerine dayanır. Örneğin, nükleer manyetik rezonans (NMR) spektroskopisi sadece sıfır olmayan bir nükleer döndürmesi ile izotoplar için kullanılabilir. NMR spektroskopisi ile kullanılan en yaygın nüklidler: 1H, 2D, 15N, 13C ve 31P'dir.
- Mössbauer spektroskopisi aynı zamanda 57Fe (demir) gibi belirli izotopların nükleer geçişlerine de bağlıdır.
- Radyonüklidlerin de önemli kullanımları vardır. Nükleer enerji ve nükleer silahların geliştirilmesi için nispeten büyük miktarlarda spesifik izotop gerektirir. Nükleer tıp ve radyasyon onkolojisi, tıbbi tanı ve tedavi için sırasıyla radyoizotopları kullanmaktadır.
Ayrıca bakınız[değiştir | kaynağı değiştir]
Kaynakça[değiştir | kaynağı değiştir]
Bu madde önerilmeyen biçimde kaynaklandırılmıştır. (Bu şablonun nasıl ve ne zaman kaldırılması gerektiğini öğrenin) |
- ^ Herzog, Gregory F. (2 June 2020). "Isotope"[1] 9 Mayıs 2020 tarihinde Wayback Machine sitesinde arşivlendi. Encyclopedia Britannica.
- ^ Soddy, Frederick (12 Aralık 1922). "İzotopların kavramlarının kökenleri "(PDF). Nobelprize.org. s. 393. Alındı 9 Ocak 2019. Böylece kimyasal olarak özdeş elementler - ya da izotoplar, onları ilk kez bu mektupta doğaya çağırdığım gibi, periyodik tabloda aynı yeri işgal ettikleri için ...
- ^ Soddy, Frederick (1913). "İntra-atomik şarj". Doğa. 92 (2301): 399–400. Bibcode: 1913Natur..92..399S. doi: 10.1038 / 092399c0.
- ^ IUPAP Kırmızı Kitap
- ^ IUPAC Altın kitap
- ^ Anorganik Kimya II (Connelly, N. G.) IUPAC; Damhus, T.; İnorganik Kimya Hartshorn, R. M.; ve Hutton, A. T., İsimlendirme – IUPAC Tavsiyelerine 2005, Kimya Royal Society, 2005; IUPAC (McCleverty, J. A.; ve Connelly, N. G.), İsimlendirme. Muhtemelen 1958 İlk Baskı Kimya 2000 öneriler, Royal Society, 2001; (öneriler 1990) İnorganik Kimya IUPAC (Leigh, G. J.), İsimlendirme, Blackwell Science, 1990; İnorganik Kimya IUPAC, İsimlendirme, İkinci Baskı, 1970; de
- ^ "Dünyadan Kayıp Radyoaktifler"
- ^ Bu gösterim 1930'ların ikinci yarısında ortaya çıkmış gibi görünüyor. Bundan önce, neon-22 (1934) için Ne (22), neon-22 (1935) için Ne22 ve hatta kurşun-210 (1933) için Pb210 gibi çeşitli gösterimler kullanıldı.
- ^ "NuDat 2 Açıklama". 2 Ocak 2016'da Alındı.
- ^ Choppin, G.; Liljenzin, Jo; Rydberg, J. (1995). Radiochemistry and Nuclear Chemistry (İngilizce) (2. bas.). Butterworth-Heinemann. ss. 3-5.
- ^ Diğerleri de izotopların olasılığını önermişti; örneğin: (1909) Strömholm, Daniel ve Svedberg Theodor "Untersuchungen über Chemie der radyoaktif Grundstoffe II ölür." 2 (kimya soruşturma radyoaktif unsurlar), Zeitschrift für Chemie anorganischen, 63: 197-206; özellikle 206.sayfaya bakın. Alexander Thomas Cameron, Radyokimya (Londra, İngiltere: JM Dent & Sons, 1910), s. 141. (Cameron ayrıca yer değiştirme yasasını da bekliyordu .)
- ^ Ley, Willy (Ekim 1966). "Gecikmeli Keşif". Bilginize. Galaxy Bilimkurgu. sayfa 116-127.
- ^ Scerri, Eric R. (2007) Periyodik Tablo Oxford University Press, s. 176–179 ISBN 0-19-530573-6
- ^ Nagel, Miriam C. (1982). "Frederick Soddy: Kimyadan İzotoplara". Kimya Eğitimi Dergisi. 59 (9): 739-740. Bibcode: 1982JChEd..59..739N. DOI: / ed059p739 10.1021.
- ^ Görmek: Kasimir Fajans (1913) "Über eine Beziehung zwischen der Art einer radioaktiven Umwandlung und dem elektrochemischen Verhalten der betreffenden Radioelemente" (Radyoaktif dönüşümün türü ve ilgili radyoaktif elementlerin elektrokimyasal davranışı arasındaki ilişki üzerine), Physikalische Zeitschrift, 14: 131 -136. Soddy "yerinden edilme yasasını" açıkladı: Soddy, Frederick (1913). "Radyo Elemanları ve Periyodik Yasa". Doğa. 91 (2264): 57-58. Bibcode: 1913Natur..91 ... 57S. DOI: / 091057a0 10.1038 .. Soddy, yerinden edilme yasasını şu şekilde detaylandırdı: Soddy, Frederick (1913) "Radyoaktivite", Kimya Derneği Faaliyet Raporu, 10: 262-288. Alexander Smith Russell (1888–1972) ayrıca bir yerinden edilme yasası yayınladı: Russell, Alexander S. (1913) "Periyodik sistem ve radyo elemanları," Chemical News ve Journal of Industrial Science, 107: 49–52
- ^ Soddy ilk önce "izotop" kelimesini kullandı: Soddy, Frederick (1913). "Atom içi yük". Doğa. 92 (2301): 399-400. Bibcode: 1913Natur..92..399S. DOI: / 092399c0 10.1038.
- ^ Fleck, Alexander (1957). "Frederick Soddy". Kraliyet Cemiyeti Arkadaşlarının Biyografik Anıları. 3: 203-216. doi: 10,1098 / rsbm.1957.0014. s. 208: 1913'e kadar 'kimyasal olarak ayrılamayan radyo elementleri' ifadesini kullandık ve o sırada Soddy'nin kayınpederi Sir George'un evinde Dr. Margaret Todd ile bir salon tartışmasında izotop kelimesi önerildi. Beilby.
- ^ Budzikiewicz H, Grigsby RD (2006). "Kütle spektrometrisi ve izotopları: bir asırlık araştırma ve tartışma". Kütle Spektrometresi Yorumları. 25 (1): 146-57. Bibcode: 2006MSRv ... 25..146B. doi: 10.1002 / mas.20061. PMID 16134128.
- ^ Scerri, Eric R. (2007) Periyodik Tablo, Oxford University Press, ISBN 0-19-530573-6, Ch. 6, not 44 (s. 312), Soddy'nin eski bir öğrencisi olarak tanımlanan Alexander Fleck'ten bahsediyor.
- ^ William T. Preyer, 1893 kitabında elementler arasındaki benzerlikleri göstermek için "izotop" kelimesini de kullandı. S. William T. Preyer, Das genetische System der chemischen Elemente [Kimyasal elementlerin genetik sistemi] (Berlin, Almanya: R. Friedländer ve Sohn, 1893): "Die ersteren habe ich der Kürze wegen izotop Elemente genannt, weil sie jedem der sieben içinde Stämmme der gleichen Ort, nämlich dieselbe Stuffe, einnehmen. " (Kısacası, eski "izotopik" elementleri adlandırdım, çünkü yedi ailenin her birinde [yani periyodik tablonun sütunları], yani aynı adımı [yani, periyodik sıra tablo]).
- ^ İzotop kavramlarının kökenleri Frederick Soddy, Nobel ödül dersi
- ^ Thomson, J.J. (1912). "XIX. Pozitif ışınlar üzerinde ileri deneyler". Felsefi Dergi. Seri 6. 24 (140): 209-253. DOI: / 14786440808637325 10.1080.
- ^ Thomson, J.J. (1910). "LXXXIII. Pozitif elektrik ışınları". Felsefi Dergi. Seri 6. 20 (118): 752-767. DOI: / 14786441008636962 10.1080.
- ^ Kitle spektrumları ve izotoplar Francis W. Aston, Nobel ödül dersi 1922
- ^ Sonzogni, Alejandro (2008). "Nüklidlerin Etkileşimli Grafiği". Ulusal Nükleer Veri Merkezi: Brookhaven Ulusal Laboratuvarı. Erişim tarihi: 2013-05-03.
- ^ Hult, Mikael; Wieslander, J.S .; Marissens, Gerd; Gasparro, Joël; Wätjen, Uwe; Misiaszek, Marcin (2009). "Bir yeraltı HPGe sandviç spektrometresi kullanarak 180mTa radyoaktivitesini arayın". Uygulamalı Radyasyon ve İzotoplar. 67 (5): 918-21. doi: 10.1016 / j.apradiso.2009.01.057. PMID 19246206.
- ^ "Dünyadan Kayıp Radyoaktifler". Erişim tarihi: 2012-06-16.
- ^ Jamin, Eric; Guérin, Régis; Rétif, Mélinda; Lees, Michèle; Martin, Gérard J. (2003). "Portakal Suyunda İlave Suyun Su ve Şekerlerden Elde Edilen Oksijen-18 / Oksijen-16 İzotop Oranlarının Eşzamanlı Tayini ile Geliştirilmesi". J. Agric. Food Chem. 51 (18): 5202-6. DOI: 10.1021 / jf030167m. PMID 12926859.
- ^ Treiman, A.H .; Gleason, J.D .; Bogard, D.D. (2000). "SNC meteoritleri Mars'lıdır". Gezegen. Space Sci. 48 (12–14): 1213. Bibcode: 2000P ve SS ... 48.1213T. DOI: 10.1016 / S0032-0633 (00) 00.105-7.






































