Kronik obstrüktif akciğer hastalığı
| Kronik obstrüktif akciğer hastalığı | |
|---|---|
| Diğer adlar | Kronik obstrüktif hava yolu hastalığı (KOHYH) |
 | |
| Genellikle sigaranın neden olduğu ve KOAH'ın önemli bir özelliği olan lobül merkezinde genişlemiş hava boşlukları ile sentrilobüler amfizem gösteren bir akciğer kesiti | |
| Olağan başlangıcı | 35 yaş üzeri[1] |
| Uzmanlık | Göğüs hastalıkları |
| Belirtiler | Nefes darlığı, kronik öksürük[1] |
| Komplikasyon | anksiyete, depresyon, Cor pulmonale, pnömotoraks[2][1] |
| Süre | Uzun dönem[1] |
| Nedenleri | Tütün kullanımı, hava kirliliği, genetik[3] |
| Tanı | Spirometri[4] |
| Ayırıcı tanı | Astım, kalp yetmezliği, bronşektazi, verem, bronşiolitis obliterans, diffüz panbronşiyolit[5] |
| Korunma | Sigarayı bırakmak, iç ve dış mekan hava kalitesinin iyileştirilmesi, tütün kontrolü ölçümleri[3][6] |
| Tedavi | Pulmoner rehabilitasyon, uzun süreli oksijen tedavisi, akciğer hacim küçültme ameliyatı[6] |
| İlaç | İnhale bronkodilatörler ve steroidler[6] |
| Sıklık | 174,5 milyon (2015)[7] |
| Ölüm | 3,2 milyon (2019)[3] |
Kronik obstrüktif akciğer hastalığı (KOAH), akciğerlerdeki hava akımında görülen kronik ve yineleyen engellemelerin görüldüğü bir hastalık topluluğudur.[8][9][10][11][12][13] Ana belirtileri nefes darlığı, öksürme ve balgam üretimidir.[8][9][10][11][12] KOAH'nın dört ana tipi vardır: kronik bronşit, amfizem (emfizem), bronşiektazi ve bronşiyal astım.[8][9][10][11][12] Solunum güçlüğü (dispne) ana bulgudur. Astımdaki solunum güçlüğü, hava kanallarının daralması; bronşiektazi ile emfizem ise akciğerin elastik yapısının bozulması sonucu ortaya çıkar.
Tütün kullanımı hastalığın en temel nedeni olup hava kirliliği ve genetik gibi daha az etkili nedenleri de vardır.[9][11][12][13] Gelişmekte olan ülkelerde, hava kirliliğinin en etkili nedenlerinden biri doğru havalandırılmamış yemek pişirme ve ısıtma ateşi dumanıdır. Bu tahriş edici şeylere uzun süreli maruz kalmalar, akciğerlerde enflamasyonlara neden olarak küçük hava yollarının daralmasına ve amfizem adı verilen doku parçalanmasına yol açar.[14] Teşhis, zayıf hava akışını kontrol eden akciğer fonksiyon testleri ile anlaşılır.[15] Astımdan farklı olarak, kronik bronşit, amfizem ve bronşiektazi hastalarında hava akışı herhangi bir ilaç yardımıyla belirgin bir şekilde düzelemez.
KOAH, bilinen nedenlere maruz kalınımı düşürerek önlenebilir. Bunlar arasında sigara içme oranlarını azaltmak ve iç/dış hava kalitesini yükseltmek gösterilebilir. KOAH tedavisi, sigarayı bırakma, aşılar, rehabilitasyon, düzenli aralıklarla solunum yoluyla alınan bronkodilatörler ve steroidler yoluyla sağlanır. Bazı insanlar, uzun süreli oksijen terapisi veya akciğer nakliyle belirgin iyileşmeler gösterebilir.[14] Akut alevlenme atakları gösteren hastalarda, artan oranlarda ilaç ve hastane altında gözetim gerekebilir.[13][16]
2015 itibarıyla KOAH dünyada 174,5 milyon insanı etkilemektedir ve bu sayı dünya nüfusunun %2,4'üne karşılık gelmektedir; özellikle 40 yaş üstü insanlarda görülür. Erkeklerde ve kadınlarda hemen hemen aynı oranlarda görülür.[17] 1990 yılında 2,4 milyon kişinin ölümüne sebep olan KOAH, 2015 yılında 3,2 milyon insanın ölüm sebebi oldu.[18] Bu ölümlerin %90'ı gelişmekte olan ülkelerde gerçekleşti.[17] Gelişmekte olan ülkelerde sigara kullanımının giderek artması ve dünyadaki birçok ülkede yaşlı nüfus oranının artması sebebiyle KOAH sebepli ölüm oranlarının artması öngörülmektedir.[19] Hastalığın 2010 yılında dünya çapında 2.1 trilyon dolarlık bir zarara yol açtığı tahmin edilmektedir.[20]
Belirtiler[değiştir | kaynağı değiştir]
KOAH'ın en belirgin belirtisi balgam üretimi, nefes darlığı ve sık öksürmelerdir.[8][9][10][11][12][21] Bu belirtiler, uzun sürelere yayılmış bir şekilde görülür[12] ve tipik olarak zamanla kötüleşir.[14] KOAH'ın farklı tiplerinin olup olmadığı kesinleştirilmiş değildir.[22] Önceden amfizem ve kronik bronşit olarak ayrılan hastalıkta, amfizem aslında bir hastalıktan ziyade akciğerdeki değişimleri belirtmek adına kullanılır. Kronik bronşit ise, KOAH hastalığına eşlik edip etmeyeceği kesin olmayan, sadece bazı belirtileri açıklayan bir terimdir.[8]
Öksürme[değiştir | kaynağı değiştir]
Kronik öksürmeler gözlenebilen ilk belirtilerdir.[8][9][10][11][12] İki yıldan uzun bir sürede, yılda üç aydan fazla süren ve balgam üretiminin eşlik ettiği durum, fazladan herhangi bir açıklama yapılmadığı sürece kronik bronşit tanımına dahil olur. Bu durum, KOAH tamamen başlamadan önce de görülebilir. Üretilen balgam miktarı, saatler veya günler arasında farklılık gösterebilir. Bazı durumlarda, öksürük görülmeyebilir ve sıklıkla gözlenmeyen bir biçimde rastlanılabilir. Bazı insanlar bu belirtileri sigaraya atfederler. Balgam, toplumsal ve kültürel koşullara göre yutulup tükürülebilir. Kuvvetli öksürmeler kaburga kırılması veya kısa süreli bilinç kaybına sebebiyet verebilir. KOAH tanısı konulan insanların genelde uzun süren "nezle" geçmişleri vardır.[21]
Nefes kesilmesi[değiştir | kaynağı değiştir]
 |
|
| Dinlerken sorun mu yaşıyorsunuz? Medya yardımı alın. | |
Nefes darlığı hastaların en çok şikayet ettiği belirtidir.[8][9][10][11][12][23] Bu durum sıklıkla şöyle tanımlanır: "zorlukla nefes alıyorum", "nefesim kesiliyor" veya "yeterince hava alamıyorum".[23] Ancak farklı terimler farklı kültürlerde kullanılabilir.[21] Tipik olarak nefes darlığı, uzun süreli güç harcama durumlarında daha kötü bir hal alır ve zamanla kötüleşir.[21] İleri vakalarda dinlenme sırasında da gözlenebilir ve sürekli gözlenebilir.[24][25] Bu durum, KOAH hastalarının endişe duyduğu ve hayat kalitesini düşüren en başlıca belirtidir.[21] Daha ileri düzey KOAH hastaları büzülmüş dudaklarından nefes alır ve bu bazı durumlarda nefes darlığını iyileştirebilir.[26][27]
Diğer belirtiler[değiştir | kaynağı değiştir]
KOAH hastalarında nefes vermek nefes almaktan uzun sürebilir[28] Göğüs sıkışması görülebilir, ancak çok yaygın değildir ve başka bir durumdan dolayı kaynaklanabilir.[21] Nefes yolları engellenmiş hastalar hırıldayabilir veya nefes alırken stetoskoba daha az ses verebilir.[28] Fıçı göğüs de KOAH hastalığının karakteristik belirtisidir ancak görece daha az rastlanır.[28] Tripod pozisyonu hastalık kötüleştikçe gözlenebilir.[12]
İleri düzey KOAH, akciğer arterlerinde yüksek basınca neden olabilir ve bu nedenle kalbin sağ karıncığına baskı uygulayabilir.[14][29][30] Cor pulmonale olarak adlandırılan bu durum, bacak şişmesine[21] ve şişen boyun damarına neden olabilir.[14] KOAH, diğer bütün akciğer hastalıklarından daha büyük bir cor pulmonale tetikleyicisidir.[29] Ancak, cor pulmonale, oksijen tedavisinin kullanımından beri daha az yaygındır.[12]
KOAH, daha çok paylaşılan risk faktörleri nedeniyle, diğer bazı durumlarla beraber gerçekleşir.[22] Bunlar arasında koroner arter hastalığı, yüksek kan basıncı, diyabet, kas yıkımı, osteoporoz, akciğer kanseri, anksiyete bozukluğu ve depresyon yer alır.[22] Ciddi hastalıkları olan insanlarda hâlsizlik yaygın görülür.[21] Çomak parmak, KOAH'ya özgü değildir ve altta yatan bir akciğer kanseri için araştırmaları tetiklemelidir.[31]
Alevlenme[değiştir | kaynağı değiştir]
Akut alevlenme, KOAH hastası bireylerde görülen, artan nefes kesilmeleri, artan balgam üretimi, balgamın temizden yeşil/sarı renge dönmesi, öksürüklerin artması olarak tanımlanabilir.[28] Bu durum, yükselen soluk almanın bulgularına da eşlik edebilir: hızlı nefes alma, yüksek kalp hızı, terleme, etkin solunum kası kullanımı, derinin mavileşmesi, konfüzyon veya ciddi alevlenmelerde görülen hırçın davranışlar.[28][32] Stetoskopla yapılan incelemelerde akciğer üstünden ral duyulabilir.[33]
Nedenleri[değiştir | kaynağı değiştir]
KOAH'ın en temel nedeni tütün kullanımıdır.[8][9][10][11][12] Bunun yanında, bazı ülkelerde mesleki nedenlerle beliren maruz kalmalar ve hava kirliliği de sebep olarak gösterilmektedir.[8] Tipik olarak bu semptomların oluşabilmesi için, maruz kalmanın birkaç on-yıl öncesinde olmuş olması gerekir.[8] İnsanların genetik yatkınlığı da hastalığa katkıda bulunabilir.[8]
Tütün kullanımı[değiştir | kaynağı değiştir]
Küresel olarak KOAH'ın bir numaralı risk faktörü tütün kullanımıdır.[8][9][10][11][12] Tütün ürünlerinin içeriğinde 43’ü kanserojen olan 4000 kimyasal madde vardır. Bu maddeler kanser ve kanser-dışı çok sayıda hastalıklara neden olur.[9] Kanser-dışı hastalıklar arasında KOAH ilk sırada yer alır; tütün kullanan insanların %20'si KOAH hastalığına yakalanır.[35] Ancak hayat boyu tütün kullananlar için bu oran %50'lere yükselir.[36] ABD ve İngiltere'de, KOAH hastalarının %80-95 kadarı ya tütün kullanıcısıdır ya da hayatlarının bir kısmında tütün kullanmıştır.[35][37][38] Hastalığa yakalanma riski toplam tütün kullanım süresiyle doğru orantılı olarak artmaktadır.[39] Ek olarak, kadınlar erkeklere oranla tütünün zararlarına karşı daha büyük hassasiyet gösterirler.[38] Tütün kullanmayanlarlarda pasif içiciler durumların %20'sini oluştururlar.[37] Marijuana, puro, nargile gibi diğer benzer kullanımlar da risk barındırır.[8] Hamilelik sırasında tütün kullanan kadınlar çocuklarındaki KOAH riskini arttırabilirler.[8]
Solunum yollarına giren tütün dumanı (aktif/pasif) öncelikle akciğerlerde dokuları savunmak için bulunan polimorf lökositlerden ve makrofajlardan yoğun bir elastaze (elastik lifleri eriten enzim) deşarjına neden olurken, serbest oksijen radikallerinin oluşmasını tetikler. Serbest oksijen radikalleri, elastaze enzimini bloke eden α1-antitripsin (α1-AT) aktivitesini engeller. Bu etki KOAH hastalığının başlangıcıdır.[9]
- Tütün nedenli kanserler: Akciğer, mesane, pankreas, larinks, uterus serviksi.[9]
- Tütün nedenli kanser-dışı hastalıklar: KOAH, ateroskleroz, iskemik kalp hastalıkları, hipertansiyon, gastrit, endarteritis obliterans (Bürger hastalığı).[9]
Hava kirliliği[değiştir | kaynağı değiştir]
Kömür veya odun ve tezek gibi biyoyakıtlarla yakılan pişirme ateşleri kötü havalandırıldığında bölge havasının kalitesi düşer.[9] Bu durum gelişmekte olan ülkelerde KOAH'ın en temel sebeplerinden biridir.[40] Bu tip ateşler, neredeyse 3 milyar insan için pişirme ve ısınma kaynağı olup maruz kalma oranları daha yüksek olduğu için özellikle kadınlar için risk oluşturur.[8][40] Bu kullanım, Hindistan, Çin ve Sahraaltı Afrika'daki evlerin %80'inin enerji kaynağıdır.[41]
Şehirlerde yaşayan insanların, kırsal alanlarda yaşayan insanlara oranla KOAH'a yakalanma oranı daha yüksektir.[42] Kentsel hava kirliliği alevlenmeler için katkı sağlayan bir faktör olup hastalığa neden olmadaki rolü kesinlik kazanmamıştır.[8] Egzoz gazı kaynaklı olanlar da dahil olmak üzere, kötü hava kalitesi olan yerlerde KOAH oranları daha yüksektir.[9][10][11][12][41] Tüm bunlara rağmen bu faktörlerin, tütün kullanımına oranla daha düşük risk taşıdığına inanılmaktadır.[8]
Meslek hastalığı[değiştir | kaynağı değiştir]
İş yeri kaynaklı tozlar, kimyasallar ve dumanlara yoğun ve uzun süre maruz kalmak, tütün kullanan veya kullanmayan herkes için KOAH riskini yükseltir.[43] Mesleksel etkilenmelerin toplam vakaların %10-20'sine neden olduğuna inanılmaktadır.[44][45] ABD'de bu şartların tütün kullanmamış KOAH hastalarının %30'undan fazlasına neden olduğu, yeterli yasaların olmadığı ülkelerde bunun daha da yükseldiği belirtilmektedir.[8]
Bazı sanayiler ve kaynakların hastalıkla bağlantılı olduğu gösterilmiştir:[41][44] kömür madeni tozu, altın madenciliği, pamuk tekstil sanayi, kadmiyum ve izosiyanat içeren uğraşlar, kaynak dumanları vb.[43] Tarımla ilgili işler de risk taşır.[41] Bazı mesleklerin sahip olduğu risk, yarım ila iki paket sigara tüketiminin verdiği riskle eşdeğer gösterilir.[46] Silika tozuna maruz kalmak da, silikozis riskinden bağımsız olarak KOAH ile sonuçlanabilr.[47] Toz ve sigaradan etkilenmenin olumsuz etkileri aditif veya muhtemelen aditiften de fazladır.[46]
Genetik[değiştir | kaynağı değiştir]
KOAH gelişiminde genetiğin rolü vardır.[8] Akrabalarından KOAH hastası olan tütün kullanıcılarının, olmayan tütün kullanıcılarına göre hastalığa yakalanma riski daha yüksektir.[8] Şimdilik, açık bir şekilde kalıtsal olarak aktarılan risk faktörü AAT'dir.[48] Bu risk, AAT kusurlu olan ve tütün kullanan bireylerde daha da yüksektir.[48] Bu, tüm vakaların %1–5'inin nedenidir[48][49] ve durum 10.000 kişiden 3-4 kişide görülür.[12] Diğer genetik faktörler araştırılmaktadır[48] ve çok olduğu öngörülmektedir.[41]
Diğer[değiştir | kaynağı değiştir]
Bazı diğer etmenler, KOAH ile daha yakından alakalıdır. Risk, yoksul insanlar için daha yüksektir. Ancak bunun doğrudan yoksullukla mı, yoksa yoksulluğun yol açtığı diğer etmenlerle (hava kirliliği, yetersiz beslenme) mi ilgili olduğu kesin değildir.[8] Astım veya solunum yolu hiperaktivitesi olan insanlarda yükselen KOAH oranları olduğuna dair bulgular bulunmaktadır.[8] Düşük doğum ağırlığı gibi doğumsal etmenler, KOAH ve bazı enfeksiyon hastalıklarına yakalanma riskini arttırır.[8] Zatürre gibi solunum enfeksiyonlarının, en azından yetişkinler için, KOAH ile yakından bir ilişkisi olmadığı görülmektedir.[12]
Alevlenme[değiştir | kaynağı değiştir]
Akut alevlenme (semptomların aniden kötüleşmesi),[50] sıklıkla enfeksiyonlar, çevresel kirleticiler ve hatta yanlış ilaç kullanımıyla tetiklenebilir.[51] Vakaların %50 ila 75'inin enfeksiyonlarla tetiklendiği görülmektedir[51][52] (bakterili olanlar %25, viral olanlar %25, ikisi birden %25).[53] Çevresel kirleticiler arasında kötü iç veya dış hava kalitesi yer alır.[51] Kişisel veya pasif olarak tütün dumanı da riski arttırır.[41] Alevlenme dönemlerinin daha çok kışın olduğu düşünüldüğünde soğuk havanın da tetikleyebileceği görülmektedir.[54] Altta yatan ağır hastalıklara sahip hastalar, alevlenmeyi daha sık yaşar: hafif hastalıklarda yılda 1,8 kez, orta derecedeki hastalıklarda yılda 2 ila 3 kez ve ağır hastalıklarda yılda 3,4 kez.[55] Sık alevlenme yaşayanlarda akciğer işlevi daha hızlı oranlarda kayba uğrar.[56] Pulmoner emboli (akciğerdeki kan pıhtıları) KOAH sahibi hastaların durumunu daha da kötüleştirir.[22]
Patofizyoloji[değiştir | kaynağı değiştir]

KOAH, kronik olarak havanın kesintili olarak iletildiği (solunum yolu sınırlanımı) ve tamamen nefes vermenin mümkün olmadığı (hava kapanı) bir obstrüktif akciğer hastalığıdır.[22] Zayıf hava akışı, akciğer dokusunda beliren yıkım (amfizem) ve obstrüktif bronşiyolit olarak bilinen küçük solunum yolu hastalığından kaynaklanmaktadır. Bu etmenlerin hastalığa katkısı kişiden kişiye değişiklik gösterebilir.[8] Küçük solunum yolundaki ciddi yıkımlar, akciğer dokusunun yerine büyük hava ceplerinin—bül olarak bilinir— oluşumuna neden olabilir. Hastalığın bu tipi büllöz veya kabarcıklı amfizem olarak adlandırılır.[57]
KOAH, ciğere çekilen tahriş ediciler sonucu kronik yangısal bir hastalık olarak gelişir.[8] Kronik bakteriyel enfeksiyonlar da bu yangısal duruma eklenebilir.[56] Yangısal hücreler, beyaz kan hücrelerinden ikisi olan nötrofil granülositler ve makrofajlar içerebilir. Tütün kullanan hastalarda Tc1 lenfosit görülebilirken, bazı hastalarda astımdakine benzer bir şekilde eozinofile rastlanabilir.[9] Bu hücresel yanıtların bir kısmı yangısal mediyatörler kemotaktik etmenler nedeniyle tetiklenir.[9][10] Akciğer yıkımıyla ilintili diğer süreçler arasında, tütün kullanımından kaynaklanan yüksek yoğunlukta serbest radikallerin yol açtığı oksidatif stres ve akciğerlerdeki bağ dokunun proteaz inhibitörleri tarafından yetersizce durdurulan proteazlar tarafından yıkımı yer alır.[9][10] Bağ dokunun yıkımı, amfizeme sebep olan sebeptir ve bu durum zayıf hava akışına ve en sonunda solunum gazlarının zayıf olarak emilip serbest bırakılmasına katkıda bulunur.[8] Hastalıkta gerçekleşen kas yıkımı, akciğerler tarafından kana salınan yangısal mediyatörler sebebiyle gerçekleşebilir.[8][9]
Solunum kanallarının daralması, yangı ve ülser oluşumu sebebiyle gerçekleşir. Bu durum tamamen nefes verememeyle sonuçlanır.[9] Hava akışı sırasında en büyük akış düşüşü, nefes verme sırasında gerçekleşir. Bunun sebebi, nefes verme sırasında göğüste oluşan basıncın hava yollarını baskılamasıdır.[58] Akciğerde önceki nefes verilmeden yeni nefes alınması, akciğerlerin toplamda daha büyük hacimde hava barındırmasına yol açar. Bu durum hiperenflasyon veya hava kapanı olarak adlandırılır.[58][59] Egzersiz sırasındaki hiperenflasyon KOAH'taki nefes kesilmesiyle ilişkilidir çünkü akciğerlerde halen bir miktar hava varken daha fazla hava almaya çalışmak rahatsızlık verir.[60] Bazı hastalarda, astıma benzer bir şekilde, tahriş edicilere karşı aşırı solunum duyarlılığı görülür.[12]
Tıkalı solunum yolundan kaynaklanan azalan havalanımdan kaynaklanan düşük oksijen düzeyi ve en sonunda kanda yükselen karbon dioksit değerleri ile hiperenflasyon ve nefes alma isteksizliği görülebilir.[8] Alevlenmeler sırasında solunum yanıgısı da yükselir. Bu durum aynı şekilde hiperenflasyonuna ve azalan solunum gazı değiş tokuşuna yol açar. Bu durumun sebep olduğu düşük kan oksijen seviyeleri, uzun süre devam ettiği takdirde kan damarlarında daralmalara (azokonstriksiyon), amfizem ise akciğerlerdeki kılcal damarların yıkımına yol açabilir.[14] Bu iki değişiklik de pulmoner arterde kan basıncını yükseltir ve cor pulmonale'ye neden olur.[8][9][61]
KOAH: Klinik-Patoloji Türleri[değiştir | kaynağı değiştir]
Kronik bronşit[değiştir | kaynağı değiştir]
Kronik bronşit, KOAH’ın başlangıç evresidir. Tütün kullananlarda kullanmayanlara oranla 4-10 kat daha fazla görülür. Yıllar süren kronik bronşit olgularında pulmoner hipertansiyon ve bronş epitelinde metaplazi kaçınılmaz komplikasyonlardır.[9]
Patoloji: Bronş mukozalarında zaman zaman alevlenen kronik yangı bulguları vardır. Kimyasal maddelerin etkisini azaltmak ve bronşları yıkamak amacıyla sıvı üretimini arttırmak için mukus üreten hücrelerin sayısı artar. Ancak, epitel silialarının silinmesi nedeniyle artan mukus (balgam) bronşial boşluklarda birikerek hava akımını engeller. Biriken mukus bakteri üremesi için çok uygun bir ortamdır; bu nedenle, akut bronşit ve ileri olgularda bronkopnömoni atakları görülür.[9][10][12][13]
Bronşiektazi[değiştir | kaynağı değiştir]
Bronşiektazi, bronş ve bronşiollerin tümünde görülen bir kronik-nekrozlu yangı tablosudur. İleri olgularda hava kanallarında dönüşü olmayan (irreversibl) genişlemeler oluşur. Öksürük ve irinli balgam önemli klinik bulgulardır. Pnömoni en önemli ve sık görülen komplikasyondur.[9][10][11][12][13] Solunum sistemi tümörlerindeki ve yabancı cisim kaçmalarındaki bronş tıkanması akciğerin yalnızca bir segmentini etkiler (bronşiektazi akciğerlerin tümünü tutar).[9] Primer olgulardaki bronşiektaziler konjenitaldir; bronş oluşumunda doğumsal anomaliler vardır.[9] Kartagener sendromunda (bronşiektazi, sinüzit, situs inversus) ve Hareketsiz (immotil) Silia Sendromu bronşiektazi görülebilen konjenital nedenlerdir. Sekonder olgularda, “tütün dumanı” ve “hava kirliliği” en önemli faktörlerdir.[9][10][11][12][13] Daha az sıklıkla etkin olan risk faktörleri de görülebilir: Solunum sistemi infeksiyonları (kızamık, boğmaca, pnömoni), kistik fibrozis, bağışıklık sistemi yetmezlikleri.[9][10][11][12][13]
Patoloji: Tütün dumanından etkilenen bronş mukozasında aşırı mukus salgısının neden olduğu tıkanmalar (obstrüksiyon) gelişir. Tıkanan bronşlara ait akciğer segmenti büzüşebilir (atelektazi). Bronş epitelinde metaplazi ve siliaların silinmesi görülür. Mukus birikmelerine infeksiyon eklenebilir. Parçalanan bronş duvarları içleri irinli mukusla dolu geniş boşluklara dönüşür.[9] Alt loblarda sıktır. Bronşlardaki genişlemenin biçimine göre silindir, kese ya da mekik görünümünde boşluklar oluşur. Radyolojik incelemede ya da otopsilerde yapılan akciğer kesitlerinde kistik boşluklar izlenir.[9][10][11][12][13] Mikroskopla, bronş ve bronşiol duvarlarında yoğun akut ve/veya kronik yangısal hücre kümeleri vardır. Bazı bronşların epiteli nekrozlaşarak dökülmüştür (erozyon ya da ülser). Bronş çeperlerindeki nekroz alanlarında akciğer absesi gelişebilir. Yer yer skuamöz epitele metaplazi vardır. Kronikleşen olgularda bronş ve bronşiol duvarlarında yoğun nedbe dokusu oluşur (fibrozis).[9][10]

Komplikasyonlar:[9][10][11][12][13] Pnömoni ve empiyem; Sepsis ve septik şok; Meninjit ve beyin absesi; Cor pulmonale; Amiloidozis.
Emfizem (amfizem)[değiştir | kaynağı değiştir]
Emfizem, akciğer alveollerinin elastik yapılarını yitirmesi sonucu genişlemeleridir. Alvoel boşluklarını kuşatan duvarlardaki (septumlar) yırtılmalar sonucu kistik boşluklar oluşur. Klinik, radyoloji ve patoloji açısından sentriasiner, panasiner, paraseptal, irregular, büllöz ve senil gibi tiplere ayrılırlar.[9][10][11][12][13]
Çoğunlukla akciğerlerin üst loblarında ve tepe (apeks) kesimlerinde oluşurlar. Patoloji incelemelerinde, çevre bronş ve bronşiollerde yangı hücreleri (bronşit, bronşiolit) ile yoğun kömür pigmenti saptanır. Emfizemli alanların çevresinde bağ dokusu artışı ve büzüşmüş alveol gruplarına (atelektazi) rastlanır. Büllöz tipinde oluşan kistik boşluklar sıklıkla plevraya komşudur; ansızın patlamaları ani ölümlere neden olabilen pnömotoraksa yol açar; bu tip emfizemlerin bir bölümü geçirilmiş tüberküloz sekelidir. Senil emfizemler, akciğer alveollerinin yaşlanma nedeniyle elastik niteliklerini yitirmesinin sonucudur. Pnömotoraks ve pnömoni en önemli komplikasyonlarıdır. Konjenital emfizem olguları doğumsal alfa1-antitripsin eksikliğinin sonucudur; bu olgularda akciğerlerin alt loblarının daha yoğun biçimde etkilendiği saptanır.[9][10][11][12][13]
Astma bronşiale[değiştir | kaynağı değiştir]
Astma bronşiale (astım; bronşial astma), Küçük bronşların ve bronşiollerin, çeşitli uyaranlara aşırı tepki vermesinin sonucu ortaya çıkan, yangının da eşlik ettiği kronik bir tablodur.[9][10][11][12][13] Ayrıntılar için; Astım
Tanı[değiştir | kaynağı değiştir]

35 ila 40 yaş üzerinde, nefes darlığı çeken, kronik öksüren, balgam üreten, kışları sıkça soğuk algınlığına yakalanan, risk etmenleriyle bir geçmişi bulunan insanlarda KOAH aranabilir.[21][62] Spirometri tanıyı onaylamak için kullanılır.[21][63]
Spirometri[değiştir | kaynağı değiştir]
Spirometre, var olan hava akışı tıkanıklığını ölçer ve hava yolunu açmak adına bronkodilatör türevi ilaçların kullanımından sonra uygulanır.[63] Tanı yapmak için iki ölçüt vardır: bir saniye içinde zorlanan nefes verme hacmi (FEV1) ve tek bir nefeste verilen en büyük hava hacmini tanımlamak için kullanılan zorlanan nefes gücüdür (FVC).[64] Normal olarak, semptomları gösteren birinde FVC değerinin %75–80'i ilk saniyede ortaya çıkması[64] ve FEV1/FVC oranının %70'ten az çıkması bu kişinin KOAH hastası olduğunu kanıtlar.[63] Bu ölçümlerden yola çıkarak, spirometri yaşlı insanlarda KOAH için aşırı-tanıya yol açabilir.[63] National Institute for Health and Care Excellence kriterleri, bunların yanında tahmin edilenin %80'inden az bir FEV1 oranı da gerektirir. Spirometrinin KOAH semptomları göstermeyen bireylerde, tarama amacıyla kullanılmasının etkileri bilinmemektedir ve şimdilik önerilmemektedir.[21][63] Astım için sıkça kullanılan zirve akım hızı (maksimum solunum hızı), KOAH tanısı için yeterli değildir.[10][13]
Şiddet[değiştir | kaynağı değiştir]
| Derece | Etki eden aktivite |
|---|---|
| 1 | Ağır iş |
| 2 | Hareketli yürüyüş |
| 3 | Normal yürüyüş |
| 4 | Birkaç dakikalık yürüyüş |
| 5 | Kıyafet değiştirmek |
| Şiddet | FEV1 % tahmin edilen |
|---|---|
| Hafif (GOLD 1) | ≥80 |
| Orta (GOLD 2) | 50–79 |
| Şiddetli (GOLD 3) | 30–49 |
| Çok şiddetli (GOLD 4) | <30 or kronik solunum yetmezliği |
KOAH'ın belirli bir hastayı ne kadar eklediğini anlamak için çeşitli yöntemler mevcuttur.[21] Düzeltilmiş Britanya Tıp Araştırma Konseyi anketi (mMRC) veya KOAH değerlendirme testi (CAT) semptomların şiddetini belirlemek için yapılan basit anketlerdir.[21] 0 ile 40 arasında değişen CAT skalasında sayı arttıkça hastalığın şiddeti artar.[65] Spirometri hava akış sınırlamasını belirlemeye yardımcı olabilir.[21] Bu genel olarak, kişinin yaşı, cinsiyeti, boyu ve ağırlığına göre tahmin edilen "normal"e kıyasla FEV1 değerlerinin yüzdesi olarak belirtilir.[21] Hem Amerikan hem Avrupa ana esasları, tedavi için kısmi önerileri FEV1 üzerinden yapar.[63] GOLD esasları ise, insanları hava akışı sınırlamalarına göre dört kategoriye ayırmayı önerir.[21] Kilo kaybı, kas güçsüzlüğü ve diğer hastalıkların varlığı da hesaba katılmalıdır.[21]
Diğer testler[değiştir | kaynağı değiştir]
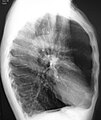
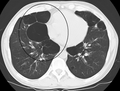
Göğüs radyografisi ve hemogram kullanımı, tanı sırasındaki diğer şartları hariç tutmak adına yapılabilir.[66] X ışını sonuçlarında genel olarak göze çarpan durumlar, olağandan büyük akciğerler, düzleşmiş diyafram, yükselen göğüs kemiği arkası hava boşluğu ve bül görülebilir. Bu sayede zatürre, pulmoner ödem veya pnömotoraks gibi durumlar hariç tutulabilir.[66] Göğüs için yapılan yüksek çözünürlüklü bir bilgisayarlı tomografi taraması akciğerlerdeki amfizemin bulunduğu yerleri teşhis etmekte kullanılır ve diğer hastalıkları hariç tutmak adına yararlıdır.[12] Yine de, ameliyat planlanmadığı sürece bu durum yönetim konusunda nadiren katkı sağlar.[12] Kan gazı analizi oksijen ihtiyacını belirlemek için kullanılır ve FEV1 değeri tahmin edilenin %35'inden az olan hastalara, çevresel oksijen doyumu %92'den az olanlara ve konjestif kalp yetmezliği belirtileri gösterenlere uygulanır.[21] Alfa-1 antitripsin eksikliğinin yoğun olduğu ülkelerde (özel olarak 45 yaş altı olan ve amfizemlerin akciğerin alt kısımlarında bulunduğu bireylerde) KOAH hastaları test edilmelidir.[21]
-
Göğüs röntgeninde açığa çıkan şiddetli KOAH. Akciğere oranla küçük kalan kalbe dikkat ediniz.
-
Amfizemli bir hastanın yandan röntgen görüntüsü. Fıçılaşmış göğsü ve düz diyaframa dikkat etiniz.
-
Şiddetli KOAH hastası birinin CXR görüntüsünde görülen uzun büller.
-
Şiddetli bir hastada büllü amfizem.
-
Son aşamasında büllü amfizemi olan hastanın eksenel CT görüntüsü.
Ayırıcı tanı[değiştir | kaynağı değiştir]
KOAH, nefes darlığına sebep olan diğer hastalıklardan ayırt edilmelidir. Bu hastalıklar arasında konjestif kalp yetmezliği, pulmoner damar tıkanıklığı, zatürre veya pnömotoraks yer alır. Birçok KOAH hastası astım olduğunu düşünür.[28] İkisi arasındaki ayrım, semptomlara göre yapılır. Buna göre tütün kullanım geçmişine, spirometride hava akışı sınırlanışının bronkodilatör kullanımıyla geri döndürülebilir olmasına bakılır.[67] Verem, kronik öksürme ile belirebildiği için, özellikle hastalığın görüldüğü yerlerde dikkate alınmalıdır.[21] Daha nadir de olsa, benzer etkiler gösteren bronkopulmoner displazi ve bronşiyolitis obliterans gibi hastalıklardan ayırt edilmelidir; kronik bronşit de normal hava akışı ile gerçekleşebilir ve bu durumda KOAH olarak sınıflandırılmaz.[12]
Önlem[değiştir | kaynağı değiştir]
KOAH'nın pek çok tipi potansiyel olarak dumana maruzu azaltarak ve hava kalitesini artırarak önlenebilmektedir.[41] Yıllık grip aşısı uygulaması sayesinde ataklar, hastaneye yatırılma ve ölüm gibi durumların olasılığı düşürülmektedir.[68][69] Pnömokok aşıları da yarar sağlayabilmektedir.[68]
Sigarayı bırakma[değiştir | kaynağı değiştir]
KOAH'nın önüne geçmenin en temel yolu insanların sigara alışkanlığı edinmesinin önüne geçmektir.[70] Hükûmetlerin, toplumsal sağlık kuruluşları ve sigara-karşıtı organizasyonların alacağı tedbirler sayesinde insanların sigaraya başlama ve sigarayı teşvik etme eğilimleri azaltılabilir.[71] Halka açık mekanlarda ve iş yerlerinde sigara yasağı uygulaması ile pasif içicilikten kaynaklanan sorunların önüne geçilebilir.[41]
Sigara kullanan kimselerde sigarayı bırakmak, KOAH'nın daha kötüleşmesinin önüne geçmek için yapılabilecek tek önlemdir.[72] Hastalığın son dönemlerinde dahi, bu uygulamayla akciğer işlevinin kötüleşme hızı azaltılabilir ve engellilik, ölüm gibi durumların geciktirilmesi sağlanabilir.[73] Sigarayı bırakmak, karar vermekle başlar. Uzun dönem bırakış genellikle birkaç deneme sonrasında başarıya ulaşır.[71] 5 yıldan fazla çaba gösteren insanların yaklaşık %40'ında başarı görülür.[74]
Bazı içiciler, sadece iradeyle uzun dönem sigarayı bırakabilirler. Ancak oldukça bağımlılık yapan bir etkinlik olduğundan,[75] sigarayı bırakmak isteyen kimselerin ek desteğe ihtiyaçları vardır. Sigarayı bırakma ihtimali, çevreden gelen destek, sigara bırakma programlarına katılım ve/veya nikotin replasman tedavisi, bupropiyon veya vareniklin gibi ilaçların kullanılmasıyla artırılabilir.[71][74]
Meslek sağlığı[değiştir | kaynağı değiştir]
Kömür madenciliği, inşaat işçiliği ve taş işçiliği gibi risk altındaki meslek gruplarının KOAH'a yakalanma oranını azaltmak adına bazı önlemler alınagelmiştir.[41] Bu önlemler arasında şöyle örnekler yer alır: kamu politikası üretimi,[41] işçilerin riskler konusunda eğitimi ve yönetimi, sigarayı bırakma konusunda destek, işçilerin erken KOAH belirtisi konusunda kontrol edilmesi, gaz maskesi kullanımı ve toz kontrolü.[76][77] Havalandırmayı geliştirmek, su spreyleri kullanmak ve toz üretimini düşüren madencilik tekniklerini uygulamak, etkili bir toz kontrolü sağlar.[78] Bir işçi KOAH'a yakalanırsa, işçinin iş rolünü değiştirmek gibi yollarla toza maruzu azaltılabilir ve hastalığın ciddileşmesinin önüne geçilebilir.[79] Hava kirliliği
Hem iç hem dış mekanlarda hava kalitesi yükseltilerek KOAH'ın önüne geçilebilir veya var olan hastalığın kötüleşmesinin önüne geçilebilir.[41] Bu durum, kamu politikası çabalarıyla ve kişisel dahiliyet ile başarılabilir.[80]
Bazı gelişmiş ülkeler, bazı düzenlemelere giderek dış mekanlarındaki hava kalitesini yükseltmiştir; bu sayede nüfuslarının KOAH geliştirme oranlarında olumlu değişimlere yol açmıştır.[41] KOAH hastası insanlar, dış mekandaki hava kalitesinin kötü olduğu durumlarda iç mekanlarda kalarak semptomlar gösterme ihtimallerini düşürebilirler.[14]
Bir diğer önlem, yemek pişirilen veya ısıtılan mekanlarda görülen yakıt dumanının, etkili havalandırma, hatta daha iyi soba ve bacalar kullanılarak azaltılmasıdır.[80] Düzgün sobala kullanımı, iç mekan hava kalitesini %85'e kadar iyileştirir. Güneş enerjisiyle yemek pişirme ve ısıtma gibi alternatif enerji kaynaklarının kullanımı, hatta biyokütle (tezek/odun) yerine kömür/gazyağı gibi yakıtların kullanımı, daha iyi sonuçlar doğurmaktadır.[41]
Beslenme[değiştir | kaynağı değiştir]
KOAH hastalarının öğün sayılarını arttırarak, gün içinde azar azar beslenmesi ventilasyon açısından oldukça önemlidir. Hastalar için belki de en önemli hususiyet Karbonhidrat tüketimini azaltmaları gerektiğidir. Zira Karbonhidrat asidik yapıda olduğundan halihazırda metabolik asidoz seviyesi kronikleşmiş olan hastada durumu daha da kötüleştirir. Bu sebepten Protein ağırlıklı beslenme tipi daha uygun olacaktır.
Yönetim[değiştir | kaynağı değiştir]
KOAH için bilinen bir tedavi bulunmamaktadır; ancak belirtiler tedavi edilebilir ve ilerlemesi ertelenebilir.[70] Yönetimin asıl amaçları arasında risk faktörlerini azaltmak, durağan bir hastalık süreci sağlamak, akut atakları önlemek veya iyileştirmek ve ilgili hastalıkları kontrol altında tutmak yer alır.[14] Hastalıktaki ölüm oranlarını azaltan yöntemlerden kanıtlanmış olanları sigarayı bırakma ve oksijen desteği almaktır.[81] Sigarayı bırakmak hastalıktan dolayı ölüm riskini %18'e kadar azaltır.[22] Diğer öneriler arasında her yıl grip aşısı olma, beş yılda bir zatürre aşısı olma ve çevredeki hava kirliliğine maruz kalma oranını azaltmak bulunur.[22] Hastalığı ilerlemiş olanlarda palyatif bakım belirtileri hafifletebilirken morfin nefes yetersizliği hissini azaltabilir.[82] Mekanik ventilasyon soluk almayı kolaylaştırmak adına kullanılabilir.[82]
Egzersiz[değiştir | kaynağı değiştir]
Pulmoner rehabilitasyon, bir egzersiz, hastalık yönetimi ve rehberlik programı olup kişinin yararı için koordine olur.[83] Yakın zamanda atak geçirenlerde, pulmoner rehabilitasyonun yaşam kalitesini, egzersiz yeteneğini arttırdığı ve ölüm riskini azalttığı görülmektedir.[84] Bunun yanında kişinin hastalığı üzerindeki ve kendi duyguları üzerindeki kontrol hissini arttırır.[85]
Optimal egzersiz rutini, egzersiz sırasında mekanik ventilasyon kullanımı ve KOAH hastaları için önerilen egzersiz yoğunluğu bilinmemektedir.[86][87] Kol dayanıklılığını arttıran egzersizler, KOAH hastalarının kol hareketini geliştirirken nefes darlığına da ufak katkılar sağlar.[88] Kol egzersizleri yapmak yaşam kalitesini arttırmak için tek başına yeterli değildir.[88] Nefes alıp verme egzersizlerinin de olumlu yararları sınırlıdır.[27] Büzük dudak nefesi egzersizleri yararlı olabilir.[27] Tai Chi egzersizleri KOAH hastaları için güvenli egzersizlerden olup sıradan tedavi programına nazaran daha solunum faaliyetleri ve kapasitesi için daha yararlı olabilir.[89] Tai Chi'nin diğer egzersiz programlarından daha etkili olduğuna dair herhangi bir çalışma yoktur.[89]
Normalden daha zayıf veya daha fazla kilolu olmak da belirtileri, engellilik seviyesi ve KOAH prognozunu etkileyebilir. Zayıf insanlar solunum kas gücünü kalori alımlarını arttırarak arttırabilirler.[14] Düzenli egzersiz veya pulmoner rehabilitasyon programları eşliğinde kalori alımı KOAH semptomlarını azalmada kayda değer katkılar sağlar. Yetersiz beslenen hastalarda ek besinler yararlıdır.[90]
Bronkodilatörler[değiştir | kaynağı değiştir]
Soluk yoluyla alınan bronkodilatörler kullanılan en birincil ilaçlardan olup[22] genel hastalığa küçük katkılar sağlarlar.[91] Bu tip ilaçların iki tipi bulunur: β2 agonistler ve antikolinerjikler. Her iki tip ilacın da uzun etkili ve kısa etkili biçimleri bulunur. Nefes darlığı, öksürme ve yetersiz egzersiz gibi olumsuzlukları azaltarak yaşam kalitesini arttırır.[92] Ancak altta yatan hastalığın gidişatında herhangi bir değişiklik yapıp yapmadıkları konusunda kesin bir çalışma yoktur.[22]
Hastalığı hafif olarak geçiren kimselerde, kısa etkili ilaçların ihtiyaç duyuldukça kullanılması önerilir.[22] Daha ciddi boyutlardaki hastalarda uzun etkili ilaçlar önerilir.[22] Uzun süreli ilaçlar kısmen hiperenflasyonu (aşırı havalanma) iyileştirme prensibiyle çalışır.[93] Uzun etkili bronkodilatörler yetersizse genelde tedaviye soluk yoluyla alınan kortikosteroidler eklenir.[22] Uzun etkili ilaçlara nazaran, tiotropiyum (uzun etkili antikolinerjik) ve uzun etkili beta-adrenoseptör agonistlerin (LABA'lar) daha iyi olup olmadıkları kesin değildir ve en uygun ilacın seçilmesi için hepsinin denenerek en iyi verim alınanının kullanılması önerilmektedir.[94] Her iki tip ilaç da akut atak riskini %15–25 aralığında azaltır.[22] İki tip aynı anda kullanılabilir fakat böylesi bir durumun kayda değer bir yarar sağlayıp sağlamadığı konusunda kesin bir çalışma yoktur.[94]
Salbutamol (Ventolin) ve terbütalin gibi bazı kısa etkili β2 agonistler mevcuttur.[95] BBunlar belirtileri dört ila altı saat arasında azaltırlar.[95] Salmeterol, formoterol ve indakaterol gibi uzun etkili β2 agonistleri bakım terapilerinde kullanılır. Bazıları bunun yararının sınırlı olduğunu öne sürerken,[96] diğerleri yeterli yarar sağladığını ileri sürer.[97][98][99] Uzun süreli kullanımlar KOAH hastaları için güvenli görünmektedir[100] fakat yan etkileri arasında istem-dışı titremeler ve kalp palpitasyon yer alır.[22] Soluk yoluyla alınan steroidlerle beraber alındığında zatürre riskini arttırırlar.[22] Steroidler ve LABA'lar beraber daha iyi sonuçlar verebilirken,[96] bu küçük katkıların artan sağlık risklerinden daha kayda değer olup olmadığı belirsizdir.[101] İndakaterol günde bir dozluk kullanım gerektirir ve günde iki kez kullanım gerektiren uzun etkili β2 agonistleri kadar etkilidir.[99]
KOAH ile mücadelede iki ana antikolinerjik kullanılır: ipratropyum ve tiotropyum. İpratropyum kısa etkili bir ajan olup tiotropyum uzun etkilidir. Tiotropyum atakları azaltarak yaşam kalitesini arttırır.[102] Bu katkıları tiotropyum, ipratropyuma göre daha verimli sağlar.[103] Bu maddeler ölüm riski veya hastanede tutulma süresinde kayda değer bir değişiklik vadetmez.[102] Antikolinerjikler ağız kuruluğu ve idrar yolu hastalıklarını arttırma eğilimi gösterebilirler.[22] Bunun yanında kalp hastalıkları ve kalp krizinde artışa yol açabilirler.[104][105] Bir diğer uzun etkili ajan olan aklidinyum, yaşam kalitesini arttırmasının yanı sıra hastanede tutulma oranlarını azaltır.[106][107][108] Aklinidinyum, tiotropyuma bir alternatif olarak geliştirildiyse de hangisinin daha etkili olduğu belirsizdir.[108]
Kortikosteroidler[değiştir | kaynağı değiştir]
Kortikosteroid ilaçlar solunum yoluyla alınsalar da akut atakların önüne geçmek adına tablet olarak da alınabilirler. Solunum yoluyla alınan kortikosteroidler (ICS) daha az ciddi KOAH hastaları için kayda değer faydalar sağlamazken, orta veya ciddi derecedeki hastaların akut ataklarını azaltır.[109] Tek başlarına bir-yıllık ölümlere bir katkıları yoktur.[81][110] Hastalığın gelişimi konusunda bir etkiye sahip olup olmadıkları kesin değildir.[22] LABA ile birlikte kullanıldıklarında, tek başında ICS veya tek başına LABA kullanımına nazaran ölüm oranlarını azaltabilirler.[111][112] Solunum yoluyla alınan steroidler, artan zatürre oranlarıyla ilişkilidir.[113] Uzun süreli steroid tabletleri kullanımının da kayda değer zararları bulunur.[95]
Diğer ilaçlar[değiştir | kaynağı değiştir]
Uzun süreli antibiyotikler, özellikle makrolid sınıfındaki eritromisin gibi ilaçlar, yılda bir veya daha fazla atak geçiren KOAH hastalarının ataklarının sıklığını azaltırlar.[114][115] Bu uygulama dünyanın bazı bölgelerinde uygun maliyet artısı getirir.[116] Bu uygulamayla ilgili endişeler arasında antibiyotik direnci ve azitromisin kaynaklı işitme sorunları yer alır.[115] Teofilin gibi metilksantinler yarardan çok zarar verdiklerinden ötürü önerilmezler,[117] ancak başka tedbirler altında tutulmayanlar tarafından ikinci basamak ajan olarak kullanılabilirler.[14] Mukolitikler kronik bronşit sahibi hastaların ataklarının azaltılmasına yardımcı olabilirler.[118] Öksürük ilaçları önerilmez.[95]
Oksijen[değiştir | kaynağı değiştir]
Ek oksijen tedavisi, dinlenme halinde düşük oksijen oranlarına (kan gazı basıncının 50–55 mmHg veya oksijen doygunluğunun %88'in altında olduğu durumlar) sahip olan kimseler için önerilir.[95][119] Bu gruptaki kimselerde günde 15 saat kullanılması durumunda kalp yetmezliği ve ölüm riskini azaltır[95][119] ve kişinin egzersiz yapma yeteneğini arttırır.[120] Oksijen seviyesi daha yüksek olan hastalarda egzersiz sırasında verilen oksijen katkısı kişinin nefes yetmezliğini arttırırken günlük aktivitelerindeki nefes yetmezliğine etki etmediği gibi hayat kalitesinde bir artışa sebep olmaz.[121] Yangın riski arttıran bu tedavi, kişinin sigaraya devam etmesi durumunda çok az bir katkı sağlar.[122] Böylesi durumlarda oksijen kullanımına karşı çıkan uzmanlar mevcuttur.[123] Akut ataklar sırasında birçok kişi oksijene ihtiyaç duyar; kişinin oksijen doygunluğu hesaba katılmadan yapılan oksijen terapileri kişinin kanında karbon dioksit oranlarının yükselmesine ve daha kötü sonuçlara neden olabilir.[124][125] Yüksek karbon dioksit riski taşıyanlarda %88–92'lık bir oksijen doygunluğu önerilirken, böyle bir risk taşımayanlarda %94–98 yeterlidir.[125]
Cerrahi[değiştir | kaynağı değiştir]
Çok ciddi boyutlardaki hastalarda cerrahi müdahale bazen yararlıdır ve akciğer nakli veya akciğer hacmi azaltma ameliyatı gibi uygulamaları içerir.[22] Akciğer nakli azaltma ameliyatında akciğerdeki en hasarlı kısımlar çıkarılarak kalan daha sağlıklı dokuların genişleyip daha iyi çalışması sağlanır.[95] Bu operasyon özellikle hastalık üst lopları etkilemişse başarılı olabilir. Ancak uygulama sonrası erken ölümler veya yan etkiler görülebilir.[126] Akciğer nakli bazı çok ciddi KOAH hastalarında, özellikle gençlerde uygulanır.[95]
Ataklar[değiştir | kaynağı değiştir]
Akut ataklar tipik olarak kısa etkiki bronkodilatörlerin kullanımının arttırılmasıyla tedavi edilir.[22] Bu, solunum yoluyla alınan kısa süreli agonistler ve antikolinerjiklerin beraber kullanılmasıyla yapılır.[50] Bu ilaçlar hava hazneli ölçülü inhalasyon aleti ile veya nebülizör (fısfıs) yardımıyla kullanılabilir olup her iki yöntem de eşit şekilde etkilidir.[50][127] Nebülizasyon, sağlık durumu daha kötü hastalar için kullanım kolaylığı sağlayabilir.[50] Oksijen eklemesi yararlı olabilir. Ancak aşırı oksijen, yükselen CO2 oranlarına ve bilinç azalmasına sebebiyet verebilir.[128]
Ağızdan alınan kortikosteroidler iyileşme şansını arttırabilir ve belirtilerin süresini kısaltabilir.[22][50] Damar içi steroidleri olarak da aynı verimde çalışsalar da, ağızdan alınanların daha az yan etkisi bulunur.[129] Beş günlük steroidler, on veya on dört günlük steroidler ile aynı verimde işe yarar.[130] Ciddi atakları olan hastalarda antibiyotikler de sonuçları daha iyiye çekebilir.[131] Amoksilin, doksisilin ve azitomisin gibi farklı antibiyotikler kullanılabilse de, hangisinin diğerlerine göre daha iyi sonuç verdiği kesin değildir.[68] FDA, barındırdığı ciddi yan etkilerden ötürü florokinolonların diğer antibiyotikler varken kullanılmamasını tembihler.[132] Bunun yanında daha az ciddi seviyedeki hastalar için kesin bir bulgu yoktur.[131]
Tip–2 solunum yetmezliği olanlarda (akut olarak CO2 oranı yüksek olanlar) mekanik ventilasyon ölüm riskini ve yoğun bakım girişlerini azaltır.[22] Ek olarak, teofilin diğer önlemlere cevap vermeyen hastalarda kullanılabilir.[22] Ataklardan %20'den daha azı hastanede yatış gerektirir.[50] Solunum yetmezliğinden dolayı asidoz (kandaki asit artışı) olmayan insanlarda ev bakımı hastane girişlerinin önüne geçebilir.[50]
Prognoz[değiştir | kaynağı değiştir]


| no data ≤110 110–220 220–330 330–440 440–550 550–660 | 660–770 770–880 880–990 990–1100 1100–1350 ≥1350 |
KOAH genelde zamanla daha da kötüleşir ve ölümle sonuçlanabilir. Tahminlere göre tüm işlev kayıplarının %3'ü KOAH ile ilgilidir.[134] KOAH'ya bağlı işlev kaybı oranı, özellikle Asya'da iyileşen hava kalitesi nedeniyle 1990'dan 2010'a düşüş gösterdi.[134] Buna karşın KOAH sebepli işlev kaybıyla yaşanan yıl sayısı arttı.[135]
KOAH hastalığının kötüleştiği oranlar solunum tıkanıklığı, egzersiz yapma yetisinde zayıflık, nefes yetersizliği, belirgin zayıflık ya da şişmanlık, kalp yetmezliği, sigara kullanımının devam etmesi ve sık ataklar gibi etmenlerle bağıntılıdır.[14] Hastalığın uzun süreli sonuçları, FEV1, vücut-kütle indeksi, altı dakikada yürünen mesafe ve değiştirilmiş MRC dispne skalası gibi testler üzerinden 0'dan 10'a kadar puanlama yapan BODE indeksi sayesinde önceden tahmin edilebilir.[136] Kayda değer kilo kayıpları kötüye işarettir.[12] Spirometri sonuçları da hastalığın gelecek gidişatını ön görmede iyi birer kaynak olsa da BODE indeksi kadar güvenilir değildir.[12][62]
Epidemiyoloji[değiştir | kaynağı değiştir]
Dünya çapında 2010 itibarıyla KOAH 329 milyon insanı (nüfusun %4,8'i) etkilemektedir.[135] Gelişmekte olan ülkelerde kadınlarda artan tütün kullanımı nedeniyle kadınlar ve erkekler hemen hemen eşit oranlarda bu hastalığa yakalanırlar.[137] Nüfusun arttığı ve aynı zamanda iyileşen bulaşıcı hastalık tedavileri yüzünden düşen ölüm oranları sayesinde nüfusun yaşlandığı gelişmekte olan ülkelerde 1970'ten 2000'lere kadar görülen KOAH artışının sebebi bu ülkelerde artan sigara kullanımıdır.[22] Ancak bazı gelişmekte olan ülkelerde KOAH oranı sabit kalırken, bazılarında düşüş görülmüştür.[22] Dünya çapında KOAH görülme oranlarında artış beklenmektedir, zira risk etmenleri halen yaygınlığını sürdürmekte ve nüfus giderek yaşlanmaktadır.[70]
1990 ve 2010 arasında KOAH nedeniyle ölüm sayısı 3,1 milyondan 2,9 milyona geriledi[138] ve en yaygın ölüm sebepleri sıralamasında dördüncü sıraya geriledi.[22] Ancak 2012 verilerinde sayının tekrar 3,1 milyon olması nedeniyle üçüncü sıraya tekrar tırmandı.[139] Bazı ülkelerde erkek KOAH ölümlerinde düşüş görülürken, kadınlarda artış gözlemlendi.[140] Bunun en birincil sebebi kadınların da sigara kullanımında erkeklere eşitlenmesidir.[12] Hastalık yaşlı insanlarda daha yaygındır;[8] 65 yaş üzeri 1000 insandan 34 ila 200'ü (incelenen topluma göre değişir) KOAH hastasıdır.[8][66]
İngiltere'de tahminen 0,84 milyon insana (50 milyonluk toplam nüfus) KOAH teşhisi konulmuştur; yani her 59 kişiden biri hayatlarının bir döneminde KOAH hastası olmuştur. Bu ülkenin sosyoekonomik olarak en yoksun bölgelerine bakılınca oran 32 insanda bire yükselirken, en zengin bölgelerde 98 insanda bire düşmektedir.[141] ABD'de yetişkin nüfusun %6,3'üne, yani yaklaşık 15 milyon insana KOAH teşhisi konulmuştur.[142] Teşhisi konulmamış kimselerle beraber bu sayının 25 milyonu bulabileceği tahmin edilmektedir.[143] 2011'de bu ülkede yaklaşık 730.000 insan KOAH nedeniyle hastaneye kaldırıldı.[144] ABD'de KOAH 2011 itibarıyla üçüncü en yaygın ölüm nedenidir.[145]
Tarih[değiştir | kaynağı değiştir]

"Amfizem" sözcüğü Yunanca kökenlidir. "Emfisan" Yunanca: ἐμφυσᾶν "şişmek" anlamına gelir -ἐν en "içeri" ve φυσᾶν fisan "nefes, esinti" anlamındadır.[146] Kronik bronşit terimi 1808'de kullanılmaya başladı[147] fakat terim olarak KOAH adının ilk kullanımının 1965'e dayandığına inanılmaktadır.[148] Daha öncesinde "kronik bronkopulmoner hastalık", "kronik obstrüktif solunum hastalığı", "kronik hava akışı tıkanması", "kronik hava akışı sınırlanımı", "kronik obstrüktif akciğer hastalığı", "spesifik olmayan kronik pulmoner hastalık" ve "yaygın obstrüktif pulmoner sendrom" gibi birçok farklı ismi bulunmaktaydı. Kronik bronşit ve amfizem terimleri resmi olarak 1959'da CIBA konuk sempozyumunda 1962'de Amerikan Toraks Topluluğu Komitesi'nin Tanı Standartları toplantısında tanımlandı.[148]
Amfizem hakkında muhtemel tanımlar arasında şunlar vardır: 1679'da T. Bonet'in "hacimli ciğerler" tanımı ve 1769'da Giovanni Morgagni'nin "özellikle havayla şişmiş" ciğerler tanımı.[148][149] 1721'de Ruysh tarafından ilk amfizem çizimleri yapıldı.[149] Bunları Matthew Baillie'nin 1789 resimleri ve durumun yıkıcı doğasının anlatıldığı tanımları izler. 1814'te Charles Badham "catarrh" sözcüğünü kronik bronşitteki aşırı mukus ve öksürme sesini tasvir etmek adına kullandı. Stetoskopun mucidi tıp adamı René Laennec, A Treatise on the Diseases of the Chest and of Mediate Auscultation (1837) adlı kitabında "amfizem"i otopsi için açtığında sönmeyen ciğerleri tanımlamakta kullandı. Notlarında bu ciğerlerin normalde olduğu gibi sönmediğini, çünkü havayla şişik olduğunu ve solunum yollarının mukusla kaplı olduğunu yazdı. 1842'de John Hutchinson, spirometreyi icat etti ve bu sayede nefes gücünün ölçümü mümkün kılındı. Ancak onun spirometresi hava akışını değil, sadece hacmi ölçüyordu. 1947'de Tiffeneau ve Pinelli hava akışının prensiplerini açıkladı.[148]
1953'te Amerikalı alerjist Dr. George L. Waldbott, Journal of the American Medical Association jurnalinde "sigara içicisi solunum sendromu" adında bir hastalığı tanımladı.[150]
İlk tedavi yolları arasında sarımsak, tarçın ve ipeka gibi bitkilerin kullanımları yer almaktaydı.[147] Modern tedaviler 20. yüzyılın ikinci yarısında geliştirildi. Steroidlerin KOAH ile mücadelede ilk kullanımlarının ipuçları 1950'ler sonunda yayımlanan makalelerde görülür. Bronkodilatörlerin kullanımı ise 1960'larda umut vadeden isoprenalinin kullanımıyla başladı. Daha sonraları salbutamol gibi diğer bronkodilatörler 1970'ler itibarıyla günlük yaşama girdi. LABA'ların kullanımı ise 1990'lar ortasını buldu.[151]
Toplum ve kültür[değiştir | kaynağı değiştir]
KOAH "sigara içicisi ciğeri" olarak anılır.[152] Amfizem sahibi insanlar pembe tenleri, hızlı solunum faaliyetleri ve büzüşmüş dudaklarıyla bilinirler (batıda pembe fısfıs veya A tipi lakabı).[153][154] Kronik bronşit sahibi insanlar ise oksijen yetersizliği nedeniyle maviye çalan deri ve dudakları, şişen bilekleriyle anılırlar (batıda mavi yağ tulumu veya B tipi lakabı).[154][155] Ancak böylesi tanımlar artık kabul görmemektedir zira KOAH hastası insanlar hem amfizem hem de kronik bronşit belirtilerini beraber gösterebilirler.[12][154]
Birçok sağlık sistemi hastalığı kimliklendirmede, tanıda ve tedavide zorluk çeker. Örneğin Britanya'daki Sağlık Departmanı bu durumu Ulusal Sağlık Servisi'nin büyük bir sorunu olduğunu belirmiştir ve bu sorunlarla savaşmak için özel stratejiler geliştirmiştir.[156]
Ekonomi[değiştir | kaynağı değiştir]
Dünya çapında 2010 itibarıyla KOAH hastalığının ekonomiye getirdiği zarar 2.1 trilyon dolar olarak tahmin edilmekte olup bu zararın yarısı gelişmekte olan ülkelere aittir.[20] Bu zararın 1.9 trilyonu tıbbi bakım gibi doğrudan harcamaları içerirken geriye kalan 0.2 trilyonu kayıp iş gücü gibi dolaylı kayıplardır.[157] Bunun 2030 itibarıyla iki katından daha fazla olacağı öngörülmektedir.[20] Avrupa'da KOAH sağlık harcamalarının %3'ünü oluşturur.[8] ABD'de hastalık çoğunluğu atak dönemlerinde olmak üzere 50 milyar dolarlık zarara yol açmaktadır.[8] 2011 yılında ABD hastanelerinde KOAH, 5,7 milyar dolarlık harcamayla ülkedeki en çok harcamalı hastalıklardan biri oldu.[144]
KOAH engel oranı[değiştir | kaynağı değiştir]
Doğuştan veya kazanılmış akciğer, plevra ve göğüs kafesi hastalıkları veya akciğeri tutan diğer bütün hastalıklarda, solunum ve dolaşım fonksiyonunda bozukluk yapmışsa; KOAH değerlendirmesi solunum fonksiyon testlerine göre değerlendirme yapılır;[158]
| Göğüs Hastalıkları (KOAH) | Oran |
| Az etkilenme varsa | %20 |
| Orta derecede etkilenme varsa | %40 |
| Ağır derecede etkilenme varsa veya kronik kor pulmonale gelişmişse | %80 |
Araştırma[değiştir | kaynağı değiştir]
Bağışıklık-baskılayan antikor Infliximab, KOAH için denendi fakat belirgin bir yararı olmadan zarar verme yatkınlığı barındırdığı görüldü.[159]
Roflumilast, cilomilast ve fosfodiesteraz-4 inhibitörü, hem bronkodilatör hem de antienflamatuvar özelliği gösterir. Atak oranlarını düşürmeye yönelik umut vadeden bu maddelerin yaşam kalitesinde bir iyileşmeye yol açacağı öngörülmemektedir.[22][160] Roflumilast ve cilomilast ise gastrointestinal sorunlar ile kilo kaybına yol açabilecek yan etkilere sahiptir. Roflumilastın buna ek olarak uyku sorunları ve duygu durumu rahatsızlıkları gibi yan etkileri de rapor edilmiştir.[160]
Bazı yeni uzun etkili ajanlar gelişim aşamasındadır.[22] Kök hücre ile tedaviler çalışma aşamasındadır.[161] Deneylerde bu çalışmaların güvenli olduğu, hayvan deneylerinden alınan verilerin umut vadedici olduğu belirtilse de 2017 itibarıyla çok az insan verisi bulunmaktadır.[162][163][164][165] Var olan insan verileri ise zayıf sonuçlar verdi.[162][166]
Hedef akciğer denervasyonu adı verilen ve akciğerlerin parasempatik sinir sistemi desteğini azaltmayı amaçlayan bir işlem, devam eden çalışmalar arasında olup kullanımı için yeterli veri bulunmamaktadır.[167] α1-antitripsin yetersizliği olan insanlarda bu maddenin destek olarak kullanılmasının getirileri üzerine yeterli ikna edici veriler yoktur.[168]
Telesağlık hizmetlerinin kullanımıyla ilgili çalışmalar devam etmektedir. Bu hizmetler ile nefes darlığı süreci geçiren KOAH hastalarının uzaktan tedavi edilmesi ve böylece hastanelerde acil bakım ünitelerinin rahatlatılarak insanların yaşam kalitesinin arttırılması amaçlanmaktadır.[169]
Hayvanlarda KOAH[değiştir | kaynağı değiştir]
Kronik obstrüktif akciğer hastalığı birçok diğer hayvanda da görülür ve özellikle tütün dumanına maruz kalmak sonucunda ortaya çıkar.[170][171] Ancak çoğu durumda hastalığın ciddiyeti ileri seviyede değildir.[172] Atlarda görülen yinelenen solunum yolu tıkanıklığı adlı sıkıntı oldukça ciddileşebilir. Bu hastalık kirlenmiş samanda bulunan bir mantar cinsine karşı alerjik tepkiden ötürü belirir.[173] KOAH yaşlı köpeklerde de sık görülür.[174]
Ayrıca bakınız[değiştir | kaynağı değiştir]
Konuyla ilgili yayınlar[değiştir | kaynağı değiştir]
- Vogelmeier, CF; Criner, GJ; Martinez, FJ; Anzueto, A; Barnes, PJ; Bourbeau, J; Celli, BR; Chen, R; Decramer, M; Fabbri, LM; Frith, P; Halpin, DM; Victorina López Varela, M; Nishimura, M; Roche, N; Rodriguez-Roisin, R; Sin, DD; Singh, D; Stockley, R; Vestbo, J; Wedzicha, JA; Agusti, A (2 Şubat 2017). "Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Lung Disease 2017 Report". Respirology (Carlton, Vic.). Cilt 22. ss. 575-601. doi:10.1111/resp.13012. PMID 28150362. (İngilizce)
- Qaseem, Amir; Wilt, TJ; Weinberger, SE; Hanania, NA; Criner, G; Van Der Molen, T; Marciniuk, DD; Denberg, T; Schünemann, H; Wedzicha, W; MacDonald, R; Shekelle, P; American College Of Physicians; American College of Chest Physicians; American Thoracic Society; European Respiratory Society (2011). "Diagnosis and Management of Stable Chronic Obstructive Pulmonary Disease: A Clinical Practice Guideline Update from the American College of Physicians, American College of Chest Physicians, American Thoracic Society, and European Respiratory Society". Annals of Internal Medicine. 155 (3). ss. 179-91. doi:10.7326/0003-4819-155-3-201108020-00008. PMID 21810710. 12 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.{{Ölü[ölü/kırık bağlantı] bağlantı|tarih=Nisan 2020 }} (İngilizce)
Kaynakça[değiştir | kaynağı değiştir]
- ^ a b c d "Chronic obstructive pulmonary disease". NICE. 9 Temmuz 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Temmuz 2021.
- ^ "Chronic obstructive pulmonary disease (COPD) - Complications | BMJ Best Practice". bestpractice.bmj.com. 11 Temmuz 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2021.
- ^ a b c "Chronic obstructive pulmonary disease (COPD)". Fact Sheets (İngilizce). World Health Organization. 18 Nisan 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 1 Temmuz 2021.
- ^ Gold Report 2021, ss. 20-27, Chapter 2: Diagnosis and initial assessment.
- ^ Gold Report 2021, ss. 33–35, Chapter 2: Diagnosis and initial assessment.
- ^ a b c Gold Report 2021, ss. 40–46, Chapter 3: Evidence supporting prevention and maintenance therapy.
- ^ GBD 2015 Disease and Injury Incidence and Prevalence Collaborators (October 2016). "Global, regional, and national incidence, prevalence, and years lived with disability for 310 diseases and injuries, 1990–2015: a systematic analysis for the Global Burden of Disease Study 2015". Lancet. 388 (10053). ss. 1545-1602. doi:10.1016/S0140-6736(16)31678-6. PMC 5055577 $2. PMID 27733282.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag Vestbo, Jørgen (2013). "Definition and Overview" (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Global Initiative for Chronic Obstructive Lung Disease. ss. 1-7.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai Kumar V, Abbas AK, Aster JC. Robbins and Cotran Pathologic Basis of Disease. 9th edt., Elsevier Saunders, Philadelphia, 2015
- ^ a b c d e f g h i j k l m n o p q r s t u v Reilly JJ, Silverman EK, Shapiro SD. Chronic Obstructive Pulmonary Disease. In Longo D, Fauci A, Kasper D, Hauser S, Jameson J, Loscalzo J (editors). Harrison's Principles of Internal Medicine (18th ed.) pp.2151–2159. McGraw Hill, New York-London-Totonto, 2011
- ^ a b c d e f g h i j k l m n o p q r Decramer M, Janssens W, Miravitlles M. Chronic obstructive pulmonary disease. Lancet, 379:(9823): 1341–1351, 2012
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af Reilly, John J.; Silverman, Edwin K.; Shapiro, Steven D. (2011). "Chronic Obstructive Pulmonary Disease". Longo, Dan; Fauci, Anthony; Kasper, Dennis; Hauser, Stephen; Jameson, J.; Loscalzo, Joseph (Ed.). Harrison's Principles of Internal Medicine (18. bas.). McGraw Hill. ss. 2151-9. ISBN 978-0-07-174889-6.
- ^ a b c d e f g h i j k l m Mason R, Broaddus VC, Martin T, et al. Murray and Nadel's Textbook of Respiratory Medicine, 5th Edition, Saunders, Philadelphia, 2010
- ^ a b c d e f g h i j k Rabe KF, Hurd S, Anzueto A, Barnes PJ, Buist SA, Calverley P, Fukuchi Y, Jenkins C, Rodriguez-Roisin R, van Weel C, Zielinski J (Eylül 2007). "Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease: GOLD executive summary". Am. J. Respir. Crit. Care Med. 176 (6). ss. 532-55. doi:10.1164/rccm.200703-456SO. PMID 17507545. 2 Ocak 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Nathell L, Nathell M, Malmberg P, Larsson K (2007). "COPD diagnosis related to different guidelines and spirometry techniques". Respir. Res. 8 (1). s. 89. doi:10.1186/1465-9921-8-89. PMC 2217523 $2. PMID 18053200.
- ^ Brulotte CA, Lang ES. Acute exacerbations of chronic obstructive pulmonary disease in the emergency department. Emergency Medicine Clinics of North America, 30(2): 223–247, 2012
- ^ a b "Chronic obstructive pulmonary disease (COPD) Fact sheet N°315". WHO. Ocak 2015. 15 Temmuz 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Mart 2016.
- ^ GBD 2013 Mortality and Causes of Death, Collaborators (17 Aralık 2014). "Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013". Lancet. Cilt 385. ss. 117-171. doi:10.1016/S0140-6736(14)61682-2. PMC 4340604 $2. PMID 25530442.
- ^ Mathers CD, Loncar D (Kasım 2006). "Projections of Global Mortality and Burden of Disease from 2002 to 2030". PLoS Med. 3 (11). ss. e442. doi:10.1371/journal.pmed.0030442. PMC 1664601 $2. PMID 17132052.[ölü/kırık bağlantı]
- ^ a b c Lomborg, Bjørn (2013). Global problems, local solutions : costs and benefits. Cambridge University Press. s. 143. ISBN 978-1-107-03959-9. 17 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 17 Temmuz 2017.
- ^ a b c d e f g h i j k l m n o p q r s t u Vestbo, Jørgen (2013). "Diagnosis and Assessment" (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Global Initiative for Chronic Obstructive Lung Disease. ss. 9-17.
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa Decramer M, Janssens W, Miravitlles M (Nisan 2012). "Chronic obstructive pulmonary disease". Lancet. 379 (9823). ss. 1341-51. doi:10.1016/S0140-6736(11)60968-9. PMID 22314182.
- ^ a b Mahler DA (2006). "Mechanisms and measurement of dyspnea in chronic obstructive pulmonary disease". Proceedings of the American Thoracic Society. 3 (3). ss. 234-8. doi:10.1513/pats.200509-103SF. PMID 16636091.
- ^ "What Are the Signs and Symptoms of COPD?". National Heart, Lung, and Blood Institute. 31 Temmuz 2013. 21 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Kasım 2013.
- ^ MedlinePlus Encyclopedia Chronic obstructive pulmonary disease
- ^ Morrison, [edited by] Nathan E. Goldstein, R. Sean (2013). Evidence-based practice of palliative medicine. Philadelphia: Elsevier/Saunders. s. 124. ISBN 978-1-4377-3796-7. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b c Holland AE, Hill CJ, Jones AY, McDonald CF (2012). Holland, Anne E (Ed.). "Breathing exercises for chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 10. ss. CD008250. doi:10.1002/14651858.CD008250.pub2. PMID 23076942.
- ^ a b c d e f Gruber, Phillip (Kasım 2008). "The Acute Presentation of Chronic Obstructive Pulmonary Disease In the Emergency Department: A Challenging Oxymoron". Emergency Medicine Practice. 10 (11). 5 Ekim 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b Weitzenblum E, Chaouat A (2009). "Cor pulmonale". Chron Respir Dis. 6 (3). ss. 177-85. doi:10.1177/1479972309104664. PMID 19643833.
- ^ "Cor pulmonale". Professional guide to diseases (9. bas.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. 2009. ss. 120-2. ISBN 978-0-7817-7899-2.
- ^ Mandell, editors, James K. Stoller, Franklin A. Michota, Jr., Brian F. (2009). The Cleveland Clinic Foundation intensive review of internal medicine (5. bas.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. s. 419. ISBN 978-0-7817-9079-6. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Brulotte CA, Lang ES (Mayıs 2012). "Acute exacerbations of chronic obstructive pulmonary disease in the emergency department". Emerg. Med. Clin. North Am. 30 (2). ss. 223-47, vii. doi:10.1016/j.emc.2011.10.005. PMID 22487106.
- ^ Spiro, Stephen (2012). Clinical respiratory medicine expert consult (4. bas.). Philadelphia, PA: Saunders. ISBN 978-1-4557-2329-4. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ World Health Organization (2008). WHO Report on the Global Tobacco Epidemic 2008: The MPOWER Package (PDF). Cenevre: World Health Organization. ss. 268-309. ISBN 92-4-159628-7. 24 Ocak 2018 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 2 Mart 2015.
- ^ a b Ward, Helen (2012). Oxford Handbook of Epidemiology for Clinicians. Oxford University Press. ss. 289-290. ISBN 978-0-19-165478-7. 10 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Laniado-Laborín, R (Ocak 2009). "Smoking and chronic obstructive pulmonary disease (COPD). Parallel epidemics of the 21st century". International journal of environmental research and public health. 6 (1). ss. 209-24. doi:10.3390/ijerph6010209. PMC 2672326 $2. PMID 19440278.
- ^ a b Rennard, Stephen (2013). Clinical management of chronic obstructive pulmonary disease (2. bas.). New York: Informa Healthcare. s. 23. ISBN 978-0-8493-7588-0. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b Anita Sharma ; with a contribution by David Pitchforth ; forewords by Gail Richards; Barclay, Joyce (2010). COPD in primary care. Oxford: Radcliffe Pub. s. 9. ISBN 978-1-84619-316-3. 29 Eylül 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Goldman, Lee (2012). Goldman's Cecil medicine (24. bas.). Philadelphia: Elsevier/Saunders. s. 537. ISBN 978-1-4377-1604-7. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b Kennedy SM, Chambers R, Du W, Dimich-Ward H (Aralık 2007). "Environmental and occupational exposures: do they affect chronic obstructive pulmonary disease differently in women and men?". Proceedings of the American Thoracic Society. 4 (8). ss. 692-4. doi:10.1513/pats.200707-094SD. PMID 18073405. 8 Aralık 2011 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b c d e f g h i j k l m Pirozzi C, Scholand MB (Temmuz 2012). "Smoking cessation and environmental hygiene". Med. Clin. North Am. 96 (4). ss. 849-67. doi:10.1016/j.mcna.2012.04.014. PMID 22793948.
- ^ Halbert RJ, Natoli JL, Gano A, Badamgarav E, Buist AS, Mannino DM (Eylül 2006). "Global burden of COPD: systematic review and meta-analysis". Eur. Respir. J. 28 (3). ss. 523-32. doi:10.1183/09031936.06.00124605. PMID 16611654.
- ^ a b Devereux, Graham (2006). "Definition, epidemiology and risk factors". BMJ. 332 (7550). ss. 1142-4. doi:10.1136/bmj.332.7550.1142. PMC 1459603 $2. PMID 16690673.
- ^ a b ILO. List of Occoational Diseases. Identification and recognition of occupational diseases: Criteria for incorporating diseases in the ILO list of occupational diseases, Occupational Safety and Health Series, No. 74, International Labour Organization, Geneva, 2010
- ^ Laine, Christine (2009). In the Clinic: Practical Information about Common Health Problems. ACP Press. s. 226. ISBN 978-1-934465-64-6. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b Barnes, Peter J.; Drazen, Jeffrey M.; Rennard, Stephen I.; Thomson, Neil C., (Ed.) (2009). "Relationship between cigarette smoking and occupational exposures". Asthma and COPD: Basic Mechanisms and Clinical Management. Amsterdam: Academic. s. 464. ISBN 978-0-12-374001-4.
- ^ Rushton, Lesley (2007). "Chronic Obstructive Pulmonary Disease and Occupational Exposure to Silica". Reviews on Environmental Health. 22 (4). ss. 255-72. doi:10.1515/REVEH.2007.22.4.255. PMID 18351226.
- ^ a b c d Foreman MG, Campos M, Celedón JC (Temmuz 2012). "Genes and chronic obstructive pulmonary disease". Med. Clin. North Am. 96 (4). ss. 699-711. doi:10.1016/j.mcna.2012.02.006. PMC 3399759 $2. PMID 22793939.
- ^ Brode SK, Ling SC, Chapman KR (Eylül 2012). "Alpha-1 antitrypsin deficiency: a commonly overlooked cause of lung disease". CMAJ. 184 (12). ss. 1365-71. doi:10.1503/cmaj.111749. PMC 3447047 $2. PMID 22761482.
- ^ a b c d e f g Vestbo, Jørgen (2013). "Management of Exacerbations" (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Global Initiative for Chronic Obstructive Lung Disease. ss. 39-45.
- ^ a b c Dhar, Raja (2011). Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. s. 1056. ISBN 978-93-5025-073-0. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Palange, Paolo (2013). ERS Handbook of Respiratory Medicine. European Respiratory Society. s. 194. ISBN 978-1-84984-041-5. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Lötvall, Jan (2011). Advances in combination therapy for asthma and COPD. Chichester, West Sussex: John Wiley & Sons. s. 251. ISBN 978-1-119-97846-6. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Barnes, Peter (2009). Asthma and COPD : basic mechanisms and clinical management (2. bas.). Amsterdam: Academic. s. 837. ISBN 978-0-12-374001-4. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Hanania, Nicola (9 Aralık 2010). COPD a Guide to Diagnosis and Clinical Management (1. bas.). Totowa, NJ: Springer Science+Business Media, LLC. s. 197. ISBN 978-1-59745-357-8. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b Beasley, V; Joshi, PV; Singanayagam, A; Molyneaux, PL; Johnston, SL; Mallia, P (2012). "Lung microbiology and exacerbations in COPD". International journal of chronic obstructive pulmonary disease. Cilt 7. ss. 555-69. doi:10.2147/COPD.S28286. PMC 3437812 $2. PMID 22969296.
- ^ Murphy DMF, Fishman AP (2008). "Chapter 53". Fishman's Pulmonary Diseases and Disorders (4. bas.). McGraw-Hill. s. 913. ISBN 0-07-145739-9.
- ^ a b Calverley PM, Koulouris NG (2005). "Flow limitation and dynamic hyperinflation: key concepts in modern respiratory physiology". Eur Respir J. 25 (1). ss. 186-199. doi:10.1183/09031936.04.00113204. PMID 15640341.
- ^ Currie, Graeme P. (2010). ABC of COPD (2. bas.). Chichester, West Sussex, UK: Wiley-Blackwell, BMJ Books. s. 32. ISBN 978-1-4443-2948-3. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ O'Donnell DE (2006). "Hyperinflation, Dyspnea, and Exercise Intolerance in Chronic Obstructive Pulmonary Disease". The Proceedings of the American Thoracic Society. 3 (2). ss. 180-4. doi:10.1513/pats.200508-093DO. PMID 16565429.
- ^ Weitzenblum E, Chaouat A. Cor pulmonale. Chronic Respiratory Disease. 6(3):177–185, 2009
- ^ a b c Şablon:NICE
- ^ a b c d e f Qaseem, Amir; Wilt, TJ; Weinberger, SE; Hanania, NA; Criner, G; Van Der Molen, T; Marciniuk, DD; Denberg, T; Schünemann, H; Wedzicha, W; MacDonald, R; Shekelle, P; American College Of Physicians; American College of Chest Physicians; American Thoracic Society; European Respiratory Society (2011). "Diagnosis and Management of Stable Chronic Obstructive Pulmonary Disease: A Clinical Practice Guideline Update from the American College of Physicians, American College of Chest Physicians, American Thoracic Society, and European Respiratory Society". Annals of Internal Medicine. 155 (3). ss. 179-91. doi:10.7326/0003-4819-155-3-201108020-00008. PMID 21810710. 12 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b Young, Vincent B. (2010). Blueprints medicine (5. bas.). Philadelphia: Wolters Kluwer Health/Lippincott William & Wilkins. s. 69. ISBN 978-0-7817-8870-0. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ "COPD Assessment Test (CAT)". American Thoracic Society. 19 Ocak 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Kasım 2013.
- ^ a b c Torres M, Moayedi S (Mayıs 2007). "Evaluation of the acutely dyspneic elderly patient". Clin. Geriatr. Med. 23 (2). ss. 307-25, vi. doi:10.1016/j.cger.2007.01.007. PMID 17462519.
- ^ BTS COPD Consortium (2005). "Spirometry in practice - a practical guide to using spirometry in primary care". ss. 8-9. 13 Nisan 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Ağustos 2014.
- ^ a b c Mackay AJ, Hurst JR (Temmuz 2012). "COPD exacerbations: causes, prevention, and treatment". Med. Clin. North Am. 96 (4). ss. 789-809. doi:10.1016/j.mcna.2012.02.008. PMID 22793945.
- ^ Poole PJ, Chacko E, Wood-Baker RW, Cates CJ (2006). Poole, Phillippa (Ed.). "Influenza vaccine for patients with chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 1. ss. CD002733. doi:10.1002/14651858.CD002733.pub2. PMID 16437444.
- ^ a b c Vestbo, Jørgen (2013). "Introduction". Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease (PDF). Global Initiative for Chronic Obstructive Lung Disease. xiii-xv. 4 Ekim 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b c Policy Recommendations for Smoking Cessation and Treatment of Tobacco Dependence. World Health Organization. ss. 15-40. ISBN 978-92-4-156240-9. 15 Eylül 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Jiménez-Ruiz CA, Fagerström KO (Mart 2013). "Smoking cessation treatment for COPD smokers: the role of counselling". Monaldi Arch Chest Dis. 79 (1). ss. 33-7. PMID 23741944.
- ^ Kumar P, Clark M (2005). Clinical Medicine (6. bas.). Elsevier Saunders. ss. 900-1. ISBN 0-7020-2763-4.
- ^ a b Tønnesen P (Mart 2013). "Smoking cessation and COPD". Eur Respir Rev. 22 (127). ss. 37-43. doi:10.1183/09059180.00007212. PMID 23457163.
- ^ "Why is smoking addictive?". NHS Choices. 29 Aralık 2011. 2 Kasım 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Kasım 2013.
- ^ Smith, Barbara K. Timby, Nancy E. (2005). Essentials of nursing : care of adults and children. Philadelphia: Lippincott Williams & Wilkins. s. 338. ISBN 978-0-7817-5098-1. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Rom, William N.; Markowitz, Steven B., (Ed.) (2007). Environmental and occupational medicine (4. bas.). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. ss. 521-2. ISBN 978-0-7817-6299-1. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ "Wet cutting". Health and Safety Executive. 25 Eylül 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Kasım 2013.
- ^ George, Ronald B. (2005). Chest medicine : essentials of pulmonary and critical care medicine (5. bas.). Philadelphia, PA: Lippincott Williams & Wilkins. s. 172. ISBN 978-0-7817-5273-2. 6 Ekim 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b Vestbo, Jørgen (2013). "Management of Stable COPD". Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease (PDF). Global Initiative for Chronic Obstructive Lung Disease. ss. 31-8. 4 Ekim 2013 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ a b Drummond MB, Dasenbrook EC, Pitz MW, Murphy DJ, Fan E (Kasım 2008). "Inhaled corticosteroids in patients with stable chronic obstructive pulmonary disease: a systematic review and meta-analysis". JAMA. 300 (20). ss. 2407-16. doi:10.1001/jama.2008.717. PMID 19033591.
- ^ a b Carlucci A, Guerrieri A, Nava S (Aralık 2012). "Palliative care in COPD patients: is it only an end-of-life issue?". Eur Respir Rev. 21 (126). ss. 347-54. doi:10.1183/09059180.00001512. PMID 23204123.
- ^ "COPD — Treatment". U.S. National Heart Lung and Blood Institute. 27 Nisan 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Temmuz 2013.
- ^ Puhan MA, Gimeno-Santos E, Scharplatz M, Troosters T, Walters EH, Steurer J (2011). Puhan, Milo A (Ed.). "Pulmonary rehabilitation following exacerbations of chronic obstructive pulmonary disease". Cochrane Database Syst Rev, 10. ss. CD005305. doi:10.1002/14651858.CD005305.pub3. PMID 21975749.
- ^ Lacasse Y, Goldstein R, Lasserson TJ, Martin S (2006). Lacasse, Yves (Ed.). "Pulmonary rehabilitation for chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 4. ss. CD003793. doi:10.1002/14651858.CD003793.pub2. PMID 17054186.
- ^ McNamara, Renae J.; McKeough, Zoe J.; McKenzie, David K.; Alison, Jennifer A. (18 Aralık 2013). "Water-based exercise training for chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews, 12. ss. CD008290. doi:10.1002/14651858.CD008290.pub2. ISSN 1469-493X. PMID 24353107.
- ^ Menadue, Collette; Piper, Amanda J.; van 't Hul, Alex J.; Wong, Keith K. (14 Mayıs 2014). "Non-invasive ventilation during exercise training for people with chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews, 5. ss. CD007714. doi:10.1002/14651858.CD007714.pub2. ISSN 1469-493X. PMID 24823712.
- ^ a b McKeough, Zoe J.; Velloso, Marcelo; Lima, Vanessa P.; Alison, Jennifer A. (15 Kasım 2016). "Upper limb exercise training for COPD". The Cochrane Database of Systematic Reviews. Cilt 11. ss. CD011434. doi:10.1002/14651858.CD011434.pub2. ISSN 1469-493X. PMID 27846347.
- ^ a b Ngai, Shirley P. C.; Jones, Alice Y. M.; Tam, Wilson Wai San (7 Haziran 2016). "Tai Chi for chronic obstructive pulmonary disease (COPD)". The Cochrane Database of Systematic Reviews, 6. ss. CD009953. doi:10.1002/14651858.CD009953.pub2. ISSN 1469-493X. PMID 27272131.
- ^ Ferreira IM, Brooks D, White J, Goldstein R (2012). Ferreira, Ivone M (Ed.). "Nutritional supplementation for stable chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 12. ss. CD000998. doi:10.1002/14651858.CD000998.pub3. PMID 23235577.
- ^ van Dijk WD, van den Bemt L, van Weel C (2013). "Megatrials for bronchodilators in chronic obstructive pulmonary disease (COPD) treatment: time to reflect". J Am Board Fam Med. 26 (2). ss. 221-4. doi:10.3122/jabfm.2013.02.110342. PMID 23471939.
- ^ Liesker JJ, Wijkstra PJ, Ten Hacken NH, Koëter GH, Postma DS, Kerstjens HA (Şubat 2002). "A systematic review of the effects of bronchodilators on exercise capacity in patients with COPD". Chest. 121 (2). ss. 597-608. doi:10.1378/chest.121.2.597. PMID 11834677. 28 Eylül 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Cooper, CB (Ekim 2006). "The connection between chronic obstructive pulmonary disease symptoms and hyperinflation and its impact on exercise and function". The American Journal of Medicine. 119 (10 Suppl 1). ss. 21-31. doi:10.1016/j.amjmed.2006.08.004. PMID 16996896.
- ^ a b Farne, Hugo A.; Cates, Christopher J. (22 Ekim 2015). "Long-acting beta2-agonist in addition to tiotropium versus either tiotropium or long-acting beta2-agonist alone for chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews, 10. ss. CD008989. doi:10.1002/14651858.CD008989.pub3. ISSN 1469-493X. PMID 26490945.
- ^ a b c d e f g h Vestbo, Jørgen (2013). "Therapeutic Options" (PDF). Global Strategy for the Diagnosis, Management, and Prevention of Chronic Obstructive Pulmonary Disease. Global Initiative for Chronic Obstructive Lung Disease. ss. 19-30.[ölü/kırık bağlantı]
- ^ a b Cave, AC.; Hurst, MM. (Mayıs 2011). "The use of long acting β₂-agonists, alone or in combination with inhaled corticosteroids, in chronic obstructive pulmonary disease (COPD): a risk-benefit analysis". Pharmacol Ther. 130 (2). ss. 114-43. doi:10.1016/j.pharmthera.2010.12.008. PMID 21276815.
- ^ Spencer, S; Karner, C; Cates, CJ; Evans, DJ (7 Aralık 2011). Spencer, Sally (Ed.). "Inhaled corticosteroids versus long-acting beta(2)-agonists for chronic obstructive pulmonary disease". Cochrane Database Syst Rev, 12. ss. CD007033. doi:10.1002/14651858.CD007033.pub3. PMID 22161409.
- ^ Wang, J; Nie, B; Xiong, W; Xu, Y (Nisan 2012). "Effect of long-acting beta-agonists on the frequency of COPD exacerbations: a meta-analysis". Journal of clinical pharmacy and therapeutics. 37 (2). ss. 204-11. doi:10.1111/j.1365-2710.2011.01285.x. PMID 21740451.
- ^ a b Geake, James B.; Dabscheck, Eli J.; Wood-Baker, Richard; Cates, Christopher J. (10 Ocak 2015). "Indacaterol, a once-daily beta2-agonist, versus twice-daily beta₂-agonists or placebo for chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews. Cilt 1. ss. CD010139. doi:10.1002/14651858.CD010139.pub2. ISSN 1469-493X. PMID 25575340.
- ^ Decramer ML, Hanania NA, Lötvall JO, Yawn BP (2013). "The safety of long-acting β2-agonists in the treatment of stable chronic obstructive pulmonary disease". Int J Chron Obstruct Pulmon Dis. Cilt 8. ss. 53-64. doi:10.2147/COPD.S39018. PMC 3558319 $2. PMID 23378756.
- ^ Nannini, LJ; Lasserson, TJ; Poole, P (12 Eylül 2012). Nannini, Luis Javier (Ed.). "Combined corticosteroid and long-acting beta(2)-agonist in one inhaler versus long-acting beta(2)-agonists for chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 9. ss. CD006829. doi:10.1002/14651858.CD006829.pub2. PMC 4170910 $2. PMID 22972099.
- ^ a b Karner, Charlotta; Chong, Jimmy; Poole, Phillippa (21 Temmuz 2014). "Tiotropium versus placebo for chronic obstructive pulmonary disease1". The Cochrane Database of Systematic Reviews, 7. ss. CD009285. doi:10.1002/14651858.CD009285.pub3. ISSN 1469-493X. PMID 25046211.
- ^ Cheyne, Leanne; Irvin-Sellers, Melanie J.; White, John (22 Eylül 2015). "Tiotropium versus ipratropium bromide for chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews, 9. ss. CD009552. doi:10.1002/14651858.CD009552.pub3. ISSN 1469-493X. PMID 26391969.
- ^ Singh S, Loke YK, Furberg CD (Eylül 2008). "Inhaled anticholinergics and risk of major adverse cardiovascular events in patients with chronic obstructive pulmonary disease: a systematic review and meta-analysis". JAMA. 300 (12). ss. 1439-50. doi:10.1001/jama.300.12.1439. PMID 18812535.
- ^ Singh S, Loke YK, Enright P, Furberg CD (Ocak 2013). "Pro-arrhythmic and pro-ischaemic effects of inhaled anticholinergic medications". Thorax. 68 (1). ss. 114-6. doi:10.1136/thoraxjnl-2011-201275. PMID 22764216.
- ^ Jones, P (Apr 2013). "Aclidinium bromide twice daily for the treatment of chronic obstructive pulmonary disease: a review". Advances in therapy. 30 (4). ss. 354-68. doi:10.1007/s12325-013-0019-2. PMID 23553509.
- ^ Cazzola, M; Page, CP; Matera, MG (Jun 2013). "Aclidinium bromide for the treatment of chronic obstructive pulmonary disease". Expert opinion on pharmacotherapy. 14 (9). ss. 1205-14. doi:10.1517/14656566.2013.789021. PMID 23566013.
- ^ a b Ni, Han; Soe, Zay; Moe, Soe (19 Eylül 2014). "Aclidinium bromide for stable chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews. Cilt 9. ss. CD010509. doi:10.1002/14651858.CD010509.pub2. ISSN 1469-493X. PMID 25234126.
- ^ Gartlehner G, Hansen RA, Carson SS, Lohr KN (2006). "Efficacy and Safety of Inhaled Corticosteroids in Patients With COPD: A Systematic Review and Meta-Analysis of Health Outcomes". Ann Fam Med. 4 (3). ss. 253-62. doi:10.1370/afm.517. PMC 1479432 $2. PMID 16735528.
- ^ Chinet, T; Dumoulin, J; Honore, I; Braun, JM; Couderc, LJ; Febvre, M; Mangiapan, G; Maurer, C; Serrier, P; Soyez, F; Terrioux, P; Jebrak, G (29 Ocak 2016). "[The place of inhaled corticosteroids in COPD]". Revue des maladies respiratoires. doi:10.1016/j.rmr.2015.11.009. PMID 26831345.
- ^ Dong, YH; Lin, HH; Shau, WY; Wu, YC; Chang, CH; Lai, MS (Ocak 2013). "Comparative safety of inhaled medications in patients with chronic obstructive pulmonary disease: systematic review and mixed treatment comparison meta-analysis of randomised controlled trials". Thorax. 68 (1). ss. 48-56. doi:10.1136/thoraxjnl-2012-201926. PMID 23042705.
- ^ Nannini, LJ; Poole, P; Milan, SJ; Kesterton, A (30 Ağustos 2013). "Combined corticosteroid and long-acting beta(2)-agonist in one inhaler versus inhaled corticosteroids alone for chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 8. ss. CD006826. doi:10.1002/14651858.CD006826.pub2. PMID 23990350.
- ^ Kew, KM; Seniukovich, A (10 Mart 2014). "Inhaled steroids and risk of pneumonia for chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 3. ss. CD010115. doi:10.1002/14651858.CD010115.pub2. PMID 24615270.
- ^ Mammen MJ, Sethi S (2012). "Macrolide therapy for the prevention of acute exacerbations in chronic obstructive pulmonary disease". Pol. Arch. Med. Wewn. 122 (1–2). ss. 54-9. PMID 22353707.
- ^ a b Herath, SC; Poole, P (28 Kasım 2013). "Prophylactic antibiotic therapy for chronic obstructive pulmonary disease (COPD)". Cochrane Database Syst Rev. Cilt 11. ss. CD009764. doi:10.1002/14651858.CD009764.pub2. PMID 24288145.
- ^ Simoens, S; Laekeman, G; Decramer, M (Mayıs 2013). "Preventing COPD exacerbations with macrolides: a review and budget impact analysis". Respiratory medicine. 107 (5). ss. 637-48. doi:10.1016/j.rmed.2012.12.019. PMID 23352223.
- ^ Barr RG, Rowe BH, Camargo CA (2003). Barr, R Graham (Ed.). "Methylxanthines for exacerbations of chronic obstructive pulmonary disease". Cochrane Database Syst Rev, 2. ss. CD002168. doi:10.1002/14651858.CD002168. PMID 12804425.
- ^ Poole, P; Chong, J; Cates, CJ (29 Temmuz 2015). "Mucolytic agents versus placebo for chronic bronchitis or chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 7. ss. CD001287. doi:10.1002/14651858.CD001287.pub5. PMID 26222376.
- ^ a b COPD Working, Group (2012). "Long-term oxygen therapy for patients with chronic obstructive pulmonary disease (COPD): an evidence-based analysis". Ontario health technology assessment series. 12 (7). ss. 1-64. PMC 3384376 $2. PMID 23074435.
- ^ Bradley JM, O'Neill B (2005). Bradley, Judy M (Ed.). "Short-term ambulatory oxygen for chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 4. ss. CD004356. doi:10.1002/14651858.CD004356.pub3. PMID 16235359.
- ^ Ekström, Magnus; Ahmadi, Zainab; Bornefalk-Hermansson, Anna; Abernethy, Amy; Currow, David (25 Kasım 2016). "Oxygen for breathlessness in patients with chronic obstructive pulmonary disease who do not qualify for home oxygen therapy". The Cochrane Database of Systematic Reviews. Cilt 11. ss. CD006429. doi:10.1002/14651858.CD006429.pub3. ISSN 1469-493X. PMID 27886372.
- ^ Chapman, Stephen (2009). Oxford handbook of respiratory medicine (2. bas.). Oxford University Press. s. 707. ISBN 978-0-19-954516-2. 18 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ Blackler, Laura (2007). Managing chronic obstructive pulmonary disease. Wiley. s. 49. ISBN 978-0-470-51798-7. 18 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ Jindal, Surinder K (2013). Chronic Obstructive Pulmonary Disease. Jaypee Brothers Medical. s. 139. ISBN 978-93-5090-353-7. 17 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ a b O'Driscoll, BR; Howard, LS; Davison, AG; British Thoracic, Society (Ekim 2008). "BTS guideline for emergency oxygen use in adult patients". Thorax. 63 (Suppl 6). ss. vi1-68. doi:10.1136/thx.2008.102947. PMID 18838559.
- ^ van Agteren, JE; Carson, KV; Tiong, LU; Smith, BJ (14 Ekim 2016). "Lung volume reduction surgery for diffuse emphysema". The Cochrane database of systematic reviews. Cilt 10. ss. CD001001. doi:10.1002/14651858.CD001001.pub3. PMID 27739074.
- ^ "Bronchodilators delivered by nebuliser versus inhalers for lung attacks of chronic obstructive pulmonary disease". Cochrane Database of Systematic Reviews. 29 Ağustos 2016. doi:10.1002/14651858.cd011826. 13 Eylül 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ Wise, Robert. "Chronic Obstructive Pulmonary Disease (COPD) - Pulmonary Disorders - Merck Manuals Professional Edition". Merck Manuals Professional Edition. 21 Haziran 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Aralık 2016.
- ^ Walters, JA; Tan, DJ; White, CJ; Gibson, PG; Wood-Baker, R; Walters, EH (Eylül 2014). "Systemic corticosteroids for acute exacerbations of chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 9. ss. CD001288. doi:10.1002/14651858.CD001288.pub4. PMID 25178099. 24 Eylül 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Walters, JA; Tan, DJ; White, CJ; Wood-Baker, R (10 Aralık 2014). "Different durations of corticosteroid therapy for exacerbations of chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 12. ss. CD006897. doi:10.1002/14651858.CD006897.pub3. PMID 25491891.
- ^ a b Vollenweider DJ, Jarrett H, Steurer-Stey CA, Garcia-Aymerich J, Puhan MA (2012). Vollenweider, Daniela J (Ed.). "Antibiotics for exacerbations of chronic obstructive pulmonary disease". Cochrane Database Syst Rev. Cilt 12. ss. CD010257. doi:10.1002/14651858.CD010257. PMID 23235687.
- ^ "Fluoroquinolone Antibacterial Drugs: Drug Safety Communication - FDA Advises Restricting Use for Certain Uncomplicated Infections". FDA. 12 Mayıs 2016. 2 Temmuz 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Mayıs 2016.
- ^ "WHO Disease and injury country estimates". World Health Organization. 2009. 11 Şubat 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Kasım 2009.
- ^ a b Murray CJ, Vos T, Lozano R, Naghavi M, Flaxman AD, Michaud C, Ezzati M, Shibuya K, Salomon JA (Aralık 2012). "Disability-adjusted life years (DALYs) for 291 diseases and injuries in 21 regions, 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859). ss. 2197-223. doi:10.1016/S0140-6736(12)61689-4. PMID 23245608.
- ^ a b Vos T, Flaxman AD, Naghavi M, Lozano R, Michaud C, Ezzati M, Shibuya K, Salomon JA, Abdalla S, Aboyans V (Aralık 2012). "Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859). ss. 2163-96. doi:10.1016/S0140-6736(12)61729-2. PMID 23245607.
- ^ Medicine, prepared by the Department of Medicine, Washington University School of (2009). The Washington manual general internal medicine subspecialty consult (2. bas.). Wolters Kluwer Health/Lippincott Williams & Wilkins. s. 96. ISBN 978-0-7817-9155-7. 17 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ "Chronic obstructive pulmonary disease (COPD) Fact sheet N°315". WHO. Ocak 2015. 15 Temmuz 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Lozano R, Naghavi M, Foreman K, Lim S, Shibuya K, Aboyans V, Abraham J, Adair T, Aggarwal R (Aralık 2012). "Global and regional mortality from 235 causes of death for 20 age groups in 1990 and 2010: a systematic analysis for the Global Burden of Disease Study 2010". Lancet. 380 (9859). ss. 2095-128. doi:10.1016/S0140-6736(12)61728-0. PMID 23245604.
- ^ "The 10 leading causes of death in the world, 2000 and 2011". World Health Organization. Temmuz 2013. 7 Temmuz 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Kasım 2013.
- ^ Rycroft CE, Heyes A, Lanza L, Becker K (2012). "Epidemiology of chronic obstructive pulmonary disease: a literature review". Int J Chron Obstruct Pulmon Dis. Cilt 7. ss. 457-94. doi:10.2147/COPD.S32330. PMC 3422122 $2. PMID 22927753.
- ^ Simpson CR, Hippisley-Cox J, Sheikh A (2010). "Trends in the epidemiology of chronic obstructive pulmonary disease in England: a national study of 51 804 patients". Brit J Gen Pract. 60 (576). ss. 483-8. doi:10.3399/bjgp10X514729. PMC 2894402 $2. PMID 20594429.
- ^ Centers for Disease Control and Prevention (23 Kasım 2012). "Chronic Obstructive Pulmonary Disease Among Adults — United States, 2011". Morbidity and Mortality Weekly Report. 61 (46). ss. 938-43. PMID 23169314. 25 Haziran 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ "Morbidity & Mortality: 2009 Chart Book on Cardiovascular, Lung, and Blood Diseases" (PDF). National Heart, Lung, and Blood Institute. 19 Ekim 2013 tarihinde kaynağından (PDF) arşivlendi.
- ^ a b Torio CM, Andrews RM (2006). "National Inpatient Hospital Costs: The Most Expensive Conditions by Payer, 2011: Statistical Brief #160". Healthcare Cost and Utilization Project (HCUP) Statistical Briefs. Agency for Health Care Policy and Research. PMID 24199255. 14 Mart 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 2 Mart 2015.
- ^ Hoyert, DL; Xu, J (10 Ekim 2012). "Deaths: preliminary data for 2011". National vital statistics reports : from the Centers for Disease Control and Prevention, National Center for Health Statistics, National Vital Statistics System. 61 (6). ss. 1-51. PMID 24984457.
- ^ "Emphysema". Dictionary.com. 4 Mart 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 21 Kasım 2013.
- ^ a b Ziment, Irwin (1991). "History of the Treatment of Chronic Bronchitis". Respiration. 58 (Suppl 1). ss. 37-42. doi:10.1159/000195969. PMID 1925077.
- ^ a b c d Petty TL (2006). "The history of COPD". Int J Chron Obstruct Pulmon Dis. 1 (1). ss. 3-14. doi:10.2147/copd.2006.1.1.3. PMC 2706597 $2. PMID 18046898.
- ^ a b Wright, Joanne L.; Churg, Andrew (2008). "Pathologic Features of Chronic Obstructive Pulmonary Disease: Diagnostic Criteria and Differential Diagnosis" (PDF). Fishman, Alfred; Elias, Jack; Fishman, Jay; Grippi, Michael; Senior, Robert; Pack, Allan (Ed.). Fishman's Pulmonary Diseases and Disorders (4. bas.). McGraw-Hill. ss. 693-705. ISBN 978-0-07-164109-8.
- ^ Waldbott, George L. (1965). A struggle with Titans. Carlton Press. s. 6. 18 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ Fishman AP (Mayıs 2005). "One hundred years of chronic obstructive pulmonary disease". Am. J. Respir. Crit. Care Med. 171 (9). ss. 941-8. doi:10.1164/rccm.200412-1685OE. PMID 15849329.
- ^ Yuh-Chin, T. Huang (2012). A clinical guide to occupational and environmental lung diseases. Humana Press. s. 266. ISBN 978-1-62703-149-3. 17 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ "Pink Puffer – definition of Pink Puffer in the Medical dictionary – by the Free Online Medical Dictionary, Thesaurus and Encyclopedia". Medical-dictionary.thefreedictionary.com. 3 Mayıs 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Temmuz 2013.
- ^ a b c Weinberger, Steven E. (2013). Principles of pulmonary medicine (6. bas.). Elsevier/Saunders. s. 165. ISBN 978-1-62703-149-3. 17 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ Des Jardins, Terry (2013). Clinical Manifestations & Assessment of Respiratory Disease (6. bas.). Elsevier Health Sciences. s. 176. ISBN 978-0-323-27749-5. 18 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ An outcomes strategy for people with chronic obstructive pulmonary disease (COPD) and asthma in England (PDF). Department of Health. 18 Temmuz 2011. s. 5. 23 Haziran 2017 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 27 Kasım 2013.
- ^ Bloom, D (2011). The Global Economic Burden of Noncommunicable Diseases (PDF). World Economic Forum. s. 24. 4 Şubat 2015 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 2 Mart 2015.
- ^ "KOAH Engel Oranı". Engelli.com. 1 Ocak 2023. 1 Ocak 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 1 Ocak 2023.
- ^ Nici, Linda (2011). Chronic Obstructive Pulmonary Disease: Co-Morbidities and Systemic Consequences. Springer. s. 78. ISBN 978-1-60761-673-3. 18 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ a b Chong, Jimmy; Leung, Bonnie; Poole, Phillippa (4 Kasım 2013). "Phosphodiesterase 4 inhibitors for chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews, 11. ss. CD002309. doi:10.1002/14651858.CD002309.pub4. ISSN 1469-493X. PMID 24190161.
- ^ Inamdar, AC; Inamdar, AA (Ekim 2013). "Mesenchymal stem cell therapy in lung disorders: pathogenesis of lung diseases and mechanism of action of mesenchymal stem cell". Experimental Lung Research. 39 (8). ss. 315-327. doi:10.3109/01902148.2013.816803. PMID 23992090.
- ^ a b Oh, DK; Kim, YS; Oh, YM (Ocak 2017). "Lung Regeneration Therapy for Chronic Obstructive Pulmonary Disease". Tuberc Respir Dis (Seoul). 80 (1). ss. 1-10. doi:10.4046/trd.2017.80.1.1. PMC 5256352 $2. PMID 28119741.
- ^ Conese, M; Piro, D; Carbone, A; Castellani, S; Di Gioia, S (2014). "Hematopoietic and mesenchymal stem cells for the treatment of chronic respiratory diseases: role of plasticity and heterogeneity". The Scientific World Journal. Cilt 2014. s. 859817. doi:10.1155/2014/859817. PMC 3916026 $2. PMID 24563632.
- ^ McQualter, JL; Anthony, D; Bozinovski, S; Prêle, CM; Laurent, GJ (Kasım 2014). "Harnessing the potential of lung stem cells for regenerative medicine". The International Journal of Biochemistry & Cell Biology. Cilt 56. ss. 82-91. doi:10.1016/j.biocel.2014.10.012. PMID 25450456.
- ^ Tzouvelekis, A; Ntolios, P; Bouros, D (2013). "Stem cell treatment for chronic lung diseases". Respiration. 85 (3). ss. 179-192. doi:10.1159/000346525. PMID 23364286.
- ^ Tzouvelekis, A; Laurent, G; Bouros, D (Şubat 2013). "Stem cell therapy in chronic obstructive pulmonary disease. Seeking the Prometheus effect". Current Drug Targets. 14 (2). ss. 246-252. doi:10.2174/1389450111314020009. PMID 23256721.
- ^ Gompelmann, D; Eberhardt, R; Herth, FJ (Ağustos 2015). "Novel Endoscopic Approaches to Treating Chronic Obstructive Pulmonary Disease and Emphysema". Seminars in Respiratory and Critical Care Medicine. 36 (4). ss. 609-615. doi:10.1055/s-0035-1555614. PMID 26238645.
- ^ Gøtzsche, Peter C.; Johansen, Helle Krogh (20 Eylül 2016). "Intravenous alpha-1 antitrypsin augmentation therapy for treating patients with alpha-1 antitrypsin deficiency and lung disease". The Cochrane Database of Systematic Reviews. Cilt 9. ss. CD007851. doi:10.1002/14651858.CD007851.pub3. ISSN 1469-493X. PMID 27644166.
- ^ McLean, Susannah; Nurmatov, Ulugbek; Liu, Joseph Ly; Pagliari, Claudia; Car, Josip; Sheikh, Aziz (6 Temmuz 2011). "Telehealthcare for chronic obstructive pulmonary disease". The Cochrane Database of Systematic Reviews, 7. ss. CD007718. doi:10.1002/14651858.CD007718.pub2. ISSN 1469-493X. PMID 21735417.
- ^ Akers, R. Michael; Denbow, D. Michael (2008). Anatomy and Physiology of Domestic Animals. Wiley. s. 852. ISBN 978-1-118-70115-7. 17 Mayıs 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2017.
- ^ Wright, JL; Churg, A (Aralık 2002). "Animal models of cigarette smoke-induced COPD". Chest. 122 (6 Suppl). ss. 301S-6S. doi:10.1378/chest.122.6_suppl.301S. PMID 12475805.
- ^ Churg, A; Wright, JL (2007). "Animal models of cigarette smoke-induced chronic obstructive lung disease". Contributions to microbiology. Contributions to Microbiology. Cilt 14. ss. 113-25. doi:10.1159/000107058. ISBN 3-8055-8332-X. PMID 17684336.
- ^ Marinkovic D, Aleksic-Kovacevic S, Plamenac P (2007). "Cellular basis of chronic obstructive pulmonary disease in horses". Int. Rev. Cytol. International Review of Cytology. Cilt 257. ss. 213-47. doi:10.1016/S0074-7696(07)57006-3. ISBN 978-0-12-373701-4. PMID 17280899.
- ^ Miller MS, Tilley LP, Smith FW (Ocak 1989). "Cardiopulmonary disease in the geriatric dog and cat". Vet. Clin. North Am. Small Anim. Pract. 19 (1). ss. 87-102. PMID 2646821.
Dış bağlantılar[değiştir | kaynağı değiştir]
| Wikimedia Commons'ta Kronik obstrüktif akciğer hastalığı ile ilgili ortam dosyaları bulunmaktadır. |
- Curlie'de Kronik obstrüktif akciğer hastalığı (DMOZ tabanlı)
- Türk Toraks Derneği