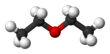
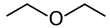Dietil eter
| |||

| |||
| Adlandırmalar | |||
|---|---|---|---|
Ethoxyethane | |||
Etoksietan | |||
Diğer adlar Etil eter, Etil oksit, Dietil oksit, 3-oksapentan, sülfürik eter | |||
| Tanımlayıcılar | |||
3D model (JSmol)
|
|||
| ECHA InfoCard | 100.000.425 | ||
CompTox Bilgi Panosu (EPA)
|
|||
| |||
| Özellikler | |||
| Kimyasal formül | C4H10O | ||
| Molekül kütlesi | 74,12 g mol−1 | ||
| Görünüm | Renksiz sıvı | ||
| Yoğunluk | 0.7134 g/cm3 | ||
| Erime noktası | -116.3°C | ||
| Kaynama noktası | 34.6°C | ||
| Buhar basıncı | 440 mmHg | ||
| Termokimya | |||
Isı sığası (C)
|
172.5 J/mol·K | ||
Standart molar entropi (S⦵298)
|
253.5 J/mol·K | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | Aşırı derecede yanıcı, havada patlayıcı peroksitler oluşturabilir | ||
| NFPA 704 (yangın karosu) |
|||
| Benzeyen bileşikler | |||
Benzeyen bileşikler
|
Etanol, Dimetil Eter | ||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |||
| Bilgi kutusu kaynakları | |||
Dietil eter, (IUPAC adı etoksietan) kısaca eter olarak da bilinen (C2H5)2O formülüne sahip berrak, renksiz, uçucu, kolay yanan ve parlayabilen, oda sıcaklığında sıvı hâlde bir bileşiktir. Kaynama noktası düşük olup hoş, karakteristik bir kokusu vardır. Toksisitesi çok düşüktür. Eterler olarak bilinen kimyasal bileşik sınıfının en çok tanınan üyesidir. Bütanolün izomeridir. Yapısı bir oksijene iki etil grubunun bağlanması ile oluşur ve CH3-CH2-O-CH2-CH3 şeklindedir. Çözücü olarak çokça kullanılır.
Tarih[değiştir | kaynağı değiştir]
Bileşik, 8. yüzyılda Câbir bin Hayyân tarafından[1] veya 1275'te Ramon Llull tarafından sentezlenmiş olabilir.[1][2]
1540 yılında Valerius Cordus tarafından sentezlendi ve "tatlı vitriol yağı" (oleum dulce vitrioli) adı verildi - bu isim, etanol ve sülfürik asit ("vitriol yağı") karışımının damıtılmasıyla elde edildiğini imâ ediyordu - ve bazı tıbbî özelliklerini gözlemledi.[1] Hemen hemen aynı zamanda Paracelsus, molekülün köpeklerde analjezik özelliklerini keşfetti.[1] Eter (aether) adı bu maddeye 1729 yılında August Sigmund Frobenius tarafından verildi.[3]
Yaklaşık 1800'de fikrin çürütülmesine kadar, bir kükürt bileşiği olarak kabul edildi[4] ve "sülfürik eter" dendi.
Üretim[değiştir | kaynağı değiştir]

Dietil eter genellikle etanol üretiminde etilenin hidrasyonunda yan ürün olarak ortaya çıkmaktadır. Bu işlemde katalizör olarak katı fosforik asit kullanılır ve daha fazla eter üretimi için ayarlanabilir. Alüminyum oksit üzerinde etanolün dehidratasyonu ile %95 oranına kadar dietil eter elde edilebilir.[5] Hem laboratuvarda, hem de sanayi yüksek miktarlarda, asit eter sentezi yoluyla dietil eter üretilebilir.[6] Etanol, sülfürik asit gibi güçlü bir asit ile karıştırılır, asit sulu ortamda proton vererek hidronyum (H3O+) iyonları oluşturur. Asidin hidrojeni, etanolün elektronegatif oksijenine proton verdiğinde etanol pozitif yüklenir:
- CH3CH2OH + H3O+ → CH3CH2OH2+ + H2O
Protonlanmamış etanolün oksijen atomu ile protonlanmış diğer etanol molekülünden bir su molekülü çıkararak su, dietil eter ve hidrojen iyonu oluşturur.
- CH3CH2OH2+ + CH3CH2OH → H2O + H+ + CH3CH2OCH2CH3
Bu tepkime etilen oluşmasını önlemek amacıyla 150 °C'den düşük sıcaklıklarda gerçekleştirilmelidir. Dietil eterin oluşma tepkimesi tersine dönebileceğinden ötürü oluşan dietil eter hemen damıtılmalıdır.
Dietil eter, Williamson eter sentezi yoluyla bir etil alkoksit ile etil halojenürden elde edilebilir.
Kullanımları[değiştir | kaynağı değiştir]
Dietil eter özellikle selüloz asetat gibi selüloz plastikleri için önemli bir çözücüdür.[7]
Yakıt[değiştir | kaynağı değiştir]
Dietil eter 86-96 yüksek bir setan numarasına sahip olduğundan benzinli ve dizel motorlarda hidrokarbonlar ile karıştırılarak kullanılabilir.[8] Uçuculuğunun fazla ve parlama noktasının düşük olması nedeniyle soğuk iklimli ülkelerde araç motorlarında başlatıcı sıvı olarak kullanılır.
Laboratuvar kullanımları[değiştir | kaynağı değiştir]
Dietil eter laboratuvarlarda aprotik çözücü olarak sıklıkla kullanılır. Suda çözünürlüğü düşüktür. Bu ve uçuculuğu birleştiğinde, sıvı-sıvı ekstraksiyonları için ideal bir apolar çözücüdür. Bir sulu çözeltiyle kullanıldığında, yoğunluğu düşük olan dietil eter tabakası üste çıkar.
Anestezik[değiştir | kaynağı değiştir]

William T. G. Morton, 16 Ekim 1846 tarihinde Boston, Massachusetts'te eterin anestezik özelliklerini göstermiştir. Dietil eter anestezik olarak ilk defa 30 Mart 1842 tarihinde Crawford Williamson Long tarafında bir ameliyatta kullanılmıştır.[9][10][11] 1840 kadar öncesinde İngiliz doktorlar eteri afyon ile birlikte kullanmaktaydı.[12] Dietil eter zehirli olmadığından çoğu zaman kloroforma tercih edilmiştir.[13] 2005 öncesinde Dünya Sağlık Örgütü'nün "En Önemli İlaçlar Listesi"nde anestezik olarak bulunmaktaydı.[14][15]
Eter Tüketimi[değiştir | kaynağı değiştir]
Soluma veya içme yoluyla yapılan dietil eter tüketimidir. Alışkanlığına eteromani de denir.
Metabolizma[değiştir | kaynağı değiştir]
Bir sitokrom P450 enziminin dietil eteri metabolize ettiği tahmin edilmektedir.[16] Dietil eter solunduğunda vücutta hızla emilir ve yaklaşık yüzde 90'ı havaya değişmeden atılır. Atılmayan dietil eter, sitokrom P450'ye bağlı bir monooksijenaz tarafından hidroksi-dietil etere ve ardından dealkilasyon ile etanal ve etanole dönüştürülür.[17]
Dietil eter, alkol dehidrojenazı inhibe eder ve böylece etanolün metabolizmasını yavaşlatır.[18]
Güvenlik[değiştir | kaynağı değiştir]
Dietil eter aşırı derecede yanıcıdır ve patlayıcı buhar/hava karışımları oluşturabilir. Eter havadan daha ağır olduğundan, zeminin altında toplanabilir ve buhar, ateşleme kaynaklarına kadar önemli mesafeler kat edebilir. Eter, açık bir aleve maruz kaldığında tutuşacaktır, ancak yüksek tutuşabilirliği nedeniyle, ateşleme için açık alev gerekli değildir. Diğer olası ateşleme kaynakları arasında -bunlarla sınırlı olmamak üzere -sıcak plakalar, buhar boruları, ısıtıcılar ve anahtarlar veya prizler tarafından oluşturulan elektrik arkları bulunur.[19] Buhar, bir kaptan diğerine eter dökülürken birikebilen statik elektrikle de tutuşabilir.
Eter, ışığa ve havaya duyarlıdır ve patlayıcı peroksitler oluşturma eğilimindedir; eter peroksitler, eterden daha yüksek kaynama noktasına sahiptir ve kuru olduklarında temas hâlinde patlayıcıdırlar.[19] Ticârî dietil eter tipik olarak eser miktarda peroksit oluşumunu azaltan antioksidan bütillenmiş hidroksitoluen (BHT) ile sağlanır.
Dietil eter zehirli değildir lâkin eter buharlarının uzun süre solunması alkol benzeri bir kafa karışıklığına ve hatta bilinç kaybına neden olabilir. Küçük dozlarda, buharların solunması, güçlü duygusal heyecan, değişen bilinç algısı ve karışık, psikotik düşünce zincirleri ile sarhoş edici durumlara neden olur. Daha yüksek dozlarda, tüketici artık konuşamayacağı kayıtsız bir duruma girer (anestezi).
Kaynakça[değiştir | kaynağı değiştir]
| Wikimedia Commons'ta Dietil eter ile ilgili ortam dosyaları bulunmaktadır. |
- ^ a b c d Toski, Judith A; Bacon, Douglas R; Calverley, Rod K (2001). The history of Anesthesiology. In: Barash, Paul G; Cullen, Bruce F; Stoelting, Robert K. Clinical Anesthesia (4 bas.). Lippincott Williams & Wilkins. s. 3. ISBN 978-0-7817-2268-1.
- ^ Hademenos, George J.; Murphree, Shaun; Zahler, Kathy; Warner, Jennifer M. (12 Kasım 2008). McGraw-Hill's PCAT. McGraw-Hill. s. 39. ISBN 978-0-07-160045-3. Erişim tarihi: 25 Mayıs 2011.
- ^ "VIII. An account of a spiritus vini æthereus, together with several experiments tried therewith". Philosophical Transactions of the Royal Society of London. 36 (413): 283-289. 1730. doi:10.1098/rstl.1729.0045.
- ^
 Chisholm, Hugh, (Ed.) (1911). "Ether". Encyclopædia Britannica. 9 (11. bas.). Cambridge University Press. s. 806.
Chisholm, Hugh, (Ed.) (1911). "Ether". Encyclopædia Britannica. 9 (11. bas.). Cambridge University Press. s. 806.
- ^ Ethyl Ether, Chem. Economics Handbook. Menlo Park, Calif: SRI International. 1991.
- ^ Cohen, Julius Berend (1920). A Class-book of Organic Chemistry, Volume 1. Londra: Macmillan and Co. s. 39.
the structure of ethyl alcohol cohen julius diethyl ether.
- ^ "Ethers, by Lawrence Karas and W. J. Piel". Kirk‑Othmer Encyclopedia of Chemical Technology. John Wiley & Sons, Inc. 2004.
- ^ "Extra Strength Starting Fluid: How it Works". Valvovine. 27 Eylül 2007 tarihinde kaynağından arşivlendi. Erişim tarihi: 5 Eylül 2007.
- ^ Hill, John W. and Kolb, Doris K. Chemistry for Changing Times: 10th Edition. p. 257. Pearson: Prentice Hall. Upper Saddle River, New Jersey. 2004.
- ^ Madden, M. Leslie (14 Mayıs 2004). "Crawford Long (1815–1878)". New Georgia Encyclopedia. University of Georgia Press. 13 Şubat 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 13 Şubat 2015.
- ^ "Crawford W. Long". Doctors' Day. Southern Medical Association. 13 Şubat 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 13 Şubat 2015.
- ^ Grattan, N. "Treatment of Uterine Haemorrhage". Provincial Medicine and Surgical Journal. Vol. 1, No. 6 (Nov. 7, 1840), p. 107.
- ^ Calderone, F.A. (1935). "Studies on Ether Dosage After Pre-Anesthetic Medication with Narcotics (Barbiturates, Magnesium Sulphate and Morphine)" (PDF). Journal of Pharmacology and Experimental Therapeutics. 55 (1): 24-39. 27 Mart 2009 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 12 Ağustos 2020.
- ^ "Essential Medicines WHO Model List (revised April 2003)" (PDF). apps.who.int (13.13 arşivurl=https://web.archive.org/web/20160627075448/http://apps.who.int/iris/bitstream/10665/68168/1/a80290.pdf bas.). Geneva, Switzerland: World Health Organization. Nisan 2003. 27 Haziran 2016 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 6 Eylül 2017.
- ^ "Essential Medicines WHO Model List (revised March 2005)" (PDF). apps.who.int (14.14ölüurl=evet bas.). Geneva, Switzerland: World Health Organization. Mart 2005. 5 Ağustos 2005 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 6 Eylül 2017.
- ^ 109. Aspergillus flavus mutant strain 241, blocked in aflatoxin biosynthesis, does not accumulate aflR transcript. 17 Eylül 2017 tarihinde Wayback Machine sitesinde arşivlendi. Matthew P. Brown and Gary A. Payne, North Carolina State University, Raleigh, NC 27695 fgsc.net
- ^ C. P. Chengelis, R. A. Neal: Microsomal metabolism of diethyl ether. In: Biochemical pharmacology. Band 29, Nummer 2, Februar 1980, S. 247–248, PMID 6767481.
- ^ P. T. Normann; A. Ripel; J. Morland (1987). "Diethyl Ether Inhibits Ethanol Metabolism in Vivo by Interaction with Alcohol Dehydrogenase". Alcoholism: Clinical and Experimental Research. 11 (2): 163-166. doi:10.1111/j.1530-0277.1987.tb01282.x. PMID 3296835.
- ^ a b "Archived copy" (PDF). 13 Kasım 2014 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 15 Şubat 2014.