Isıl denge
Bu madde hiçbir kaynak içermemektedir. (Mayıs 2020) (Bu şablonun nasıl ve ne zaman kaldırılması gerektiğini öğrenin) |
Bu maddenin veya maddenin bir bölümünün gelişebilmesi için kimya konusunda uzman kişilere gereksinim duyulmaktadır. (Eylül 2016) |
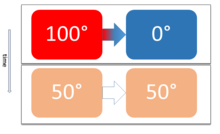
Isıl denge, kimya biliminde maddelerin son sıcaklıklarının eşit olma durumudur. Isıl denge değeri her daim, bir araya konulan maddelerin ilk sıcaklıkları arasında bir değerdedir. Isıca yalıtılmış bir kaba hem sıcak hem de soğuk su koyulursa, sıcak sudan soğuk suya enerji aktarımı gerçekleşir. Enerji aktarımı her zaman sıcaktan soğuğa doğrudur. Böylece etkileşim sonucunda sıcak madde soğur, soğuk madde ısınır. Bu olay, sıcaklıklar eşitlenene kadar devam eder. Bu durum "Qalınan = Qverilen" şeklinde sembolize edilir.
Isıl denge hesabı[değiştir | kaynağı değiştir]
- Eşit miktarda olması kaydıyla aynı cins sıvılar karıştırılırsa ısıl denge maddelerin sıcaklıklarının aritmetik ortalamasıdır. Örneğin ısıca yalıtılmış A ve B kaplarını düşünelim: A kabında bulunan sıvının sıcaklığı 20°, B kabında bulunan sıvının sıcaklığı 40°dir. İki kaptaki sıvılar aynı cins ve eşit miktarda ise, ısıl denge 30°dir.
- Sıvılar farklı miktarda karıştırılırsa, karışımın ısıl dengesi değeri, ısı sığası büyük olan sıvının sıcaklığına daha yakındır. Isı sığası kütle ile öz ısının çarpımı anlamına gelir ve formülü C=mc'dir.
- Maddelerin hâl değiştirmemesi şartıyla aynı kaba konulan x tane maddenin ısıl dengesi değeri; her bir maddenin ısı sığası ile sıcaklığı çarpılır, tüm maddelerin bu değerleri toplanır. Son olarak maddelerin ısı sığası toplamlarına bölünür.
- Farklı kütleleri ve farklı öz ısıları olan iki ayrı cins sıvıyı ele alalım. Bu sıvılarımız X ve Y sıvısı olsun. Bu iki sıvı aynı kaba koyulduğunda oluşan karışımın ısıl denge sonucunda ulaştığı denge sıcaklığını mx . cx .(Tx - Tdenge) = my . cy .(Tdenge - Ty) denklemi ile bulabiliriz. Bu denklemde T=sıcaklık, c=öz ısı, m=kütle'dir (bu denklemde sıcaklığı büyük olan sıvı X sıcaklığı küçük olan sıvı Y olarak alınmıştır, sıvılar hal değiştirmemiştir).
| Kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |
