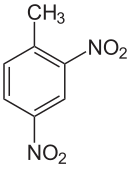
2,4-Dinitrotoluen
| |

| |
| Adlandırmalar | |
|---|---|
1-Metil-2,4-dinitrobenzen | |
Diğer adlar Dinitrotoluol, Metildinitrobenzen | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.004.046 |
| KEGG | |
PubChem CID
|
|
| UNII | |
| UN numarası | Erimiş: 1600 Katı veya sıvı: 2038 |
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Kimyasal formül | C7H6N2O4 |
| Molekül kütlesi | 182,13 g mol−1 |
| Görünüm | Uçuk sarı- turuncu renge sahip kristal katı |
| Yoğunluk | 1.52 g/cm3[1] |
| Erime noktası | 70 °C[1] |
| Kaynama noktası | 250–300 °C’de bozunur[1] |
| Buhar basıncı | 1.47X10-4 mm Hg @ 22 C |
| Tehlikeler | |
| İş sağlığı ve güvenliği (OHS/OSH): | |
| Ana tehlikeler | kanserojen, yanıcı (tutuşması zor olsa da)[3] |
| GHS etiketleme sistemi: | |
| Piktogramlar |   
|
| İşaret sözcüğü | Tehlike |
| Tehlike ifadeleri | H301+H311+H331, H341, H350, H361f, H373, H410 |
| Önlem ifadeleri | P201, P261, P280, P301+P310+P330, P308+P313, P403+P233 |
| Parlama noktası | 404 °C |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz)
|
1,954 mg/kg (oral, fare)[4] |
LDLo (yayınlanan en düşük)
|
27 mg/kg (kedi, oral)[4] |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | TWA 1.5 mg/m3 [deri][3] |
| REL (tavsiye edilen) | Ca TWA 1.5 mg/m3 [deri][3] |
| IDLH (anında tehlike) | Ca [50 mg/m3][3] |
| Patlayıcı verileri | |
| Şok duyarlılığı | Duyarsız |
| Sürtünme duyarlılığı | Çok düşük |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
2,4-Dinitrotoluen (DNT) veya dinitro, C7H6N2O4 formülüne sahip bir organik bileşiktir. Bu uçuk sarı kristal katı, trinitrotoluenin (TNT) bir öncü maddesi olarak bilinse de, esas olarak toluen diizosiyanatın bir öncü maddesi olarak üretilir.
Dinitrotoluen izomerleri
[değiştir | kaynağı değiştir]Dinitrotoluen için altı konumsal izomer mümkündür. En yaygın olanı 2,4-dinitrotoluen’dir. Toluenin nitrolaması sırayla mononitrotoluen, DNT ve son olarak TNT’yi verir. 2,4-DNT, dinitrolamadan elde edilen ana ürün olup, diğer ana ürün yaklaşaık %30 1,3-DNT’dir. 4-nitrotoluenin nitrolanması 2,4-DNT verir.[5]
Kullanım alanları
[değiştir | kaynağı değiştir]DNT çoğunlukla, esnek poliüretan köpükler üretmek için kullanılan toluen diizosiyanat üretiminde kullanılır. DNT, hidrojene edilerek 2,4-toluendiamin üretilir. Elde edilen 2,4-toluendiamin fosgen ile işleme sokularak toluen diizosiyanat üretilir. Bu şekilde, 1999–2000 yılları arasında yaklaşık 1,4 milyar kilogram üretilmiştir.[6] Diğer kullanım alanı patlayıcı maddeler endüstrisidir. Tek başına patlayıcı madde olarak kullanılmaz. Ancak üretiminin bir kısmı TNT'ye dönüştürülür.
Dinitrotoluen, itici yakıtlarda (örn., dumansız barutlar) sıklıkla plastikleştirici, önleyici kaplaması ve yanma oranı değiştiricisi olarak kullanılır. Kanserojen[3] ve zehirli olduğu için, modern formülasyonlar kullanımından kaçınma eğilimindedir. Bu uygulamada genellikle dibütil ftalat ile birlikte kullanılır.
Zehirlilik
[değiştir | kaynağı değiştir]Dinitrotoluenler, 1.5 mg/m3 eşik sınır değeri (TLV) ile oldukça zehirlidir.[7] Hemoglobini methemoglobine dönüştürür.
2,4-Dinitrotoluen ayrıca 40 CFR 261.24 kapsamında listelenmiş bir tehlikeli atıktır. Amerika Birleşik Devletleri Çevre Koruma Ajansı (EPA) Tehlikeli Atık Numarası D030’dur. Toksik özelliklere sahip olmamak için içerilebilecek maksimum konsantrasyon 0.13 mg/L’dir.
Yararlanılan kaynaklar
[değiştir | kaynağı değiştir]- ^ a b c Alman İş Güvenliği ve Sağlığı Enstitüsü'nün GESTIS Madde Veritabanındaki 2,4-Dinitrotoluene kaydı, accessed on 9. October 2007.
- ^ Pella, PA. J. Chem. Thermodyn. 9: 301-305, 1977
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards. "#0235". National Institute for Occupational Safety and Health (NIOSH).
- ^ a b "Dinitrotoluene (mixed isomers)". Immediately Dangerous to Life or Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH). 4 Aralık 2014. 10 Şubat 1999 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Temmuz 2023.
- ^ Gerald Booth (2007). "Nitro Compounds, Aromatic". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a17_411. ISBN 978-3527306732.
- ^ Six, C.; Richter, F. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a14_611.
- ^ "NIOSH Pocket Guide to Chemical Hazards - Dinitroluene". 10 Mayıs 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 25 Temmuz 2023.
Dış bağlantılar
[değiştir | kaynağı değiştir] Wikimedia Commons'ta Dinitrotoluenes ile ilgili çoklu ortam belgeleri bulunur
Wikimedia Commons'ta Dinitrotoluenes ile ilgili çoklu ortam belgeleri bulunur
