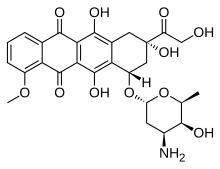
Doksorubisin
 | |
| Klinik verisi | |
|---|---|
| Gebelik kategorisi |
|
| Uygulama yolu | İntravenöz |
| Hukuki durum | |
| Hukuki durum |
|
| Farmakokinetik veri | |
| Biyoyararlanım | 5% (Oral) |
| Metabolizma | CYP3A4 |
| Eliminasyon yarı ömrü | 12–18.5 saat, lipozomlardan salındığında[1] |
| Boşaltım | Safra ve fekal |
| Tanımlayıcılar | |
| |
| CAS Numarası | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| CompTox Bilgi Paneli (EPA) | |
| ECHA Bilgi Kartı | 100.041.344 |
| Kimyasal ve fiziksel veriler | |
| Formül | C27H29NO11 |
| Mol kütlesi | 543.52 |
Doksorubisin ya da hidroksidaunorubisin (ticarî adıyla Adriamisin), kanser kemoterapisinde kullanılan bir ilaçtır. Bir antrasiklin türevi antibiyotiktir, doğal bir ürün olan daunomisin ile yakından ilişkilidir ve diğer tüm antrasiklinler gibi DNA içine enterkalasyon yapar. Çeşitli kanserlerin tedavisinde kullanılır, bunların arasında hematolojik kanserler, çeşitli karsinoma tipleri ve yumuşak doku sarkomaları sayılabilir.
İlaç hidroklorür tuzu şeklinde damardan verilir. Marka ismi olarak Adriamycin PFS, Adriamycin RDF veya Rubex olarak satılabilir.[2] Işığa duyarlıdır ve ışık tarafından etkilenmemek için genelde alüminyum torba içinde saklanır.
Molekül DSÖ'nün Temel İlaçlar Listesi'nde yer almaktadır.
Tarih
[değiştir | kaynağı değiştir]Doksorubisinin tarihi 1950'lerde, Farmitalia adlı bir İtalyan araştırma şirketinin toprak mikroplarından üretilen antikanser bileşikleri bulma girişimine dayanır. 13. yüzyıldan kalma bir kale olan Castel del Monte civarından elde edilen bir toprak numunesinde yeni bir Streptomyces peucetius suşu izole edilmiş ve bu bakterinin ürettiği kırmızı renkli bir antibiyotiğin fare tümörleri üzerinde iyi bir etkinliğe sahip olduğu bulunmuştur. Yaklaşık aynı zamanda bir grup Fransız araştırmacı da aynı bileşiği keşfettiği için bu iki araştırma ekibi ona daunorubisin adını verdiler. Bu ad, İtalya'da bu maddenin keşfedildiği bölgede yaşamış olan Roma-öncesi bir kabile olan Dauni ile, bu kimyasalın yakut renginin Fransızca kaşılığı olan rubis sözcüğünün birleştirilmesi ile türetilmiştir.[3] 1960'larda klinik deneylere başlanmış ve ilacın akut lösemi ve lenfoma tedavisinde başarılı olmuştur. Ancak 1967'de daunorubisinin ölümcül kardiyak toksisiteye neden olduğu bulunmuştur.[4]
Framitalia'daki araştırmacılar bu bileşiğin kimyasal yapısında modifikasyonlar yaparak biyolojik etkinlikte değişiklikler elde edilebildiğini keşfettiler. Başka bir Streptomyces suşu mutasyona uğratılmış ve bu yeni suş farklı bir kırmızı renkli antibiyotik üretmiştir. Bu yeni bileşik (Adriyatik denizine atfen) Adriamycin olarak adlandırılmış, daha sonra adlandırma konvasiyonlarına uyumlu olmak için bu ad doksorubisin olarak değiştirilmiştir.[5] Doksorubisin fare tümörlerinde, özellikle katı tümörlerde, daunorubisinden daha iyi etki göstermiştir. Ayrıca daha yüksek bir terapötik endeks göstermiş ama kardiyotoksisitesi kalmıştır.[6]
Doksorubisin ve daunorubisin birlikte antrasiklinler için prototip bileşikler olarak düşünülebilir. İzleyen araştırmalar ile pek çok başka antrasiklin antibiyotikleri keşfedilmiştir, günümüzde doksorubisin'in 2000'den çok analogu olduğu kestirilmektedir. 1991'de bunlardan 553'ü ABD Millî Kanser Ensititüsünün (National Cancer Institute) bir tarama programında değerlendirilmiştir.[3]
Biyosentez
[değiştir | kaynağı değiştir]Doksorubisin (DXR)'in biyosentetik yolağının son adımında onun öncülü (prekürsörü) olan daunorubisin'in 14 numaralı karbonu hidroksile edilir. Daunorubisin bir doğal ürün olarak daha bol miktarda bulunur çünkü streptomyces cinsinin çeşitli yaban tipi (wild type) suşları tarafından üretilir. Buna karşın tek bir yaban tipi olmayan tür, streptomyces peucetius alt türü olan cesius ATCC 27952'nin, tıpta daha yaygın kullanılan doksorubisin'i ürettiği bulunmuştur.[7] Bu suş, daunorubisin üreten ama DXR üretmeyen bir suşun mutasyonu ile elde edilmiştir.[8] Bunun ardından özel şartlarda veya mutasyon yoluyla, diğer streptomyces suşlarının da doksorubisin ürettiği gösterilmiştir.[9] DXR üretimi için gerekli olan çoğu gen klonlanmıştır. 1996'da daunorubisin'i DXR'ye dönüştüren dox A geni keşfedilmiş ve karakterize edilmişir.[10] Bu genin ürünü, bir sitokrom P450 oksidaz olan Dox A'dır. Dox A proteini 1999'da rekombinant biçimi üretilmiş ve DXR biyosentezinin birden çok adımını (daunorubisin'i oluşturan son adım da dahil olmak üzere) katalizlediği bulunmuştur.[11] Bu önemli bir keşifti çünkü daunorbisin üreten suşların hepsinde DXR üretmek için gerekli olan genlere sahip olduğu bulunmuştur. Tıbben daha önemli olan DXR'nin eldesini iyileştirmek için çeşitli çalışmalar yapılmış, bakterinin içine DoxA kodlayan plazmitler sokulmuş, ayrıca DXR prekürsörlerini faydasız bileşiklere (örneğin baumycin-benzeri glikositlere) dönüştüren enzimler mutasyon yoluyla inaktive edilmiştir.[7] Dox A'yı aşırı derecede ifade eden bazı üçlü mutantlar DXR eldesini iki katına çıkarabilmiştir. O tarihlerde DXR'nin fiyatı $1.37 million/kg'di ve 1999'da yıllık üretim 225 kg idi.[12] Daha verimli üretim teknikleri sayesinde lipozomal olmayan formülasyon için fiyatı $1.1 milyon/kg'a düşürmüştür. DXR yarı sentetik olarak daunorubisinden de üretilebilir ama bu süreç elektrofilik brominasyon ve çok sayıda reaksiyon içerir, bu yüzden reaksiyon eldesi düşüktür.[13] Daunorubisin fermantasyon ile üretildiği için bakterilerin DXR'yi daha etkili şekilde sentezleyebilmesi ideal olacaktır.

Etki mekanizması
[değiştir | kaynağı değiştir]Doksorubisin'in tam etki mekanizması karmaşık ve hâlâ tamamen anlaşılmamış olmakla beraber enterkalasyon yoluyla DNA ile etkileştiği düşünülmektedir.[14] Doksorubisin enterkalasyon yoluyla etkileşip onun biyosentezini engellediği bilinmektedir.[15] transkripsiyon sırasında DNA'nın açılmasını sağlayan Topoizomeraz II enziminin ilerlemesi engellenir. Doksorubisin DNA ikileşmesi sırasında topoizomerazın DNA'yı kesmesinin ardından meydana gelen topoizomeraz-DNA kompleksini stabilize ederek DNA ikili sarmalının tekrar birleşmesini engeller ve böylece DNA ikileşmesini durdurur.
Kristal yapılarının analizinde görüldüğü üzere, molekülün düzlemsel kromofor kısmı DNA'daki iki baz çifti arasına enterkale olur, onun altı-üyeli daunosamin şekeri DNA'nın küçük oyuğuna yerleşir ve enterkalasyon yerinin iki tarafındaki baz çiftleri ile etkileşir.[16][17]
Klinik kullanım
[değiştir | kaynağı değiştir]Doksorubisin bazı lösemileri, Hodgkin lenfoma, yumuşak doku sarkoması, mültipl miyelom ayrıca mesane, göğüs, mide, akciğer, over, tiroit ve diğer kanseleri tedavi etmek için kullanılır.[2] Yaygın kullanılan doksorubisin içeren rejimler arasında AC (Adriamycin, cyclophosphamide), TAC (Taxotere, CA), ABVD (Adriamycin, Bleomycin, Vinblastine, Dacarbazine), BEACOPP, CHOP (Cyclophosphamide, Adriamycin, Vincristine, Prednisone) and FAC (5-Fluorouracil, Adriamycin, Cyclophosphamide) sayılabilir. Doxil, AIDS-ilişkili Kaposi sarkom tedavisinde, ayrıca over kanseri tedavisinde kullanılır, hastalık platin-tabanlı kemoterapiden sonra ilerler veya nüksederse.[18]
Deneysel tedavi
[değiştir | kaynağı değiştir]Sirolimus (rapamycin) ve doksorubisin ile yapılan kombine tedavi deneyleri farelerde Akt-pozitif lenfomaların iyileştirilmesinde ümit verici olmuştur.[19]
Doksorubisin'in bir fare monoklonal antikoruna bağlanmasıyla elde edilen immünobileşik farelerde HIV-1 enfeksiyonunu yok edebilmiştir. antiretroviral tedavi (ART) hâlâ konak canlıda bir miktar HIV bırakmaktadır. Antijen ifade etmeye devam eden T hücrelerini yok etmek için doksorubisinli immünobileşiğin, ART'yi tamamlayıcı bir tedavi olma potansiyeli vardır.[20]
Liposomal formülasyonlar
[değiştir | kaynağı değiştir]Doxil peglenmiş (polietilen glikol kaplı) lipozom içine kapsüllenmiş bir doksorubisin biçimidir, ABD'de Johnson & Johnson için Ben Venue Laboratories tarafından imal edilir. Bu ilaç Kaposi sarkomunu tedavi etmek için geliştirilmiştir (AIDS'le ilişkili olan bu hastalıkta oluşan lezyonlar deri, ağzın içi, burun, boğaz ve diğer organlarda büyür). Polietilen glikol kaplama Doxil'in deride konsantre olmasını sağlar. Ancak, bunun bir yan etkisi, el-ayak sendromu olarak da bilinen palmar plantar erythrodysesthesia (PPE)'dir. Doxil verilmesinin ardından bu ilacın ufak bir bölümü el ayası ve ayak tabanındaki kapiler damarlardan sızabilir. Bu sızmanın sonucu deride rahatsız edici hatta acı verici derecede bir kızarıklık, hassasiyet ve soyulmadır. Klinik denemelerde hastalara 4 hafta boyunca 50 mg/m2 dozajda Doxil verilince hastaların yaklaşık yarısında el-ayak sendromu oluşmuştur. Bu yan etkinin sıklığı, aynı tedavi rejiminde doksorubisin yerine Doxil verilmesine kısıtlama getirir. Bu yan etki olmasa Doxil substitusyonu tercihlidir, çünkü lipozom enkapsüle doksorubisin, enkapsüle edilmemiş doksorubisinden daha az kardiotoksiktir. Doxil ayrıca over kanseri ve mültipl miyelom tedavisi için ABD'de FDA tarafından onaylıdır. ABD dışında Doxil, Caelyx olarak bilinir ve Schering-Plough tarafından pazarlanır.
Myocet, peglenmemiş bir lipozomal doksorubisin formülasyonudur, Enzon Pharmaceuticals tarafından Avrupa'da Cephalon için, ABD ve Kanada'da Sopherion Therapeutics için imal edilir. Myocet,cyclophosphamide ile birlikte, Avrupa ve Kanada'da metastatik göğüs kanseri tedavisinde kullanılır, ama ABD'de bu tedavi hâlâ FDA onayı beklemektedir. Doxil'den farklı olarak Myocet lipozomunda polietilen glikol olmadığı için el-ayak sendromuna neden olmaz. Bu yan etkinin bertaraf edilmesi bu ilacın doksorubisin ile birebir değiştirilmesine olanak verir. Doxil gibi Myocet'de de kardiotoksisite olmadığı için diğer kardiotoksik kemoterapi ilaçları (Herceptin gibi) ile birlikte kombine tedaviler için kullanılabilir.[21][22]
Yan etkiler
[değiştir | kaynağı değiştir]Doksorubisin'in akut yan etkileri arasında mide bulanması, kusma ve kalp düzensizliği sayılabilir. Ayrıca nötropenia (akyuvarlarda azalma) ve kellik de olabilir. Kümülatif doksorubisin dozu 550 mg/m²'ye ulaşınca kardiyak yan etkiler (kalp yetmezliği, kardiyomiyopati ve ölüm) dramatik şekilde artar. Doksorubisin kardiotoksisitesi mitokondrilerdeki oksidatif fosforilasyonda dozla orantılı bir azalma ile karakterizedir. Doksorubisin ve demir etkileşiminden kaynaklanan Reaktif oksijen türleri miyositlere (kalp hücrelerine) zarar verebilir, miyofibrilar kayıp ve sitoplazmada vakuol oluşmasına neden olabilmektedir. Ayrıca, bazı hastalarda el-ayak sendromu (palmar plantar erythrodysesthesia) meydana gelebilmektedir.[18]
Bu yan etkiler ve kırmızı rengi nedeniyle doksorubisin "kırmızı şeytan"[23] veya "kırmızı ölüm"[24] takma adları ile anılır.
Ayrıca bakınız
[değiştir | kaynağı değiştir]Kaynakça
[değiştir | kaynağı değiştir]- ^ Laginha, K.M. "Determination of Doxorubicin Levels in Whole Tumor and Tumor Nuclei in Murine Breast Cancer Tumors 26 Ağustos 2009 tarihinde Wayback Machine sitesinde arşivlendi.." Clinical Cancer Research. October 1, 2005. Vol. 11 (19). Retrieved on April 19, 2007.
- ^ a b "Doxorubicin (Systemic) 3 Nisan 2007 tarihinde Wayback Machine sitesinde arşivlendi.." Mayo Clinic. Last updated on: June 15, 1999. Retrieved on April 19, 2007.
- ^ a b Weiss, Raymond B. "The Anthracyclines: Will We Ever Find a Better Doxorubicin?" Seminars in Oncology. Vol. 19, No. 6. December 1992. pp. 670–686. PMID 1462166.
- ^ Tan, C.; Tasaka, H.; Kou-Ping, Y.; et al. Daunomycin, An Antitumor Antibiotic, In the Treatment of Neoplastic Disease. Clinical Evaluation with Special Reference to Childhood Leukemia. 1967, Cancer, 20, 333 – 353. PMID 4290058.
- ^ Arcamone, F.; Cassinelli, G.; Fantini, G.; et al. Adriamycin, 14-hydroxydaunomycin, A New Antitumor Antibiotic from S. peucetius var. caesius. 1969, Biotechnol. Bioeng., 11, 1101 – 1110. PMID 5365804.
- ^ Di Marco, A.; Gaetani, M.; Scarpinato, B. Adriamycin (NSC-123,127): A New Antibiotic with Antitumor Activity. 1969, Cancer Chemotherapy Reports, 53, 33 – 37. PMID 5772652.
- ^ a b Lomovskaya N, Otten SL, Doi-Katayama Y; ve diğerleri. (1999). "Doxorubicin overproduction in Streptomyces peucetius: cloning and characterization of the dnrU ketoreductase and dnrV genes and the doxA cytochrome P-450 hydroxylase gene". J. Bacteriol. 181 (1). ss. 305-18. PMID 9864344.
- ^ Arcamone F, Cassinelli G, Fantini G; ve diğerleri. (1969). "Adriamycin, 14-hydroxydaunomycin, a new antitumor antibiotic from S. peucetius var. caesius". Biotechnol. Bioeng. 11 (6). ss. 1101-10. doi:10.1002/bit.260110607. PMID 5365804.
- ^ Grimm A, Madduri K, Ali A, Hutchinson CR (1994). "Characterization of the Streptomyces peucetius ATCC 29050 genes encoding doxorubicin polyketide synthase". Gene. 151 (1–2). ss. 1-10. doi:10.1016/0378-1119(94)90625-4. PMID 7828855.
- ^ Dickens ML, Strohl WR (1996). "Isolation and characterization of a gene from Streptomyces sp. strain C5 that confers the ability to convert daunomycin to doxorubicin on Streptomyces lividans TK24". J. Bacteriol. 178 (11). ss. 3389-95. PMID 8655530.
- ^ Walczak RJ, Dickens ML, Priestley ND, Strohl WR (1999). "Purification, properties, and characterization of recombinant Streptomyces sp. strain C5 DoxA, a cytochrome P-450 catalyzing multiple steps in doxorubicin biosynthesis". J. Bacteriol. 181 (1). ss. 298-304. PMID 9864343.
- ^ Hutchinson CR, Colombo AL (1999). "Genetic engineering of doxorubicin production in Streptomyces peucetius: a review". J. Ind. Microbiol. Biotechnol. 23 (1). ss. 647-52. doi:10.1038/sj.jim.2900673. PMID 10455495.
- ^ Lown JW (1993). "Anthracycline and anthraquinone anticancer agents: current status and recent developments". Pharmacol. Ther. 60 (2). ss. 185-214. doi:10.1016/0163-7258(93)90006-Y. PMID 8022857.
- ^ Fornari, F.A.; Randolph, J.K.; Yalowich, J.C.; Ritke, M.K.; Gewirtz, D.A. Interference by Doxorubicin with DNA Unwinding in MCF-7 Breast Tumor Cells. 1994, Molecular Pharmacology, 45, 649 – 656. PMID 8183243.
- ^ Momparler, R.L.; Karon, M.; Siegel, S.E.; Avila, F. Effect of Adriamycin on DNA, RNA and Protein Synthesis in Cell-Free Systems and Intact Cells. 1976, Cancer Research, 36, 2891 – 2895. PMID 1277199. Free full text 5 Şubat 2009 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ Frederick, C.A.; Williams, L.D.; Ughetto, G.; van der Marel, G.A.; van Boom, J.H.; Rich, A.; Wang, A.H. Structural Comparison of Anticancer Drug-DNA Complexes: Adriamycin and Daunomycin. 1990, Biochemistry, 29, 2538 – 2549. PMID 2334681. Crystal structure is available for download as a PDB 14 Ocak 2008 tarihinde Wayback Machine sitesinde arşivlendi. file.
- ^ Pigram, W.J.; Fuller, W.; Hamilton, L.D. Stereochemistry of Intercalation: Interaction of Daunomycin with DNA. 1972, Nature New Biology, 235, 17 – 19. PMID 4502404.
- ^ a b "DOXIL Product Information" (PDF). Ortho Biotech Products, L.P. 13 Mayıs 2008 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 19 Nisan 2007.
|çalışma=dış bağlantı (yardım) - ^ Wendel H, De Stanchina E, Fridman J, Malina A, Ray S, Kogan S, Cordon-Cardo C, Pelletier J, Lowe S (2004). "Survival signalling by Akt and eIF4E in oncogenesis and cancer therapy". Nature. 428 (6980). ss. 332-7. doi:10.1038/nature02369. PMID 15029198.
- ^ Johansson S, Goldenberg D, Griffiths G, Wahren B, Hinkula J (2006). "Elimination of HIV-1 infection by treatment with a doxorubicin-conjugated anti-envelope antibody". AIDS. 20 (15). ss. 1911-1915. doi:10.1097/01.aids.0000247111.58961.60. PMID 16988511.
- ^ "Cancerbackup: Liposomal doxorubicin (Caelyx, Myocet)". 4 Mayıs 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Ocak 2011.
- ^ "Chemocare: Doxorubicin liposomal". 2 Ocak 2010 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Ocak 2011.
- ^ Bloch, Richard. "25 Most Asked Questions". Fighting Cancer. R. A. Bloch Cancer Foundation. 9 Nisan 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 28 Haziran 2007.
- ^ Groopman, Jerome E. (2007). How Doctors Think. Boston: Houghton Mifflin. ss. 49. ISBN 0-618-61003-0.
Dış bağlantılar
[değiştir | kaynağı değiştir]- Overview at BC Cancer Agency
- Doxil Site
- Adriamycin Solution / Doxorubicin hydrochloride Virtual Cancer Centre
- Doksorubisin içeren ilçalar 26 Ocak 2013 tarihinde Wayback Machine sitesinde arşivlendi.
