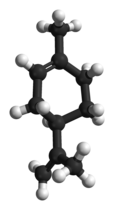
Limonen
Bu Lemonene ya da bir kısmının Türkçeye çevrilmesi gerekmektedir. Bu sayfanın tamamı ya da bir kısmı Türkçe dışındaki bir dilde yazılmıştır. Madde, alakalı dilin okuyucuları için oluşturulmuşsa o dildeki Vikipedi'ye aktarılmalıdır. İlgili değişiklikler gerçekleşmezse maddenin tamamının ya da çevrilmemiş kısımların silinmesi sözkonusu olabilecektir. İlgili çalışmayı yapmak üzere bu sayfadan destek alabilirsiniz |

| |||
| |||

| |||
| Adlandırmalar | |||
|---|---|---|---|
Tercih edilen IUPAC adı 1-Methyl-4-(prop-1-en-2-yl)cyclohex-1-ene | |||
Diğer adlar 1-Methyl-4-(1-methylethenyl)cyclohexene 4-Isopropenyl-1-methylcyclohexene p-Menth-1,8-diene Racemic: DL-Limonene; Dipentene | |||
| Özellikler | |||
| Kimyasal formül | C10H16 | ||
| Molekül kütlesi | 136,23 g mol−1 | ||
| Görünüm | renksizden soluk-sarı sıvıya | ||
| Koku | Portakal | ||
| Yoğunluk | 0.8411 g/cm3 | ||
| Erime noktası | -74.35 | ||
| Kaynama noktası | 176 | ||
| Çözünürlük | Miscible with benzene, chloroform, ether, CS2, and oils soluble in CCl4 | ||
Kiral dönüş ([α]D)
|
87–102° | ||
| Kırınım dizimi (nD) | 1.4727 | ||
| Termokimya | |||
Standart yanma entalpisi (ΔcH⦵298)
|
−6.128 MJ mol−1 | ||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | Skin sensitizer / Contact dermatitis – After aspiration, pulmonary oedema, pneumonitis, and death[1] | ||
| GHS etiketleme sistemi: | |||
| Piktogramlar |    
| ||
| İşaret sözcüğü | Tehlike | ||
| Tehlike ifadeleri | H226, H304, H315, H317, H410 | ||
| Önlem ifadeleri | P210, P233, P235, P240, P241, P242, P243, P261, P264, P272, P273, P280, P301+P330+P331, P302+P352, P303+P361+P353, P304+P340, P312, P333+P313, P362, P370+P378, P391, P403+P233, P405, P501 | ||
| NFPA 704 (yangın karosu) |
|||
| Parlama noktası | 50 | ||
| 237 °C (459 °F; 510 K) | |||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa). | |||
| Bilgi kutusu kaynakları | |||
Limonen renksiz bir sıvıdır alifatik hidrokarbon döngüsel monoterpen olarak sınıflandırılır ve turunçgillerin meyve kabuklarının içindeki yağın ana bileşenidir.[1] D-izomeri doğada daha çok portakal kokusu olarak ortaya çıkan gıda üretiminde kullanılan bir tatlandırıcıdır.[1][2] Ayrıca kimyasal sentezde öncü ila carvone ve temizlik ürünlerinde yenilenebilir bazlı çözücü olarak da kullanılır.[1] Daha az yaygın olan L- izomer nane yağlarında bulunur ve çam, terebentin benzeri bir kokuya sahiptir.[1] Bileşik iğne yapraklıların reçinesinde özellikle Pinaceae ve portakal yağında bulunan ana uçucu monoterpenlerden biridir. Limonene adını Fransızca lemondan ("limon") alır.[3] Limonen bir kiral molekülüdür ve biyolojik kaynaklar bir enantiyomer üretir: ana endüstriyel kaynak narenciye (R)-enantiyomer olan D-limonene((+)- limonen) içerir.[4] D-Limonen ticari olarak iki ana yöntemle turunçgillerden elde edilir: santrifüjlü ayırma veya buharla damıtma.
Kimyasal reaksiyonlar
Limonen nispeten kararlı bir mono terpen 'dir ve yüksek sıcaklıklarda izopren oluşturmak için çatlamasına rağmen ayrışma olmaksızın damıtılabilir.[5] Carveol, carvone ve limonen oksit üretmek için nemli havada kolayca oksitlenir.[1][6] Kükürt ile "p" - simen şeklinde dehidrojenasyona uğrar.[7]
Kaynakça
- ^ a b c d e f "D-Limonene". PubChem Compound Database. National Center for Biotechnology Information, US National Library of Medicine. 2017. 18 Mayıs 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 Aralık 2017.
- ^ Kaynak hatası: Geçersiz
<ref>etiketi;Ullmannisimli refler için metin sağlanmadı (Bkz: Kaynak gösterme) - ^ Merriam-Webster's dictionary entry for "limonene". Accessedon 16 March 2020.
- ^ Simonsen, J. L. (1947). The Terpenes. 1 (2nd bas.). Cambridge University Press. OCLC 477048261.[sayfa belirt]
- ^ Pakdel, H. (2001). "Production of DL-limonene by vacuum pyrolysis of used tires". Journal of Analytical and Applied Pyrolysis. 57: 91-107. doi:10.1016/S0165-2370(00)00136-4.
- ^ Karlberg, Ann-Therese; Magnusson, Kerstin; Nilsson, Ulrika (1992). "Air oxidation of D-limonene (the citrus solvent) creates potent allergens". Contact Dermatitis. 26 (5): 332-340. doi:10.1111/j.1600-0536.1992.tb00129.x. PMID 1395597.
- ^ Weitkamp, A. W. (1959). "I. The Action of Sulfur on Terpenes. The Limonene Sulfides". Journal of the American Chemical Society. 81 (13): 3430-3434. doi:10.1021/ja01522a069.