Magnezyum sülfat
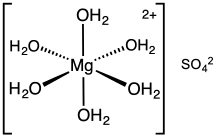 Magnesium sulfate hexahydrate
| |
 Anhydrous magnesium sulfate
| |
 Epsomite (Magnesium sulfate heptahydrate)
| |
| Adlandırmalar | |
|---|---|
Magnesium sulfate | |
Diğer adlar
| |
| Tanımlayıcılar | |
| |
3D model (JSmol)
|
|
| ChEBI |
|
| ChEMBL |
|
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.028.453 |
| EC Numarası |
|
| KEGG |
|
PubChem CID
|
|
| RTECS numarası |
|
| UNII |
|
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Molekül formülü | MgSO 4 |
| Molekül kütlesi |
|
| Görünüm | beyaz kristalin katı |
| Koku | kokusuz |
| Yoğunluk |
|
| Erime noktası |
|
| Çözünürlük (su içinde) |
|
Çözünürlük ürünü (Ksp)
|
738 (502 g/L) |
| Çözünürlük | |
| −50·10−6 cm3/mol | |
| Kırınım dizimi (nD) | 1.523 (monohydrate) 1.433 (heptahydrate) |
| Yapı | |
| monoclinic (hidrat) | |
| Farmakoloji | |
| A06AD04 (WHO) A12CC02 (DSÖ) B05XA05 (DSÖ) D11AX05 (DSÖ) V04CC02 (DSÖ) | |
| Tehlikeler | |
| NFPA 704 (yangın karosu) |
|
| Benzeyen bileşikler | |
Diğer katyonlar
|
|
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |

Magnezyum sülfat kimyasal formülü MgSO4 olan, magnezyum, kükürt ve oksijen ihtiva eden bir inorganik tuz. Genellikle heptahidrat (MgSO4·7H2O) formunda sülfat minerali olan Epsomit ya da diğer adıyla Epsom tuzu (İngiliz tuzu) hâlinde bulunur. Epsom adını İngiltere'deki bir yerleşim yerinden almıştır. Monohidrat formu olan kieseritin (MgSO4·H2O) 1970'lerin ortalarında genel küresel yıllık kullanımı 2.3 milyon ton civarındaydı ve bunun büyük çoğunluğu tarımda kullanılmıştır.[1]
Anhidröz magnezyum sülfat, bir kurutma maddesi olarak kullanılır. Susuz form higroskopik (kolaylıkla havadan su absorbe edebilen) olduğundan doğru bir şekilde tartılması zordur. Bu nedenle örneğin tıbbi preparatlar hazırlanırken çoğu zaman hidratlı formlar tercih edilir. İngiliz tuzu geleneksel banyo tuzlarının bir bileşeni olarak kullanılmıştır. Aynı zamanda bir güzellik ürünü olarak da kullanılabilir. Bahçıvanlar tarafından bitkileri geliştirmek için ve sporcular tarafından boğaz kaslarını rahatlatmak için kullanılır.[2] Bu kullanımlarının yanı sıra medikal alanda da yoğun olarak kullanılmaktadır.
Kaynakça
[değiştir | kaynağı değiştir]- ^ Industrial Inorganic Chemistry, Karl Heinz Büchel, Hans-Heinrich Moretto, Dietmar Werner, John Wiley & Sons, 2d edition, 2000, ISBN 9783527613335
- ^ "Quick Cures/Quack Cures: Is Epsom Worth Its Salt?". Wall Street Journal. 9 Nisan 2012. 6 Ekim 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Mart 2014.

