Emisyon spektrumu
Kimyasal elementlerin ya da kimyasal bileşiklerin emisyon spektrumu atom ya da moleküllerin yüksek enerji seviyesinden düşük enerji seviyesine geçişinden elde edilen elektromanyetik radyasyonun frekans spektrumudur. Yayılmış fotonun enerjisi iki enerji düzeyi arasındaki farka eşittir. Her atom için birçok mümkün geçişler vardır ve enerji düzeyleri arasındaki her geçiş spesifik enerji farkına sahiptir. Bu farklı geçişlerin toplamı, farklı ışınlar halinde gönderilmiş dalga boylarına ve emisyon spektrumunun düzenlenmesine neden olur. Her elementin emisyon spektrumu özeldir. Dahası, spektroskopi elementlerin madde içindeki bilinmeyen kompozisyonunu tespit etmek için kullanılabilir. Buna benzer olarak, moleküllerin emisyon spektrumları maddelerin kimyasal analizlerinde kullanılabilir.
Emisyon
[değiştir | kaynağı değiştir]Fizikte, emisyon, parçacığın yüksek enerjili kuantum mekanik düzeyden düşük foton emisyonuna doğru ışık üretimi sonucu çevrilmesi sürecidir. Elde edilen ışık sıklığı geçiş enerjisidir. Enerji muhafaza edilmek zorunda olduğundan, iki düzey arasındaki enerji farkı foton tarafından taşınan enerjiye eşit olacaktır. Geçişlerdeki enerji düzeyleri çok büyük mesafeli sıklıklarda emisyona neden olur. Örnek olarak, görülebilir ışık atom ve moleküllerde elektron eşleşmesi sonucunda flüoresans olarak adlandırılan olay sonucunda elde edilir. Buna karşın nükleer dönme geçişleri düşük enerjili radyo dalgaları yayarken, nükleer kabuk geçişleri yüksek enerjili gama ışınlarını yayabilir.
Herhangi bir cismin yayma gücü ışığın cisim tarafından ne kadar yayımlanmış olduğuyla belirlenir. Bu durum, Stefan-Boltzmann yasası aracılığıyla cisimlerin diğer özellikleriyle ilgili olabilir. Birçok cisim için, emisyon miktarları renk derecesi ve emisyon çizgilerinin görünüşüne neden olan dereceye ve cismin spektroskopik kompozisyonuna bağlı olarak çeşitlilik gösterir. Birçok dalga boyları üzerinde yapılan kesin ölçümler maddeyi emisyon spektroskopisi aracılığıyla belirlemeye olanak tanır.
Radyasyon emisyonu genel olarak yarı klasik kuantum mekaniğini kullanarak parçacığın enerji seviyesi ve aralıkları kuantum mekaniği tarafından belirlenir ve ışık salınım yapan sistemin doğal sıklığıyla rezonans halinde olduğu takdirde geçişleri yürüten elektrik alan gibi davranır olarak tanımlanır. Kuantum mekaniği problemi zamana bağlı pertürbasyon teorisi ile işlenmiş olup, Fermi’nin Altın Kuralı adı verilen genel bir sonuca varır. Çoğu durumda yarı klasik versiyonu daha kullanışlı olmaya devam etse de, tanım kuantum elektrodinamiği olarak değiştirildi.
Orijinler
[değiştir | kaynağı değiştir]Atomdaki elektronlar uyarıldığında, örneğin ısıtıldığında, oluşan enerji elektronları daha yüksek orbitallere iter. Elektronlar uyarılmış hallerini terk edip eski seviyelerine geri döndüklerinde enerji, foton halinde yeniden dışarı salınır. Foton’ un dalga boyu (ya da frekansı) iki seviye arasındaki enerji farkı ile belirlenir. Dışarı salınan fotonlar elementlerin spektrumlarını oluşturur. Bir elementin atomik emisyon spektrumunda sadece belirli renklerin görünmesi gerçeği, ışığın sadece belirli frekanslarının salındığı anlamına gelir. Bu frekansların her biri aşağıda belirtilen formül aracılığıyla enerjiye bağlıdır.
E fotonun enerjisi anlamına gelirken, V fotonun frekansı ve h ise Planck sabiti anlamına gelir. Bu sadece belirli miktarda enerjiye sahip fotonların atomlar tarafından salındığını neticelendirir. Atomik emisyon spektrumu prensibi, çeşitli renklerdeki neon işaretlerini, aynı zamanda kimyasal yanma testleri sonuçlarını (aşağıda açıklanmıştır) açıklar. Bir atomun yayabileceği ışığın frekansları elektronların bulunabileceği seviyelere bağlıdır. Elektronlar uyarıldıkları zaman daha yüksek enerjili seviyelere veya orbitallere taşınır. Elektron eski seviyesine döndüğü zaman, ışık yayılır.
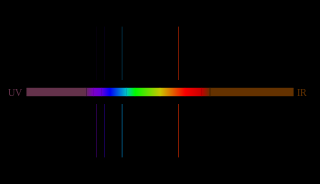
Yan taraftaki fotoğraf Hidrojen’ in görünür ışık emisyon spektrumunu gösterir. Eğer sadece bir Hidrojen atomu olsaydı, o anda sadece bir dalga boyu gözlemlenebilirdi. Örnek farklı başlangıç ve bitiş enerjilerine sahip birçok Hidrojen atomu içerdiği için, birçok muhtemel emisyonlar gözlemlenebilmiştir. Bu farklı kombinasyonlar, farklı dalga boyuna sahip eşzamanlı emisyonları doğurur.
Molekül Kaynaklı Radyasyonlar
[değiştir | kaynağı değiştir]Elektronik geçişler yukarıda tartışılmasına rağmen, bir molekülün enerjisi rotasyonel, titreşimsel ve vibronik (titreşimsel ve elektroniğin kombinesi) geçişler sayesinde de değişebilir. Bu enerji değişimleri spektral şeritler olarak da bilinen birbirine yakın birçok farklı spektral doğru gruplarının oluşumuna sebebiyet verir. Çözümlenmemiş spektrum şeritleri, spektral süreç halinde de görünebilir.
Emisyon Spektroskopisi
[değiştir | kaynağı değiştir]Işık, farklı dalga boylarının elektromanyetik radyasyonlarından meydana gelir. Dolayısıyla, elementler veya bileşimleri ateş üstünde veya elektrik kıvılcımı ile ısıtıldığında elementler ışık halinde enerji yayar. Bu ışığın spektroskop yardımı ile analizi bize süreksiz bir spektrum verir. Spektroskop ve spektrometre, farklı dalga boylarına sahip ışıkların bileşenlerine ayırılmasında kullanılan bir araçtır. Spektrum, doğru spektrumu adı verilen doğru demetinde görülür. Bu doğru spektrumuna, elementin içinde meydana geldiği için atomik spektrum da denir. Her bir elementin farklı bir atomik spektrumu vardır. Bir elementin atomları tarafından üretilen doğru spektrumları, bir atomun sadece belirli bir miktarda enerji yayabileceğini gösterir. Bu, sınırda bulunan elektronların herhangi bir miktarda değil, sadece belirli bir miktarda enerjiye sahip olabileceğini gösterir.

Emisyon spektroskopi, periyodik cetveldeki her element için farklı bir değere sahip olduğundan maddenin bileşimini kararlaştırmada kullanılabilir. Örneğin astronomik spektroskopi: elde edilen ışık analiz edilerek yıldızların tanımlanması. Bazı elementlerin emisyon spektrum karakterleri bu elementler ısıtıldığında açıkça çıplak gözle görülür. Örnek olarak, platin kablo stronsiyum nitrata batırıldığında ve aleve maruz bırakıldığında, stronsiyum nitrat atomları etrafa kırmızı renk yayar. Buna benzer olarak, bakır aleve maruz bırakıldığında, alev yeşil renge dönüşür. Bu belirli karakteristikler, elementlerin atomik emisyon spektrumu tarafından belirlenmesine olanak tanır. Yayılan ışıkların tamamı çıplak gözle fark edilemez, çünkü spektrum ayrıca ultraviyole ışınlar ve kızılötesi aydınlatma içerir. Emisyon, uyarılmış gaz direkt olarak spektroskoptan geçirildiği görüldüğünde oluşur.
Emisyon spektroskopisi, atomların ya da moleküllerin uyarılmış hallerinden alt enerji seviyesine geçişleri boyunca dışarı verilen fotonların dalga boylarını mercek altına alan spektroskopik tekniktir. Her bir karakteristik ayrık dalga boyları kümesini elektronik yapısına göre dışarı verir ve bu dalga boylarını gözlemleyerek, tipik örneklerin doğadaki güçlere özgü kompozisyonuna karar verilebilir. Emisyon spektroskopisi 19.yüzyılın sonlarına doğru geliştirilmiştir ve en sonunda kuantum mekaniklerine sebep olan atomla ilgili emisyon spektrumlarının teorik olarak açıklanması için efor gösterilmiştir.
Atomları uyarılmış duruma getirebilmek için birçok yol vardır. Elektromanyetik radyasyon ile etkileşim flüoresans spektroskopisinde, protonlar ya da Parçacık-Uyarılmış X-ışını Emisyonu ve elektronlar ya da Enerji-dağıtıcı X-ışını spektroskopisi ya da X-ışını flüoresans içerisindeki diğer ağır parçacıklarda kullanılır. En basit metodu tipik örneği, örnek atomlar arasındaki çarpışmalarla üretilen uyarımdan sonra yüksek derecede ısıtmaktır. Bu metot alev emisyon spektroskopisinde kullanılır ve ayrıca Anders Jonas Ångström tarafından 1850 yıllarında, ayrık emisyon çizgilerini keşfettiği zaman kullanılmıştır.
Emisyon çizgilerine belirli dereceye kadar enerji içeren enerji seviyelerindeki geçiş neden olsa da, sonlu genişliklere sahiptirler. Başka bir deyişle, birden fazla ışık dalga boyundan oluşmuşlardır. Bu spektral çizgi genişletmesi birçok farklı sebebiyetlere sahiptir.
Emisyon spektroskopisi sıklıkla görüş ile ilgili emisyon spektroskopisi olarak anılır.
Tarihçe
[değiştir | kaynağı değiştir]Sıcak gazların emisyon çizgileri ilk olarak Ångström tarafından keşfedildi ve daha sonrasında bu teknik David Alter, Gustav Kirchhoff ve Robert Bunsen tarafından geliştirildi.
Alev Emisyon Spektroskopisindeki Deneysel Teknikler
[değiştir | kaynağı değiştir]İlgili maddeleri içeren çözelti analiz edilmek için yakıcı içerisine konulmuştur ve alev içerisinde serpinti olarak dağılmıştır. Çözelti önce iyi bir şekilde bölünen, gaz atomlarının ve iyonlarının üretildiği alevin en sıcak bölgesine giden katı parçacıklarını terk ederek buharlaşmıştır. Elektronlar yukarıda tanımlandığı gibi uyarılmıştır. Monokromatörlerin bu basit belirlemenin yapılması için kullanılması yaygındır.
Basit bir düzeyde, alev emisyon spektroskopisi sadece alev ve metal tuz örnekleri kullanılarak gözlemlenebilir. Bu niteleyici analiz metoduna alev testi denir. Örnek olarak, alev içerisine yerleştirilmiş sodyum tuzu sodyum iyonlarından sarı renkte parlarken, stronsiyum iyonlarından dolayı kırmızı olarak parlar. Bakır kablo mavi renkte alev yaratırken, klorür mevcudiyeti CuCl’nin moleküler katkısından dolayı yeşil rengi verir.
Emisyon Katsayısı
[değiştir | kaynağı değiştir]Emisyon katsayısı fizikte hesaplanmış değerleri olan elektromanyetik kaynaktaki birim başına düşen güç çıkışıdır. Gazların emisyon katsayısı ışık dalga boyuna göre değişiklik gösterir. Ayrıca çevresel emisyonların kütle ile ölçülmesinde kullanılır.
Işığın Saçılması
[değiştir | kaynağı değiştir]Thomson saçılmasında yüklü parçacıklar özel durumlu ışık altında radyasyon açığa çıkarırlar. Parçacık sıradan atomsal elektron olabilir, yani emisyon katsayısı pratik uygulamalara sahip olabilir.
Eğer X dV dΩ dλ hacim elementi dV tarafından katı açısı dΩ içerisine λ ve λ+dλ dalga boyları arasındaki her birim zamana düşen enerji saçılmasıysa emisyon katsayısı X’tir.
Kendiliğinden Olan Emisyon
[değiştir | kaynağı değiştir]Foton tarafından yayımlanan ısıtılan madde, derecesi ve toplam güç radyasyonuyla ilişkili monokromatik emisyon katsayısına sahiptir. Buna bazen “Einstein Katsayısı” denir ve kuantum mekanik teorisinden sonuca varılır.
Enerji Spektrumu
[değiştir | kaynağı değiştir]Enerji spektrumu büyük parçacık topluluklarındaki enerji ayırımıdır. Dalga enerjisinin dalga sıklığına göre fonksiyonunun istatistiksel olarak gösterimidir ve spektral fonksiyonun deneyime dayalı olarak tahmin edicisidir.
Bu parçacıklar atomlar, fotonlar ya da basit parçacıkların akısı olabilir.
Schrödinger denklemleri ve sınır şartları kümesi öz değer problem olarak şekillenmiştir. E’nin mümkün değerine öz değer enerjisi denir. Dalga fonksiyonunun sıfırdan farklı çözümlerine öz değer durumu denir.
Elektromanyetik spektrum ayrıca elektromanyetik radyasyonun enerjiye bağlı dağılımı olarak gösterilebilir. Dalga boyu, sıklık ve enerji arasındaki ilişki:
Fizik alanındaki enerji spektrumuna örnek olarak okyanus kıyısındaki dalga kırılmasıdır. Bazı dalgaların diğerlerinden daha büyük olduğu gözlemlenebilir.[1]
Optik Spektroskopi ve Astrofizik ile İlgili Uygulama
[değiştir | kaynağı değiştir]Enerji spektrumları sıklıkla astrofizik ile ilgili spektroskopide kullanılır.
Çizilmiş büyüklük, enerji birimleri, dalga boyu kere her birimdeki dalga boyu enerjisidir ve bu yüzden kesin olarak her bir dalga boyunun miktar enerjisini gösterir. Her birim dalga boyundaki enerji ve tepe noktasındaki sıklık enerjisi, sıklık ve dalga boyu arasındaki karşılıklı ilişkiden dolayı önemli ölçüde değişik dalga boylarıdır.[2]
Kaynakça
[değiştir | kaynağı değiştir]- ^ Jump up to: a b Solar Energy Spectrum, Integrated Energy, Wavelengths of Light Colors and Visual Response of Eye
- Jump up ^ Allen, C.W. Astrophysical Quantities, 3rd edition, 1973, p. 109, 172.
Dış bağlantılar
[değiştir | kaynağı değiştir]- Atmosferik gazların emisyon spektrumları[ölü/kırık bağlantı]
- NIST Fiziksel Kaynak Data, Atomik Spektroskopi Data 3 Şubat 2010 tarihinde Wayback Machine sitesinde arşivlendi.
- Element Emisyon Spektrumunun NIST datasına Bağlı Olarak Renk Benzeşimi
- Hidrojen emisyon spektrumu
- Java Uygulamasının Emisyon Spektrumu 15 Şubat 2015 tarihinde Wayback Machine sitesinde arşivlendi.
- Chicago Üniversitesinden emisyon katsayısı ile ilgili astrofizik ders slaytları


