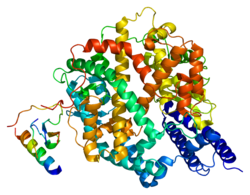
Anjiyotensin dönüştürücü enzim 2
Anjiyotensin dönüştürücü enzim 2 veya kısaca ACE2;[4] akciğerler, arterler, kalp, böbrekler ve bağırsaklardaki hücrelerin dış yüzeyine (hücre zarına) bağlı bir enzimdir.[5][6] ACE2, damar daraltıcı olan anjiyotensin II hormonunun anjiyotensin (1-7)'ye hidrolizini hızlandırarak kan basıncının düşmesini sağlar.[7][8][9] Ayrıca ACE2, bazı koronavirüsler için hücrelere giriş noktası görevini üstlenir. Enzimin insan versiyonuna hACE2 denir.[10]
ACE2, anjiyotensin-II miktarını azaltarak ve anjiyotensin (1-7)'yi arttırarak[11] anjiyotensin dönüştürücü enzimin (ACE) aktivitesine karşı koymaktadır. Bu sayede kardiyovasküler hastalıkların tedavisinde umut verici bir ilaç hedefi haline gelmiştir.[12][13]
Anjiyotensin dönüştürücü enzim 2, endotel hücreleri ve diğer hücrelerin yüzeyinde bulunan çinko içeren bir metaloenzimdir.[14] ACE2 proteini, bir N-terminalli peptidaz M2 alanı ve bir C-terminalli kollektrin renal amino asit taşıyıcı etki alanı içerir.
ACE2, akciğer ve diğer organ dokularındaki hücrelerin yüzeyinde enzimatik olarak aktif bir etki alanı bulunan, tek geçişli tip I membran proteinidir.[5] ACE2'nin hücre dışındaki etki alanı, şeddaz olarak bilinen diğer bir enzim vasıtasıyla transmembran etki alanından ayrılır. Devamında elde edilen çözülebilen protein, kan akışına salınarak idrar yoluyla atılmaktadır.[15][16]
Vücut içindeki konumu[değiştir | kaynağı değiştir]
ACE2'nin, birçok organda bulunduğu bilinmektedir. ACE2'nin bağlandığı yerler çoğunlukla, akciğer alveoler epitel hücrelerinin hücre zarı, ince bağırsağın enterositleri, arteriyel ve venöz endotel hücreleri ve birçok organdaki arteriyel düz kas hücreleridir. Ayrıca ACE2 mRNA'sı, serebral korteks, striatum, hipotalamus ve beyin sapında da bulunur.[17]
Görevi[değiştir | kaynağı değiştir]
ACE2'nin başlıca görevi, ACE'ye karşı bir denge vazifesi görmektir. ACE enzimi, anjiyotensin I hormonunu vazokonstriktör anjiyotensin II'ye ayırır. ACE2, sırayla karboksil terminal amino asit olan fenilalanini anjiyotensin II'den ayırır ve vazodilatör anjiyotensine (1-7) hidrolize eder.[14] Ayrıca ACE2, diğer birçok peptidi de ayırabilir ([des-Arg9]-bradykinin, apelin, nörotensin, dinorfin A ve grelin peptitleri). ACE2 ayrıca nötr amino asit taşıyıcısı SLC6A19'un membran çıkışını da düzenler ve Hartnup hastalığında rol oynar.[18]
[değiştir | kaynağı değiştir]
Transmembran proteini olan ACE2, hücreler için ana giriş noktası olarak görev alır ve çeşitli koronavirüs türlerinin hücre içine sızmasına neden olur HCoV-NL63;[4] SARS-CoV (SARS'a neden olan virüs)[19][20][21] ve SARS-CoV-2[22] (COVID-19'a neden olan virüs).[23][24][25] Daha detaylı anlatmak gerekirse SARS-CoV ve SARS-CoV2'nin uç kısımlarında yer alan S1 proteininin, hücre zarı üzerindeki ACE2'nin enzimatik alanına tutunduğunda, hem virüsün hem de enzimin, hücre içerisine endositoz yoluyla alınması gerçekleşir.[26][27] Ayrıca bu giriş işlemi ile virüsteki S proteini üretiminin, hücredeki serin proteazı TMPRSS2 tarafından yürütülmesine başlanır. Bu inhibisyon, potansiyel bir tedavi edici olarak görülüp halen üzerinde çalışmalar yürütülmektedir.[28]
Bu durum, hücrelerde ACE2 miktarını düşürmenin koronavirüsle mücadelede yardımcı olabileceği fikrine öncülük etmiştir. Buna antitez olarak ACE2'nin, vazodilatör anjiyotensin 1-7 üretimini artırarak virüs kaynaklı akciğer hasarına karşı koruyucu bir etkiye sahip olduğu da gösterilmiştir. Ayrıca, fareler üzerinde yapılan bazı çalışmalara göre, koronavirüsün uç proteininin ACE2 ile etkileşiminin, proteinin hücre içine doğru çekilmesi ve bozunması ile hücre zarında ACE2 seviyelerinde bir düşüşe neden olduğu ve bu nedenle akciğer hasarını arttırabileceği göstermiştir.[29][30]
Kemirgenler üzerinde yapılan çalışmalarda, yüksek kan basıncını tedavi etmek için kullanılan ACE inhibitörleri ve anjiyotensin reseptör blokerlerinin (ARB'lerin) her ikisinin de ACE2 miktarını arttırdığı ve bu nedenle koronavirüs enfeksiyonlarının şiddetini arttırabileceğini göstermiştir.[31][32] Ancak birçok profesyonel topluluk ve düzenleyici kurum ise, standart ACE inhibitörü ve ARB tedavisine devam edilmesini önermektedir.[33][34][35] 11 Temmuz 2012'de yayımlanan sistematik bir inceleme ve meta-analiz, "ACE inhibitörlerinin kullanımının, pnömoni riskinde kontrollere kıyasla % 34'lük bir azalma sağladığını buldu. Ayrıca, pnömoni riski yüksek olan, özellikle inme ve kalp yetmezliği olan hastalarda, ACE inhibitörleri ile tedavi edilmesi sayesinde pnömoni riskin de azaldığı görülmüştür. Ayrıca ACE inhibitörlerinin kullanımının, pnömoniye bağlı ölümleri azalttığı görülse de, ortaya çıkan sonuçların ortalama pnömoni riskinden daha az sağlam olduğunu ortaya koydu. ” [36]
Rekombinant ACE2 Proteini[değiştir | kaynağı değiştir]
Rekombinant ACE2 proteinini (rhACE2) isimli yeni bir tedavinin, akut akciğer hasarını giderdiği tahmin edilmekte ve pulmoner hemodinamiği iyileştirdiği görülmektedir.[netleştirme gerekli] Ayrıca lipopolisakkarit kaynaklı akut solunum sıkıntısı sendromu yaşayan domuz yavrularında da oksijen satürasyonunu arttırdığı gözlemlenmiştir.[37] İnsanlarda rhACE2'nin yarılanma ömrü yaklaşık 10 saattir ve 24 saatlik bir etki süresi bulunmaktadır. Etkinin başlangıcı ise 30 dakikadır. Çeşitli bulguların yol açıtığı sonuçlar üzerine, rhACE2'nin klasik renin-anjiyotensin sistem inhibitörlerine (RAS inhibitörlerine) toleransı olmayanlar ve kan dolaşımındaki anjiyotensin II'nin yükseldiği hastalıklarda umut verici bir ilaç olabileceğini düşündürmektedir.
İnfüze edilen rhACE2'nin kullanımı akut solunum sıkıntısı sendromunun tedavisi için klinik çalışmalarda değerlendirilmiştir.[38]
Ayrıca bakınız[değiştir | kaynağı değiştir]
Kaynakça[değiştir | kaynağı değiştir]
Bu madde önerilmeyen biçimde kaynaklandırılmıştır. (Bu şablonun nasıl ve ne zaman kaldırılması gerektiğini öğrenin) |
- ^ a b c GRCh38: Ensembl release 89: ENSG00000130234 - Ensembl, May 2017
- ^ "İnsan PubMed Başvurusu:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ "Fare PubMed Başvurusu:". National Center for Biotechnology Information, U.S. National Library of Medicine.
- ^ a b "Gene: ACE2, angiotensin I converting enzyme 2". National Center for Biotechnology Information (NCBI). U.S. National Library of Medicine. 28 Şubat 2020. 24 Aralık 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Nisan 2020.
- ^ a b "Tissue distribution of ACE2 protein, the functional receptor for SARS coronavirus. A first step in understanding SARS pathogenesis". The Journal of Pathology. 203 (2). Haziran 2004. ss. 631-7.
- ^ "A Novel Angiotensin-Converting Enzyme–Related Carboxypeptidase (ACE2) Converts Angiotensin I to Angiotensin 1-9". Circulation Research. 87 (5). 1 Eylül 2000. ss. e1-e9.
- ^ "ACE2 of the heart: From angiotensin I to angiotensin (1-7)". Cardiovascular Research. 73 (3). Şubat 2007. ss. 463-9.
- ^ "Angiotensin-Converting Enzyme 2 Metabolizes and Partially Inactivates Pyr-Apelin-13 and Apelin-17: Physiological Effects in the Cardiovascular System". Hypertension. 68 (2). Ağustos 2016. ss. 365-77.
- ^ "A novel angiotensin-converting enzyme-related carboxypeptidase (ACE2) converts angiotensin I to angiotensin 1-9". Circulation Research. 87 (5). Eylül 2000. ss. E1-9.
- ^ Kasmi Y, Khataby K, Souiri A (2019). "Coronaviridae: 100.000 Years of Emergence and Reemergence". Ennaji MM (Ed.). Emerging and Reemerging Viral Pathogens. Volume 1: Fundamental and Basic Virology Aspects of Human, Animal and Plant Pathogens. Elsevier. s. 135. ISBN 978-0-12-819400-3.
- ^ "Angiotensin-converting enzyme 2 as a therapeutic target for heart failure". Current Heart Failure Reports. 11 (1). Springer Science and Business Media LLC. Mart 2014. ss. 58-63.
The discovery of ACE2 and its role in counteracting the effect of Ang-II through Ang(1-7) formation...An imbalance in ACE2/Ang-(1-7) and ACE/Ang-II axes is critical in the development of cardiovascular diseases. The central role of ACE2, therefore, appears to counter ACE activity by reducing Ang-II bioavailability and increasing Ang(1-7) formation...The use of RAS-modulating agents and molecules as novel therapeutic agents in hypertension and cardiovascular therapeutic research.
- ^ "Angiotensin-converting enzyme 2 as a therapeutic target for heart failure". Current Heart Failure Reports. 11 (1). Springer Science and Business Media LLC. Mart 2014. ss. 58-63.
Studies with recombinant human ACE2 (rhACE2) have shown beneficial cardiac effects [18, 36]. rhACE2 has anti-fibrotic properties and can attenuate effect on systolic and diastolic dysfunction, presumably via Ang-II inhibition .
- ^ "Angiotensin II and angiotensin 1-7: which is their role in atrial fibrillation?". Heart Failure Reviews. 25 (2). Springer Science and Business Media LLC. Mart 2020. ss. 367-380.
the possibility of using the A1-7 or ACE2 analogues, to enlarge current therapeutic options for AF, may represent an important field of research.
- ^ a b Turner AJ (2015). "Chapter 25: ACE2 Cell Biology, Regulation, and Physiological Functions". Unger T, Ulrike M, Steckelings UM, dos Santos RA (Ed.). The Protective Arm of the Renin Angiotensin System (RAS): Functional Aspects and Therapeutic Implications. Academic Press. ss. 185-189. doi:10.1016/B978-0-12-801364-9.00025-0. ISBN 978-0-12-801364-9.
- ^ "Tumor necrosis factor-alpha convertase (ADAM17) mediates regulated ectodomain shedding of the severe-acute respiratory syndrome-coronavirus (SARS-CoV) receptor, angiotensin-converting enzyme-2 (ACE2)". The Journal of Biological Chemistry. 280 (34). Ağustos 2005. ss. 30113-9.
- ^ "Angiotensin II induced proteolytic cleavage of myocardial ACE2 is mediated by TACE/ADAM-17: a positive feedback mechanism in the RAS". Journal of Molecular and Cellular Cardiology. Cilt 66. Ocak 2014. ss. 167-76.
- ^ Kabbani (1 Nisan 2020). "Does COVID19 infect the brain? If so, smokers might be at a higher risk". Molecular Pharmacology. s. 1-7.
- ^ "Multiple functions of angiotensin-converting enzyme 2 and its relevance in cardiovascular diseases". Circulation Journal : Official Journal of the Japanese Circulation Society. 77 (2). 2013. ss. 301-8.
- ^ "Coronaviruses: an overview of their replication and pathogenesis". Methods in Molecular Biology. Cilt 1282. Springer New York. 2015. ss. 1-23.
Many α-coronaviruses utilize aminopeptidase N (APN) as their receptor, SARS-CoV and HCoV-NL63 use angiotensin-converting enzyme 2 (ACE2) as their receptor, MHV enters through CEACAM1, and the recently identified MERS-CoV binds to dipeptidyl-peptidase 4 (DPP4) to gain entry into human cells (See Table 1 for a list of known CoV receptors).
- ^ "Receptor recognition and cross-species infections of SARS coronavirus". Antiviral Research. 100 (1). Ekim 2013. ss. 246-54.
- ^ "A crucial role of angiotensin converting enzyme 2 (ACE2) in SARS coronavirus-induced lung injury". Nature Medicine. 11 (8). Ağustos 2005. ss. 875-9.
- ^ "What are the official names of the disease and the virus that causes it?". Q&A on coronaviruses. World Health Organization. 5 Mart 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 Şubat 2020.
- ^ "A pneumonia outbreak associated with a new coronavirus of probable bat origin". Nature. 579 (7798). Mart 2020. ss. 270-273.
- ^ "Evolution of the novel coronavirus from the ongoing Wuhan outbreak and modeling of its spike protein for risk of human transmission". Science China. Life Sciences. 63 (3). Mart 2020. ss. 457-460.
- ^ "COVID-19 Vaccine Will Close in on the Spikes". DNA Science Blog. Public Library of Science. 20 Şubat 2020. 22 Şubat 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 22 Şubat 2020.
- ^ "SARS coronavirus entry into host cells through a novel clathrin- and caveolae-independent endocytic pathway". Cell Research. 18 (2). Şubat 2008. ss. 290-301.
- ^ "Physiological and molecular triggers for SARS-CoV membrane fusion and entry into host cells". Virology. Cilt 517. Nisan 2018. ss. 3-8.
- ^ Akhmerov Akbarshakh. "COVID-19 and the Heart". Circulation Research. 0 (0). 6 Ekim 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Nisan 2020.
- ^ "The discovery of angiotensin-converting enzyme 2 and its role in acute lung injury in mice". Experimental Physiology. 93 (5). Mayıs 2008. ss. 543-8.
- ^ "Pulmonary Angiotensin-Converting Enzyme 2 (ACE2) and Inflammatory Lung Disease". Shock. 46 (3). Augusta, Ga. Eylül 2016. ss. 239-48.
Once SARS-CoV binds to its receptor, the abundance on the cell surface, mRNA expression and the enzymatic activity of ACE2 are significantly reduced. ... These effects are, in part, due to enhanced shedding/internalizing processes. ... The spike protein binds to ACE2 and subsequently down regulated ACE2 protein expression and resulted in worsened acid aspiration pneumonia
- ^ "Good ACE, bad ACE do battle in lung injury, SARS". Nature Medicine. 11 (8). Ağustos 2005. ss. 821-2.
- ^ "Hypothesis: angiotensin-converting enzyme inhibitors and angiotensin receptor blockers may increase the risk of severe COVID-19". Journal of Travel Medicine. Mart 2020.
- ^ "Position Statement of the ESC Council on Hypertension on ACE-Inhibitors and Angiotensin Receptor Blockers". European Society of Cardiology (ESC). 13 Mart 2020. 14 Mart 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Nisan 2020. Diğer özet – Medscape.
- ^ "EMA advises continued use of medicines for hypertension, heart or kidney disease during COVID-19 pandemic". European Medicines Agency (EMA). 27 Mart 2020. 28 Mart 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Nisan 2020. Diğer özet – Medscape.
- ^ "HFSA/ACC/AHA Statement Addresses Concerns Re: Using RAAS Antagonists in COVID-19". American College of Cardiology (ACC). 27 Mart 2020. 21 Mart 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Nisan 2020. Diğer özet – Medscape.
- ^ "Risk of pneumonia associated with use of angiotensin converting enzyme inhibitors and angiotensin receptor blockers: systematic review and meta-analysis". BMJ. 345 (jul11 1). Temmuz 2012. ss. e4260.
Our results suggest an important role of ACE inhibitors, but not ARBs, in reducing the risk of pneumonia. These data may discourage the withdrawal of ACE inhibitors in some patients with tolerable adverse events (namely, cough) who are at particularly high risk of pneumonia. ACE inhibitors also lowered the risk of pneumonia related mortality, mainly in patients with established disease, but the robustness of the evidence was weaker.
- ^ Colafella KM, Uijl E, Danser J (2019). "Interference With the Renin–Angiotensin System (RAS): Classical Inhibitors and Novel Approaches". Encyclopedia of Endocrine Diseases. Elsevier. ss. 523-530. doi:10.1016/b978-0-12-801238-3.65341-2. ISBN 978-0-12-812200-6.
- ^ "A pilot clinical trial of recombinant human angiotensin-converting enzyme 2 in acute respiratory distress syndrome". Critical Care. 21 (1). Eylül 2017. s. 234.