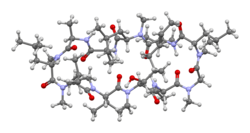
Siklosporin
 | |
 | |
| Klinik verisi | |
|---|---|
| Telaffuz | /ˌsaɪkləˈspɔːrɪn/[1] |
| Ticari adlar | Neoral, Sandimmune, Restasis, diğer |
| Diğer adlar | siklosporin A,[2], cyclosporine (USAN ABD) |
| AHFS/Drugs.com | Monografi |
| MedlinePlus | a601207 |
| Lisans veri |
|
| Gebelik kategorisi |
|
| Uygulama yolu | ağız yoluyla, intravenöz (IV), göz damlası |
| İlaç sınıfı | Kalsinörin inhibitörü |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum |
|
| Farmakokinetik veri | |
| Biyoyararlanım | değişken |
| Metabolizma | Karaciğer CYP3A4 |
| Eliminasyon yarı ömrü | değişken (yaklaşık 24 saat) |
| Boşaltım | Safra yolu |
| Tanımlayıcılar | |
| |
| CAS Numarası | |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Bilgi Paneli (EPA) | |
| ECHA Bilgi Kartı | 100.119.569 |
| Kimyasal ve fiziksel veriler | |
| Formül | C62H111N11O12 |
| Mol kütlesi | 1 202.635 g·mol−1 |
| 3D model (JSmol) | |
| |
| |
| Siklosporin | |
|---|---|
| Tanımlayıcılar | |
| Sembol | Yok |
| OPM üst ailesi | 94 |
| OPM proteini | 1cwa |
Siklosporin, immünsupresif ilaç olarak kullanılan bir kalsinörin inhibitörüdür. Romatoid artrit, sedef hastalığı, Crohn hastalığı, nefrotik sendrom ve organ nakillerinde reddi önlemek için oral veya intravenöz olarak alınır.[10][11] Ayrıca keratokonjonktivitis sicca için göz damlası olarak kullanılır.[12]
Yaygın yan etkiler arasında yüksek tansiyon, baş ağrısı, böbrek sorunları, kıllanma artışı ve kusma yer alır.[11] Diğer ciddi yan etkiler arasında enfeksiyon riskinde artış, karaciğer sorunları ve lenfoma riskinde artış yer alır.[11] Yan etki riskini azaltmak için ilacın kan seviyeleri kontrol edilmelidir.[11] Hamilelik sırasında kullanım erken doğumla sonuçlanabilir; ancak siklosporinin doğum kusurlarına neden olduğu görülmemektedir.[13]
Siklosporinin lenfositlerin işlevini azaltarak çalıştığı düşünülmektedir.[11] Bunu, kalsinörinin fosfataz aktivitesini bloke etmek için siklofilin ile bir kompleks oluşturarak yapar ve bu da T-lenfositler tarafından inflamatuar sitokinlerin üretimini azaltır.[14]
Siklosporin 1971 yılında Tolypocladium inflatum mantarından izole edilmiş ve 1983 yılında tıbbi kullanıma girmiştir.[15] Dünya Sağlık Örgütünün Temel İlaçlar Listesi'nde yer almaktadır.[16][17] 2020 yılında, 2 milyondan fazla reçete ile Amerika Birleşik Devletleri'nde en sık reçete edilen 212. ilaç olmuştur.[18][19] Jenerik bir ilaç olarak mevcuttur.[20]
Tıbbi kullanım[değiştir | kaynağı değiştir]
Siklosporin, kemik iliği naklinde graft-versus-host hastalığını tedavi etmek ve önlemek ve böbrek, kalp ve karaciğer nakillerinin reddini önlemek için endikedir.[5][6] Ayrıca ABD'de romatoid artrit ve sedef hastalığı, adenoviral keratokonjonktivit sonrası kalıcı nummular keratit tedavisi[5][21] ve Sjögren sendromu ve meibomian bezi disfonksiyonunun neden olduğu göz kuruluğunun tedavisi için göz damlası olarak onaylanmıştır.[7]
Bu endikasyonlara ek olarak, siklosporin şiddetli atopik dermatit,[22] Kimura hastalığı, piyoderma gangrenozum, kronik kurdeşen, akut sistemik mastositoz ve enfektif olmayan nedenli arka veya orta üveitte de kullanılır.[kaynak belirtilmeli] Seyrek de olsa şiddetli romatoid artrit ve ilgili hastalıklarda da kullanılır.[23][kaynak belirtilmeli]
Siklosporin ayrıca steroid tedavisine yanıt vermeyen akut şiddetli ülseratif kolit ve kurdeşeni olan kişilerde de kullanılmıştır.[24]
Yan etkiler[değiştir | kaynağı değiştir]
Siklosporinin yan etkileri arasında dişeti büyümesi, kıllanma artışı, kasılmalar, peptik ülser, pankreatit, ateş, kusma, ishal, konfüzyon, kolesterol artışı, nefes almada güçlük, uyuşma ve karıncalanma (özellikle dudaklarda), kaşıntı, yüksek tansiyon, potasyum tutulması (muhtemelen hiperkalemiye yol açar), böbrek ve karaciğer fonksiyon bozukluğu,[25] parmak uçlarında yanma hissi ve fırsatçı mantar ve viral enfeksiyonlara karşı artan hassasiyet sayılabilir. Siklosporin böbreklerde vazokonstriksiyona neden olarak ve sodyum geri emilimini artırarak hipertansiyona neden olur. Kan basıncındaki artış kardiyovasküler olaylara neden olabilir; bu nedenle uzun süreli tedavi gerektiren kişiler için en düşük etkili dozun kullanılması önerilir.[26]
Böbrek naklinden sonra siklosporin kullanımı, kanda ürik asit seviyelerinin artması ve bazı durumlarda gut hastalığı ile ilişkilidir.[27] Bunun nedeni, ürik asit retansiyonuna yol açan glomerüler filtrasyon hızındaki azalmadır.[kaynak belirtilmeli] Alternatif olarak azatioprin kullanımının gut artriti insidansını azalttığı gösterilmiştir.[kaynak belirtilmeli]
Siklosporin, özellikle skuamöz hücreli cilt kanseri ve non-Hodgkin lenfomaya yol açan bir IARC Grup 1 kanserojen (yani insanlarda kanserojen olduğuna dair yeterli kanıt vardır) olarak listelenmiştir.[28][29]
Farmakoloji[değiştir | kaynağı değiştir]
Aksiyon mekanizması[değiştir | kaynağı değiştir]
Siklosporinin ana etkisi T hücrelerinin aktivitesini düşürmektir; bunu kalsinörin-fosfataz yolağındaki kalsinörini inhibe ederek ve mitokondriyal geçirgenlik geçiş gözeneğinin açılmasını önleyerek yapar. Siklosporin, lenfositlerin, özellikle de T hücrelerinin sitozolik protein siklofilinine (immünofilin) bağlanır. Bu siklosporin-siklofilin kompleksi, normalde interlökin 2'nin transkripsiyonunu aktive etmekten sorumlu olan kalsinörini inhibe eder. T hücrelerinde, T hücre reseptörünün aktivasyonu normalde kalsinörini aktive etmek için kalmodulin yoluyla hareket eden hücre içi kalsiyumu artırır. Kalsinörin daha sonra transkripsiyon faktörü NF-AT'yi (aktive T-hücrelerinin nükleer faktörü) defosforile eder, bu da T-hücresi çekirdeğine hareket eder ve IL-2 ve ilgili sitokinler için genlerin transkripsiyonunu artırır.[14] Siklosporin, NF-AT'nin defosforilasyonunu önleyerek efektör T-hücre fonksiyonunun azalmasına yol açar;[30][31][32][33] sitostatik aktiviteyi etkilemez.[kaynak belirtilmeli]
Siklosporin ayrıca mitokondriyal geçirgenlik geçiş porunun (MPTP) bir parçasını oluşturan siklofilin D proteinine bağlanarak MPTP'nin açılmasını önler.[31][34] MPTP kalp kası hücrelerinin mitokondriyal membranında bulunur. MPTP açılması, iç mitokondriyal membran geçirgenliğinde ani bir değişiklik anlamına gelir ve protonların ve ~1,5 kDa'ya kadar büyüklükteki diğer iyonların ve çözünen maddelerin iç membrandan geçmesine izin verir. Bu geçirgenlik değişikliği, hücre ölümüne yol açan hücresel bir felaket olarak kabul edilir.[35][36] Bununla birlikte, kısa mitokondriyal geçirgenlik geçiş poru açıklıkları, sağlıklı mitokondriyal homeostazın sürdürülmesinde önemli bir fizyolojik rol oynar.[37]
Farmakokinetik[değiştir | kaynağı değiştir]
Siklosporin 11 amino asitten oluşan siklik bir peptittir; doğada nadiren rastlanan tek bir D-amino asit içerir. Çoğu peptidin aksine, siklosporin ribozomlar tarafından sentezlenmez.[38]
Siklosporin, alımından sonra insanlarda ve hayvanlarda yüksek oranda metabolize olur. Siklosporin B, C, D, E, H ve L'yi içeren metabolitler,[39] siklosporinin immünosupresan aktivitesinin %10'undan daha azına sahiptir ve daha yüksek böbrek toksisitesi ile ilişkilidir.[40] Bireysel siklosporin metabolitleri izole edilmiş ve karakterize edilmiştir ancak kapsamlı olarak çalışılmamıştır.[kaynak belirtilmeli]
Biyosentez[değiştir | kaynağı değiştir]
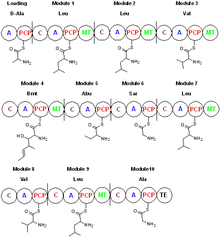
Siklosporin, nonribozomal bir peptit sentetaz olan siklosporin sentetaz tarafından sentezlenir.[41] Enzim bir adenililasyon alanı, bir tiyolasyon alanı, bir yoğunlaşma alanı ve bir N-metiltransferaz alanı içerir. Adenililasyon alanı substrat tanıma ve aktivasyonundan sorumluyken, tiyolasyon alanı adenillenmiş amino asitleri fosfopantetine kovalent olarak bağlar ve kondensasyon alanı peptit zincirini uzatır. Siklosporin sentetaz substratları arasında L-valin, L-lösin, L-alanin, glisin, 2-aminobütirik asit, 4-metiltreonin ve biyosentetik süreçte başlangıç amino asidi olan D-alanin bulunur.[42] Adenilasyon alanı ile siklosporin sentetaz, açil-adenillenmiş amino asitleri üretir, ardından amino asidi bir tiyoester bağı yoluyla fosfopantetine kovalent olarak bağlar. Amino asit substratlarının bazıları S-adenozil metiyonin tarafından N-metillenir. Siklizasyon adımı siklosporini enzimden serbest bırakır.[43] D-Ala ve butenil-metil-L-treonin (Bmt) gibi amino asitler siklosporin sentetazın diğer enzimlerin etkisini gerektirdiğini gösterir. L-Ala'nın alanin rasemaz tarafından D-Ala'ya rasemizasyonu piridoksal fosfata bağlıdır. Bütenil-metil-L-treonin oluşumu, başlangıç malzemesi olarak asetat/malonat kullanan bir Bmt poliketit sentaz tarafından gerçekleştirilir.[44]
Gen kümesi[değiştir | kaynağı değiştir]
Şu anda siklosporinin seri üretimi için kullanılan tür olan Tolypocladium inflatum, 12 gen kümesi halinde düzenlenmiş biyosentetik genlere sahiptir. Bu 12 genden SimA (Q09164) siklosporin sentetaz, SimB (CAA02484.1) alanin rasemaz ve SimG (ATQ39432.1'e benzer) poliketid sentazdır.[45] Bu genler aktif bir retrotranspozon ile ilişkilidir.[46] Bu diziler GenBank ve diğer veri tabanlarında zayıf bir şekilde tanımlanmış olsa da, siklosporin üreten Beauveria felina (veya Amphichorda ~) için %90 benzer diziler bulunabilir.[47] SimB'nin aynı organizmada, düşük özgüllükleri sayesinde farklı ancak örtüşen işlevlere sahip iki paralogu vardır.[48]
Tarihçe[değiştir | kaynağı değiştir]
1970 yılında İsviçre'nin Basel kentindeki Sandoz (şimdiki adıyla Novartis) çalışanları tarafından Norveç ve ABD'nin Wisconsin eyaletinden alınan toprak örneklerinden yeni mantar türleri izole edildi. Her iki suş da siklosporin adı verilen bir doğal ürün ailesi üretti. Bu mantarlardan elde edilen özütlerden antifungal aktiviteye sahip iki ilgili bileşen izole edilmiştir. Norveç suşu Tolypocladium inflatum Gams, daha sonra siklosporinin büyük ölçekli fermantasyonu için kullanılmıştır.[49]
Doğal ürün siklosporinin bağışıklık sistemini baskılayıcı etkisi 31 Ocak 1972'de[50] Sandoz'da Hartmann F. Stähelin tarafından tasarlanan ve uygulanan bağışıklık sisteminin baskılanmasına ilişkin bir tarama testinde keşfedilmiştir.[49][51] Siklosporinin kimyasal yapısı 1976 yılında yine Sandoz'da belirlenmiştir.[52][53] İlaç adayı siklosporinin organ reddini önlemedeki başarısı Cambridge Üniversitesinde R.Y. Calne ve meslektaşları tarafından böbrek nakillerinde[54] ve Pittsburgh Üniversitesi Hastanesinde Thomas Starzl tarafından gerçekleştirilen karaciğer nakillerinde gösterilmiştir. İlk hasta 9 Mart 1980 tarihinde 28 yaşında bir kadındı.[55] Amerika Birleşik Devletleri'nde Gıda ve İlaç Dairesi (FDA) 1983 yılında siklosporini klinik kullanım için onayladı.[56][57][58][59]
Toplum ve kültür[değiştir | kaynağı değiştir]
Mevcut formlar[değiştir | kaynağı değiştir]
Siklosporin suda çok az çözünürlük gösterir ve sonuç olarak ilacın oral uygulama ve enjeksiyon için süspansiyon ve emülsiyon formları geliştirilmiştir. Siklosporin ilk olarak Sandoz (günümüzde Novartis) tarafından Sandimmune markası altında yumuşak jelatin kapsüller, oral solüsyon ve intravenöz uygulama için bir formülasyon olarak pazara sunulmuştur. Bunların hepsi sulu olmayan bileşimlerdir.[6] Daha yeni bir mikroemülsiyon,[60] oral yoldan uygulanan bir formülasyon olan Neoral,[5] bir çözelti ve yumuşak jelatin kapsüller olarak mevcuttur. Neoral'ın bileşimleri su ile temas halinde mikroemülsiyonlar oluşturacak şekilde tasarlanmıştır.[61][62]
Jenerik siklosporin preparatları, Cicloral (Sandoz/Hexal tarafından), Gengraf (Abbott tarafından) ve Deximune (Dexcel Pharma tarafından) dahil olmak üzere çeşitli ticari isimler altında pazarlanmaktadır. 2002 yılından bu yana, göz kuruluğunun neden olduğu iltihabı tedavi etmek için topikal bir siklosporin emülsiyonu Restasis ticari adı altında pazarlanmaktadır.[7] Ikervis %0,1 konsantrasyona sahip benzer bir formülasyondur.[63] İnhale siklosporin formülasyonları klinik geliştirme aşamasındadır ve propilen glikol ve lipozom dispersiyonları içinde bir çözelti içerir.[64][65]
Araştırma[değiştir | kaynağı değiştir]
Nöroproteksiyon[değiştir | kaynağı değiştir]
Siklosporin şu anda Avrupa'da travmatik beyin hasarında nöronal hücresel hasarı ve reperfüzyon hasarını (faz III) iyileştirme yeteneğini belirlemek için faz II/III (uyarlanabilir) bir klinik çalışmadadır. Bu çok merkezli çalışma, NeuroVive Pharma ve Avrupa Beyin Hasarı Konsorsiyumu tarafından NeuroVive'ın NeuroSTAT (kardiyoproteksiyon ticari adıyla CicloMulsion olarak da bilinir) adlı siklosporin formülasyonu kullanılarak düzenlenmektedir. Bu formülasyonda kremofor ve etanol yerine bir lipid emülsiyon bazı kullanılmaktadır.[66] NeuroSTAT bir faz I çalışmasında Sandimmune ile karşılaştırılmış ve biyoeşdeğer olduğu bulunmuştur. Bu çalışmada NeuroSTAT, kremofor ve etanol bazlı ürünlerde bulunan anafilaktik ve aşırı duyarlılık reaksiyonlarını göstermemiştir.[67]
Siklosporin, travmatik beyin hasarı gibi durumlarda olası bir nöroprotektif ajan olarak araştırılmış ve hayvan deneylerinde yaralanmayla ilişkili beyin hasarını azalttığı gösterilmiştir.[68] Siklosporin, kafa travması ve nörodejeneratif hastalıklarla ilişkili hasarın çoğuna neden olduğu tespit edilen mitokondriyal geçirgenlik geçiş porunun oluşumunu engeller. Siklosporinin nöroprotektif özellikleri ilk olarak 1990'ların başında iki araştırmacı (Eskil Elmér ve Hiroyuki Uchino) hücre nakli üzerine deneyler yaparken keşfedilmiştir. İstenmeyen bir bulgu, siklosporin A'nın kan-beyin bariyerini geçtiğinde güçlü bir şekilde nöroprotektif olduğuydu.[69] Aynı mitokondriyal yıkım süreci, MPT gözeneğinin açılması yoluyla travmatik beyin hasarlarını çok daha kötü hale getirmektedir.[70]
Kalp hastalığı[değiştir | kaynağı değiştir]
Siklosporin deneysel olarak kardiyak hipertrofiyi (hücre hacminde artış) tedavi etmek için kullanılmıştır.[31][71]
Mitokondriyal geçirgenlik geçiş porunun (MPTP) uygunsuz şekilde açılması, iskemi (dokuya kan akışının kısıtlanması)[31] ve reperfüzyon hasarında (iskemi sonrasında dokuya kan akışı geri döndüğünde meydana gelen hasar),[31] miyokard enfarktüsü (kalp krizi) sonrasında[32] ve mitokondriyal DNA polimerazda mutasyonlar meydana geldiğinde ortaya çıkar.[31] Kalp, kasılma döngü hızlarını artırmak için hücre içi Ca+2'yi artırarak hastalık durumunu telafi etmeye çalışır.[34] Konstitütif olarak yüksek mitokondriyal Ca+2 uygunsuz MPTP açılmasına neden olarak kardiyak fonksiyon aralığında bir azalmaya yol açar ve sorunu telafi etme girişimi olarak kardiyak hipertrofiye yol açar.[32][34]
Siklosporin A'nın kardiyak miyositleri birçok şekilde etkileyerek kardiyak hipertrofiyi azalttığı gösterilmiştir. Siklosporin A, MPTP'nin açılmasını engellemek için siklofilin D'ye bağlanır ve böylece programlanmış hücre ölümüne neden olabilecek protein sitokrom C salınımını azaltır.[31][34][72] CypD, MPTP içinde kapı görevi gören bir proteindir; siklosporin A tarafından bağlanması MPTP'nin uygunsuz açılma miktarını azaltır, bu da intramitokondriyal Ca+2'yi azaltır.[34] İntramitokondriyal Ca+2'nin azaltılması, orijinal kardiyak yanıtta neden olunan kardiyak hipertrofinin tersine çevrilmesini sağlar.[34] Sitokrom C salınımının azaltılması, yaralanma ve hastalık sırasında hücre ölümünün azalmasına neden olmuştur.[31] Siklosporin A ayrıca fosfataz kalsinörin yolunu (14) da inhibe eder.[31][32][73] Bu yolun inhibisyonunun miyokardiyal hipertrofiyi azalttığı gösterilmiştir.[32][71][73]
Veterinerlikte kullanım[değiştir | kaynağı değiştir]
İlaç, Amerika Birleşik Devletleri'nde köpeklerde atopik dermatit tedavisi için onaylanmıştır.[74] İlacın insan formundan farklı olarak, köpeklerde kullanılan daha düşük dozlar, ilacın bir immünomodülatör olarak hareket ettiği ve insanlara göre daha az yan etkiye sahip olduğu anlamına gelir. Bu ürünü kullanmanın faydaları arasında, durumu kontrol altına almak için eşzamanlı tedavilere olan ihtiyacın azalması yer almaktadır. Merck'in bir parçası olan Intervet tarafından üretilen Optimmune adlı köpekler için oftalmik bir merhem olarak mevcuttur. Ayrıca sebasöz adenit (yağ bezlerine karşı bağışıklık yanıtı), pemfigus foliaceus (otoimmün kabarcıklı deri hastalığı), inflamatuar bağırsak hastalığı, anal furunküloz (anal iltihaplı hastalık) ve myastenia gravis (nöromüsküler bir hastalık) tedavisinde de kullanılır.[74][75]
Kaynakça[değiştir | kaynağı değiştir]
- ^ "cyclosporin". Dictionary.com Unabridged. Random House. n.d. 18 Kasım 2010 tarihinde kaynağından arşivlendi. Erişim tarihi: 13 Temmuz 2011.
- ^ Laupacis A, Keown PA, Ulan RA, McKenzie N, Stiller CR (May 1982). "Cyclosporin A: a powerful immunosuppressant". Canadian Medical Association Journal. 126 (9): 1041-6. PMC 1863293 $2. PMID 7074504.
- ^ "Search Page - Drug and Health Product Register". 23 Ekim 2014. 7 Haziran 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Haziran 2022.
- ^ "Search Page - Drug and Health Product Register". 23 Ekim 2014. 7 Haziran 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Haziran 2022.
- ^ a b c d "Neoral- cyclosporine capsule, liquid filled Neoral- cyclosporine solution". DailyMed. 5 Temmuz 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Şubat 2022.
- ^ a b c "Sandimmune- cyclosporine capsule, liquid filled Sandimmune- cyclosporine injection Sandimmune- cyclosporine solution". DailyMed. 21 Nisan 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Şubat 2022.
- ^ a b c "Restasis- cyclosporine emulsion". DailyMed. 30 Mart 2014 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Şubat 2022.
- ^ "Vevye- cyclosporine ophthalmic solution solution/ drops". DailyMed. 26 Mayıs 2023. 29 Ağustos 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 29 Ağustos 2023.
- ^ "Ikervis". European Medicines Agency. 17 Eylül 2018. 13 Ağustos 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 27 Şubat 2023.
- ^ World Health Organization (2009). Stuart MC, Kouimtzi M, Hill SR (Ed.). WHO Model Formulary 2008. World Health Organization. s. 221. hdl:10665/44053. ISBN 9789241547659.
- ^ a b c d e "Cyclosporine". The American Society of Health-System Pharmacists. 17 Ekim 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 8 Aralık 2016.
- ^ "Cyclosporine eent". The American Society of Health-System Pharmacists. 13 Ocak 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 8 Aralık 2016.
- ^ "Cyclosporine Use During Pregnancy". Drugs.com. 14 Eylül 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 20 Aralık 2016.
- ^ a b Matsuda S, Koyasu S (May 2000). "Mechanisms of action of cyclosporine" (PDF). Immunopharmacology. 47 (2–3): 119-25. doi:10.1016/S0162-3109(00)00192-2. PMID 10878286. 11 Ağustos 2017 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 4 Mart 2018.
- ^ Watts R, Clunie G, Hall F, Marshall T (2009). Rheumatology. Oxford University Press. s. 558. ISBN 978-0-19-922999-4. 5 Kasım 2017 tarihinde kaynağından arşivlendi.
- ^ World Health Organization (2019). World Health Organization model list of essential medicines: 21st list 2019. Cenevre: World Health Organization. hdl:10665/325771. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ World Health Organization (2021). World Health Organization model list of essential medicines: 22nd list (2021). Cenevre: World Health Organization. hdl:10665/345533. WHO/MHP/HPS/EML/2021.02.
- ^ "The Top 300 of 2020". ClinCalc. 12 Şubat 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Ekim 2022.
- ^ "Cyclosporine - Drug Usage Statistics". ClinCalc. 8 Temmuz 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Ekim 2022.
- ^ "FDA Approves First Generic of Restasis". U.S. Food and Drug Administration (FDA) (Basın açıklaması). 2 Şubat 2022. 2 Şubat 2022 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Şubat 2022.
- ^ Reinhard T (2000). "Lokales Cyclosporin A bei Nummuli nach Keratoconjunctivitis epidemica Eine Pilotstudie - Springer". Der Ophthalmologe. 97 (11): 764-768. doi:10.1007/s003470070025. PMID 11130165.
- ^ Lee SS, Tan AW, Giam YC (May 2004). "Cyclosporin in the treatment of severe atopic dermatitis: a retrospective study" (PDF). Annals of the Academy of Medicine, Singapore. 33 (3): 311-313. PMID 15175770. 21 Ocak 2022 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 11 Ekim 2021.
- ^ Dijkmans BA, van Rijthoven AW, Goei Thè HS, Boers M, Cats A (August 1992). "Cyclosporine in rheumatoid arthritis". Seminars in Arthritis and Rheumatism. 22 (1): 30-36. doi:10.1016/0049-0172(92)90046-g. PMID 1411580.
- ^ Lichtiger S, Present DH, Kornbluth A, Gelernt I, Bauer J, Galler G, Michelassi F, Hanauer S (June 1994). "Cyclosporine in severe ulcerative colitis refractory to steroid therapy". The New England Journal of Medicine. 330 (26): 1841-5. doi:10.1056/NEJM199406303302601. PMID 8196726.
- ^ Naesens M, Kuypers DR, Sarwal M (February 2009). "Calcineurin inhibitor nephrotoxicity" (PDF). Clinical Journal of the American Society of Nephrology. 4 (2): 481-508. doi:10.2215/CJN.04800908. PMID 19218475. 20 Temmuz 2018 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 20 Nisan 2018.
- ^ Robert N, Wong GW, Wright JM (January 2010). "Effect of cyclosporine on blood pressure". Cochrane Database of Systematic Reviews (1): CD007893. doi:10.1002/14651858.CD007893.pub2. PMID 20091657.
- ^ Figg WD (February 1990). "Cyclosporine-induced hyperuricemia and gout". The New England Journal of Medicine. 322 (5): 334-336. doi:10.1056/NEJM199002013220514. PMID 2296276.
- ^ Agents Classified by the IARC Monographs, Volumes 1–110 25 Ekim 2011 tarihinde Wayback Machine sitesinde arşivlendi.
- ^ IARC Working Group on the Evaluation of Carcinogenic Risk to Humans (2012). Ciclosporin (İngilizce). International Agency for Research on Cancer. 28 Ağustos 2021 tarihinde kaynağından arşivlendi. Erişim tarihi: 23 Şubat 2018.
- ^ Ganong WF (2005). "27". Review of medical physiology (22.22isbn=978-0-07-144040-0 bas.). New York: McGraw-Hill Medical. s. 530.
- ^ a b c d e f g h i Mott JL, Zhang D, Freeman JC, Mikolajczak P, Chang SW, Zassenhaus HP (July 2004). "Cardiac disease due to random mitochondrial DNA mutations is prevented by cyclosporin A". Biochemical and Biophysical Research Communications. 319 (4): 1210-5. doi:10.1016/j.bbrc.2004.05.104. PMID 15194495.
- ^ a b c d e Youn TJ, Piao H, Kwon JS, Choi SY, Kim HS, Park DG, Kim DW, Kim YG, Cho MC (December 2002). "Effects of the calcineurin dependent signaling pathway inhibition by cyclosporin A on early and late cardiac remodeling following myocardial infarction". European Journal of Heart Failure. 4 (6): 713-8. doi:10.1016/S1388-9842(02)00120-4. PMID 12453541.
- ^ Handschumacher RE, Harding MW, Rice J, Drugge RJ, Speicher DW (November 1984). "Cyclophilin: a specific cytosolic binding protein for cyclosporin A". Science. 226 (4674): 544-7. Bibcode:1984Sci...226..544H. doi:10.1126/science.6238408. PMID 6238408.
- ^ a b c d e f Elrod JW, Wong R, Mishra S, Vagnozzi RJ, Sakthievel B, Goonasekera SA, Karch J, Gabel S, Farber J, Force T, Brown JH, Murphy E, Molkentin JD (October 2010). "Cyclophilin D controls mitochondrial pore-dependent Ca(2+) exchange, metabolic flexibility, and propensity for heart failure in mice". Journal of Clinical Investigation. 120 (10): 3680-7. doi:10.1172/JCI43171. PMC 2947235 $2. PMID 20890047.
- ^ Briston T, Selwood DL, Szabadkai G, Duchen MR (January 2019). "Mitochondrial Permeability Transition: A Molecular Lesion with Multiple Drug Targets" (PDF). Trends in Pharmacological Sciences. 40 (1): 50-70. doi:10.1016/j.tips.2018.11.004. PMID 30527591. 21 Ocak 2022 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 2 Ağustos 2021.
- ^ Morciano G, Giorgi C, Bonora M, Punzetti S, Pavasini R, Wieckowski MR, Campo G, Pinton P (January 2015). "Molecular identity of the mitochondrial permeability transition pore and its role in ischemia-reperfusion injury". Journal of Molecular and Cellular Cardiology. 78: 142-53. doi:10.1016/j.yjmcc.2014.08.015. hdl:11392/2149014. PMID 25172387.
- ^ Zorov DB, Juhaszova M, Sollott SJ (July 2014). "Mitochondrial reactive oxygen species (ROS) and ROS-induced ROS release". Physiological Reviews. 94 (3): 909-50. doi:10.1152/physrev.00026.2013. PMC 4101632 $2. PMID 24987008.
- ^ Borel JF (June 2002). "History of the discovery of cyclosporin and of its early pharmacological development". Wiener Klinische Wochenschrift. 114 (12): 433-7. PMID 12422576.
- ^ Wang CP, Hartman NR, Venkataramanan R, Jardine I, Lin FT, Knapp JE, Starzl TE, Burckart GJ (1989). "Isolation of 10 cyclosporine metabolites from human bile". Drug Metabolism and Disposition. 17 (3): 292-6. PMC 3154783 $2. PMID 2568911.
- ^ Copeland KR, Yatscoff RW, McKenna RM (February 1990). "Immunosuppressive activity of cyclosporine metabolites compared and characterized by mass spectroscopy and nuclear magnetic resonance". Clinical Chemistry. 36 (2): 225-9. doi:10.1093/clinchem/36.2.225. PMID 2137384.
- ^ Lawen A (October 2015). "Biosynthesis of cyclosporins and other natural peptidyl prolyl cis/trans isomerase inhibitors". Biochimica et Biophysica Acta (BBA) - General Subjects. 1850 (10): 2111-20. doi:10.1016/j.bbagen.2014.12.009. PMID 25497210.
- ^ Dittmann J, Wenger RM, Kleinkauf H, Lawen A (January 1994). "Mechanism of cyclosporin A biosynthesis. Evidence for synthesis via a single linear undecapeptide precursor". Journal of Biological Chemistry. 269 (4): 2841-6. doi:10.1016/S0021-9258(17)42019-9. PMID 8300618.
- ^ Hoppert M, Gentzsch C, Schörgendorfer K (October 2001). "Structure and localization of cyclosporin synthetase, the key enzyme of cyclosporin biosynthesis in Tolypocladium inflatum" (PDF). Archives of Microbiology. 176 (4): 285-93. doi:10.1007/s002030100324. PMID 11685373.
- ^ Dewick, P. (2001) Medicinal Natural Products.
- ^ Yang X, Feng P, Yin Y, Bushley K, Spatafora JW, Wang C (October 2018). "Tolypocladium inflatum Benefits Fungal Adaptation to the Environment". mBio. 9 (5). doi:10.1128/mBio.01211-18. PMC 6168864 $2. PMID 30279281.
- ^ Bushley KE, Raja R, Jaiswal P, Cumbie JS, Nonogaki M, Boyd AE, Owensby CA, Knaus BJ, Elser J, Miller D, Di Y, McPhail KL, Spatafora JW (June 2013). "The genome of tolypocladium inflatum: evolution, organization, and expression of the cyclosporin biosynthetic gene cluster". PLOS Genetics. 9 (6): e1003496. doi:10.1371/journal.pgen.1003496. PMC 3688495 $2. PMID 23818858.
- ^ Xu L, Li Y, Biggins JB, Bowman BR, Verdine GL, Gloer JB, Alspaugh JA, Bills GF (March 2018). "Identification of cyclosporin C from Amphichorda felina using a Cryptococcus neoformans differential temperature sensitivity assay". Applied Microbiology and Biotechnology. 102 (5): 2337-2350. doi:10.1007/s00253-018-8792-0. PMC 5942556 $2. PMID 29396588.
- ^ di Salvo ML, Florio R, Paiardini A, Vivoli M, D'Aguanno S, Contestabile R (January 2013). "Alanine racemase from Tolypocladium inflatum: a key PLP-dependent enzyme in cyclosporin biosynthesis and a model of catalytic promiscuity". Archives of Biochemistry and Biophysics. 529 (2): 55-65. doi:10.1016/j.abb.2012.11.011. PMID 23219598.
- ^ a b Borel JF, Kis ZL, Beveridge T (1995). "The history of the discovery and development of Cyclosporin (Sandimmune)". Merluzzi VJ, Adams J (Ed.). The search for anti-inflammatory drugs case histories from concept to clinic. Boston: Birkhäuser. ss. 27-63. ISBN 978-1-4615-9846-6. 5 Kasım 2017 tarihinde kaynağından arşivlendi.
- ^ Cheng M (2013). "Hartmann Stahelin (1925-2011) and the contested history of cyclosporin A". Clinical Transplantation. 27 (3): 326-329. doi:10.1111/ctr.12072. PMID 23331048.
- ^ Borel JF, Feurer C, Gubler HU, Stähelin H (July 1976). "Biological effects of cyclosporin A: a new antilymphocytic agent". Agents and Actions. 6 (4): 468-75. doi:10.1007/bf01973261. PMID 8969.
- ^ Rüegger A, Kuhn M, Lichti H, Loosli HR, Huguenin R, Quiquerez C, von Wartburg A (1976). "[Cyclosporin A, a Peptide Metabolite from Trichoderma polysporum (Link ex Pers.) Rifai, with a remarkable immunosuppressive activity]" [Cyclosporin A, a Peptide Metabolite from Trichoderma polysporum (Link ex Pers.) Rifai, with a remarkable immunosuppressive activity]. Helvetica Chimica Acta (Almanca). 59 (4): 1075-92. doi:10.1002/hlca.19760590412. PMID 950308.
- ^ Heusler K, Pletscher A (June 2001). "The controversial early history of cyclosporin". Swiss Medical Weekly. 131 (21–22): 299-302. doi:10.4414/smw.2001.09702. PMID 11584691. 2 Eylül 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 10 Ocak 2019.
- ^ Calne RY, White DJ, Thiru S, Evans DB, McMaster P, Dunn DC, Craddock GN, Pentlow BD, Rolles K (1978). "Cyclosporin A in patients receiving renal allografts from cadaver donors". The Lancet. 2 (8104–5): 1323-7. doi:10.1016/S0140-6736(78)91970-0. PMID 82836.
- ^ Starzl TE, Klintmalm GB, Porter KA, Iwatsuki S, Schröter GP (July 1981). "Liver transplantation with use of cyclosporin a and prednisone". The New England Journal of Medicine. 305 (5): 266-9. doi:10.1056/NEJM198107303050507. PMC 2772056 $2. PMID 7017414.
- ^ Kolata G (September 1983). "FDA speeds approval of cyclosporin". Science. 221 (4617): 1273. Bibcode:1983Sci...221.1273K. doi:10.1126/science.221.4617.1273-a. PMID 17776314.
On 2 September (1983), the Food and Drug Administration approved cyclosporin, a new drug that suppresses the immune system.
- ^ Gottesman J (20 Mart 1988). "Milestones in Cardiac Care". Los Angeles Times. 26 Şubat 2017 tarihinde kaynağından arşivlendi.
- ^ "First Successful Pediatric Heart Transplant [9 June 1984]". Columbia University Medical Center, Dept. of Surgery, Cardiac Transplant Program. 1 Mart 2017 tarihinde kaynağından arşivlendi.
It [cyclosporine] gained FDA approval at the end of 1983, ...
- ^ "Drugs@FDA: FDA Approved Drug Products [Click on "Approval Date(s) and History]". United States Food and Drug Administration. 1 Mart 2017 tarihinde kaynağından arşivlendi.
Drug Name(s): Sandimmune (Cyclosporine), Company: Novartis, Action Date: 11/14/1983, Action Type: Approval, Submission Classification: Type 1 - New Molecular Entity, Review Priority: Priority
- ^ Gibaud S, Attivi D (August 2012). "Microemulsions for oral administration and their therapeutic applications". Expert Opinion on Drug Delivery. 9 (8): 937-51. doi:10.1517/17425247.2012.694865. PMID 22663249. 5 Mart 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 4 Mart 2018.
- ^ Min DI (March 1996). "Neoral: a microemulsion cyclosporine". Journal of Transplant Coordination. 6 (1): 5-8. doi:10.7182/prtr.1.6.1.f04016025hh795up. PMID 9157923.
- ^ "Neoral" (PDF). FDA Data Dashboard. Food and Drug Administration (FDA); Novartis. September 2009. 20 Ekim 2022 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 24 Ekim 2022.
- ^ "Ikervis". Santen. 3 Temmuz 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Temmuz 2018.
- ^ National Heart, Lung, and Blood Institute (NHLBI) (4 Eylül 2020). "Phase II Trial of Cyclosporine Inhalation Solution (CIS) in Lung Transplant and Hematopoietic Stem Cell Transplant Recipients for Treatment of Bronchiolitis Obliterans Syndrome". 25 Mart 2023 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Haziran 2023.
- ^ Trammer B, Amann A, Haltner-Ukomadu E, Tillmanns S, Keller M, Högger P (November 2008). "Comparative permeability and diffusion kinetics of cyclosporine A liposomes and propylene glycol solution from human lung tissue into human blood ex vivo". European Journal of Pharmaceutics and Biopharmaceutics. 70 (3): 758-64. doi:10.1016/j.ejpb.2008.07.001. PMID 18656538.
- ^ Administrator. "Hem - NeuroVive Pharmaceutical AB". neurovive.com. 6 Ocak 2014 tarihinde kaynağından arşivlendi.
- ^ Ehinger KH, Hansson MJ, Sjövall F, Elmér E (January 2013). "Bioequivalence and tolerability assessment of a novel intravenous ciclosporin lipid emulsion compared to branded ciclosporin in Cremophor EL" (PDF). Clinical Drug Investigation. 33 (1): 25-34. doi:10.1007/s40261-012-0029-x. PMC 3586182 $2. PMID 23179472. 26 Ekim 2018 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 26 Ekim 2018.
- ^ Sullivan PG, Thompson M, Scheff SW (February 2000). "Continuous infusion of cyclosporin A postinjury significantly ameliorates cortical damage following traumatic brain injury". Experimental Neurology. 161 (2): 631-7. doi:10.1006/exnr.1999.7282. PMID 10686082.
- ^ Uchino H, Elmér E, Uchino K, Lindvall O, Siesjö BK (December 1995). "Cyclosporin A dramatically ameliorates CA1 hippocampal damage following transient forebrain ischaemia in the rat". Acta Physiologica Scandinavica. 155 (4): 469-71. doi:10.1111/j.1748-1716.1995.tb09999.x. PMID 8719269.
- ^ Sullivan PG, Sebastian AH, Hall ED (February 2011). "Therapeutic window analysis of the neuroprotective effects of cyclosporine A after traumatic brain injury". Journal of Neurotrauma. 28 (2): 311-8. doi:10.1089/neu.2010.1646. PMC 3037811 $2. PMID 21142667.
- ^ a b Mende U, Kagen A, Cohen A, Aramburu J, Schoen FJ, Neer EJ (November 1998). "Transient cardiac expression of constitutively active Galphaq leads to hypertrophy and dilated cardiomyopathy by calcineurin-dependent and independent pathways". Proceedings of the National Academy of Sciences of the United States of America. 95 (23): 13893-8. Bibcode:1998PNAS...9513893M. doi:10.1073/pnas.95.23.13893. PMC 24952 $2. PMID 9811897.
- ^ Wilkinson ST, Johnson DB, Tardif HL, Tome ME, Briehl MM (March 2010). "Increased cytochrome c correlates with poor survival in aggressive lymphoma". Oncology Letters. 1 (2): 227-230. doi:10.3892/ol_00000040. PMC 2927837 $2. PMID 20798784.
- ^ a b Lim HW, De Windt LJ, Mante J, Kimball TR, Witt SA, Sussman MA, Molkentin JD (April 2000). "Reversal of cardiac hypertrophy in transgenic disease models by calcineurin inhibition". Journal of Molecular and Cellular Cardiology. 32 (4): 697-709. doi:10.1006/jmcc.2000.1113. PMID 10756124.
- ^ a b Archer TM, Boothe DM, Langston VC, Fellman CL, Lunsford KV, Mackin AJ (2014). "Oral cyclosporine treatment in dogs: a review of the literature". Journal of Veterinary Internal Medicine. 28 (1): 1-20. doi:10.1111/jvim.12265. PMC 4895546 $2. PMID 24341787.
- ^ Palmeiro BS (January 2013). "Cyclosporine in veterinary dermatology". Veterinary Clinics of North America: Small Animal Practice. 43 (1): 153-71. doi:10.1016/j.cvsm.2012.09.007. PMID 23182330.
Dış bağlantılar[değiştir | kaynağı değiştir]
- Medical Subject Headings Cyclosporine (İngilizce)
- "Cyclosporine". Drug Information Portal. U.S. National Library of Medicine. 20 Aralık 2016 tarihinde kaynağından arşivlendi. (İngilizce)
- ChemSub Online: Cyclosporin A 30 Eylül 2017 tarihinde Wayback Machine sitesinde arşivlendi. (İngilizce)
