Membran potansiyeli

Çeper potansiyeli (zar voltajı olarak da bilinir) biyolojik hücrenin içi ve dışı arasındaki elektrik potansiyel farkıdır. Dış kısım için bu potansiyel değeri genellikle -40 mV ile -80 mV arasındadır.
Bütün hayvan hücreleri içinde protein bulunduran çift katlı lipit katmanının oluşturduğu hücre zarıyla sarılıdır ve bu zar iyon hareketlerine karşı yalıtkan bir difüzyon bariyeri görevi görür. İyon taşıyıcı proteinler iyonları aktif olarak hücre duvarının içine iter ve duvar boyunca bir yoğunluk meyiline sebep olur. İyon kanalları iyonların bu meyil doğrultusunda duvar boyunca ilerlemesine izin yardımcı olur. İyon kanalları ve taşıyıcıları elektriksel olarak pil ve direnç takımına eşdeğerdir. Bu yüzden duvarın iki tarafında potansiyel fark oluşur.
Neredeyse hiçbir hücrenin (hayvan, bitki ve mantar hücreleri de dâhil) zar potansiyeli sıfır değildir. Genellikle hücrenin iç tarafı dış tarafa göre negatiftir ve -40 mV ile -80 mV arasında değişen bir voltaja sahiptir. Zar voltajının iki temel fonksiyonu vardır. Birincisi, hücre duvarının içindeki moleküler araçlara güç vererek hücrenin pil işlevi görmesini sağlar. İkincisi, nöronlar ve kas hücreleri gibi elektriksel olarak uyarılabilen hücrelerde, hücrenin farklı parçaları arasındaki iletim sinyalleri olarak kullanılır. Bu sinyaller iyon kanallarının açılması ya da kapanmasıyla oluşan potansiyel değişiklik sayesinde üretilir. Elektrik alandaki bu değişiklik uzaktaki iyon kanallarını bile etkileyebilir ve onların da açılıp kapanarak sinyal üretmesine sebep olabilir.
Uyarılamayan hücrelerde ve uyarılabilen hücrelerin temel durumlarında, zar potansiyeli neredeyse sabittir ve bu duruma dingin potansiyel denir. Nöronların dingin potansiyeli genellikle -70, -80 milivolt aralığındadır ve iç tarafındaki negatif temel voltajı o voltajın onda birinden daha azdır. İyon kanallarının açılıp kapanması, dingin potansiyel durumundan çıkılmasına sebep olabilir. Eğer iç taraftaki potansiyel arttıysa (örneğin -70 mV, -60 mV arası) buna depolarizasyon (kutupsuzlaşma), eğer azaldıysa (örneğin -70 mV, -80 mV arası) buna hiperpolarizasyon denir. Uyarılabilen hücrelerde, çok büyük depolarizasyonlar kutupların ters dönmesine sebep olan, zar potansiyelini çok hızlı ve art arda değiştirebilen (milisaniyenin yüzde biri gibi) aksiyon potansiyeline sebep olabilir. Aksiyon potansiyeli voltaja duyarlı iyon kanallarının aktifleşmesiyle üretilir.
Nöronlarda zar potansiyeline etki eden faktörler değişkendir. Oldukça fazla sayıda iyon kanalı bulundururlar ve bunlardan bazıları kimyasala, bazıları voltaja duyarlıdır. Voltaja duyarlı iyon kanalları membran potansiyeli tarafından kontrol edildiği için, membran potansiyelinin kendisi de bu kanallardan etkilendiğinde, geri besleme döngüsü aksiyon potansiyeli gibi titreşen ve yeniden üretilebilir kompleks temporal dinamiklerin artışına sebep olur.
Fiziksel temeli[değiştir | kaynağı değiştir]
Membran potansiyeli iki temel faktörden meydana gelir; difüzyon ve elektriksel kuvvet. Elektriksel kuvvet zıt yüklü parçacıkların birbirini çekip aynı yüklülerin itmesiyle oluşur. Difüzyon ise parçacıkların yüksek yoğunluklu bölgelerden düşük yoğunluktaki bölgelere geçme eğilimiyle meydana gelir (termal enerji sayesinde).
Voltaj[değiştir | kaynağı değiştir]
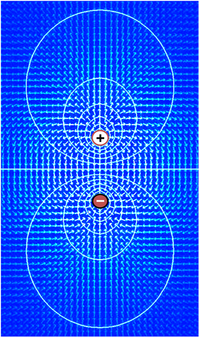
Voltaj, yani elektriksel potansiyel farkı, elektrik akımının dirençten geçebilme kabiliyetidir. Voltajın daha basit tanımı Ohm yasası tarafından yapılabilir: V=IR. Burada V voltaj, I akım, R ise dirençtir. Eğer bir devrede pil gibi bir voltaj kaynağı varsa, bu kaynağın voltaj yüksekliği direnci aşan daha fazla akım anlamına gelir. Voltaj sadece iki nokta arasında potansiyel fark olduğu zaman işlevseldir. Tek bir noktadaki voltajın herhangi bir işlevi yoktur. Elektronikte geleneksel olarak devredeki rastgele elemanlardan birine sıfır voltaj atanıp diğer elemanların voltajı bu sıfır noktasındaki elemana göre ölçülür. Devredeki bir elemanı sıfır noktası seçmenin o eleman için bir anlamı yoktur devrenin işlevi tek başına voltaja bağlı değildir. Ayrıca çoğu durumda sıfır noktası devrenin topraklama kısmı olarak kabul edilir.
Aynı prensip hücre biyolojisindeki voltaj için de geçerlidir. Elektriksel olarak etkin dokunun potansiyel farkı, dokunun herhangi iki noktasına batırılan elektrotlar sayesinde ölçülür. Mesela elektrotlardan biri hücrenin içine diğeri dışına takılıp sonra da bu elektrotlar bir voltmetreye bağlanıp değer okunur. Hücrenin dış tarafı sıfır noktası kabul edilir ve potansiyel farkın işaretine içerideki potansiyelin dışarıya göre ölçümüyle karar verilir.
Matematiksel olarak voltajın tanımı elektrik alanı (E) ile başlar. Birçok durumda elektrik alanı korunumlu alandır ve voltajın skaler fonksiyon eğimi olarak yazılabilir; E = –∇V. Bu skaler büyüklük voltaj dağılımını gösterir. Mutlak değerli voltajın bir anlamı yoktur çünkü tanım integral içerir. Genellikle eğer manyetik alanın çok fazla etkisi yoksa, elektrik alanı korunumlu alan kabul edilir ve bu biyolojik dokular için de işe yarar.
Elektrik alanı voltajın dağılım eğimi olduğu için küçük bir bölgedeki hızlı voltaj değişimleri, şiddetli elektrik alanı anlamına gelir. Tam tersi eğer voltaj büyük bir alanda yaklaşık olarak aynı değere sahipse bu bölgedeki elektrik alan çok zayıf olur. Güçlü elektrik alan, güçlü voltaj eğimi demektir ve dolayısıyla bölgedeki yüklü parçacıklara şiddetli bir kuvvet uygulanır.
İyonlar ve hareketlerini yönlendiren kuvvetler[değiştir | kaynağı değiştir]
[1]
Biyolojik organizmalarda elektrik sinyalleri genellikle iyonlar tarafından taşınır.[2] Aksiyon potansiyeli için en önemli katyonlar sodyum (Na+) ve Potasyumdur (K+).[3] İkisi de tek bir pozitif yük taşıyan tek değerli katyonlardır. Ayrıca kalsiyum (Ca2+) da iki tane pozitif yük taşıyan çift değerli bir katyon olarak aksiyon potansiyelinde rol alabilir.[4] Klorür anyonu (Cl−) ise bazı Alglerde aksiyon potansiyelindeki en önemli role sahiptir[5] ama hayvanlardaki önemi yok denecek kadar azdır.[6]
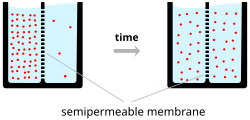
Hücre zarındaki iyon geçişi iki etki altında gerçekleşir: difüzyon ve elektrik alanı. Mesela, A ve B isimli iki çözeltinin geçirgen olan gözenekli (porlu) bir bariyerle ayrıldığını düşünelim. Bu iki çözelti aralarındaki yoğunluk farkından dolayı zamanla karışacak ve iki eş çözelti oluşacak. Yüksek yoğunluktaki bölgeden düşük yoğunlukluya doğru bir difüzyon gerçekleşecek. Örneği genişletecek olursak, A çözeltisi 30 tane sodyum ve 30 tane klorür iyonu barındırsın, B çözeltisi de 20 sodyum ve 20 klorür. Aradaki bariyerin iki iyon tipini de geçirebildiğini farz edersek, son durumda iki çözeltide de 25 sodyum ve 25 klorür iyonu olacak. Eğer bariyerdeki porlar iyonlara göre seçiciyse sonuç daha farklı olur. Örneğin önceki bariyerin sadece sodyum iyonlarına karşı geçirgen olduğunu düşünelim. Bu sefer sodyum iyonları yüksek yoğunluktaki bölgeden düşük yoğunluktakine geçecek, yani A'dan B'ye. Bunun sonucunda B çözeltisindeki sodyum birikimi klorürden fazla olacak, tersi şekilde A çözeltisindeki klorür sayısı sodyum sayısından daha fazla olacak.
Yani B çözeltisinde pozitif yüklü iyonların sayısı negatif yüklülerden daha fazla olacak ve çözelti pozitif yüklenmiş olacak. Aynı şekilde A çözeltisinde negatif yüklü iyonların sayısı fazla olacağından, negatif yüklenmiş olacak. Zıt yükler birbirini çektiğinden, iyonlar bu sefer elektrik alanından etkilenmeye başlayacak ve pozitif sodyum iyonlarının B'ye gitmesi daha da zor olacak. Bu noktada difüzyon ve elektrik alanı birbirini dengelemeye başlayacak ve denge potansiyelini oluşturacak, iyon geçişi tamamen duracak.
Plazma zarları[değiştir | kaynağı değiştir]

Her hayvan hücresi, içinde birçok molekül içeren çift katlı lipit katmanından oluşun plazma zarıyla kaplıdır. Bu zar lipitten (yağ) oluştuğu için doğal olarak yüksek elektrik direncine sahiptir. Diğer bir deyişle düşük iyon geçirgenliğine sahiptir. Fakat zar içindeki bazı moleküller iyonların geçişini sağlayabilir ya da onları geçirecek kanalları açabilir. .[7]
Elektrik terminolojisine göre hücre zarı direnç ve kapasitör fonksiyonu görür. Direnç, zarın yük hareketini engellemesinden doğar. Kapasite (sığa) ise çok ince olan lipit katmanının dışarıdaki ve içerideki zıt yüklü parçacıkların birbirini çekmesine olanak verecek kadar ince olmasıdır. Zarın kapasitesi içerdiği moleküllerden etkilenmez ve bu yüzden yaklaşık olarak 2 µF/cm² civarı sabit bir değere sahiptir (zar parçasının toplam kapasitesi alanıyla doğru orantılıdır). Saf yağ katmanının iletkenliği çok düşüktür ama biyolojik durumlarda her zaman başka moleküller tarafından bu yalıtkanlık baskılanır. Bu yüzden zarın kapasitesi neredeyse sabittir ve direnci oldukça değişkendir.
Hücre zarının kalınlığı yaklaşık olarak 7-8 nanometre civarındadır. Çok ince olduğu için içerisinden çok güçlü bir elektrik alanı yaratacak kadar voltaj geçiremez. Tipik bir hayvan hücresinin membran potansiyeli 100 milivolt civarındadır (voltun onda biri) ama hesaplamalar gösteriyor ki hücre zarı taşıyabileceği maksimum elektrik alanı taşıyor (voltaj farkı elektriksel kırılıma sebep olabilecek 200 milivolttan çok daha yüksek çıktı).
Kolaylaştırılmış difüzyon ve taşıma[değiştir | kaynağı değiştir]
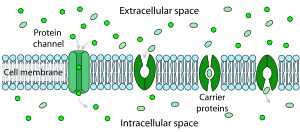
Lipit tabakasının direnci çok yüksek olmasına rağmen zar içindeki bazı yapılar aktif ya da pasif olarak iyon geçişine yardım edebilir. Bu mekanizmaya kolaylaştırılmış taşıma ya da kolaylaştırılmış difüzyon denir. Kolaylaştırılmış difüzyonda en büyük rolü ikisi de proteinden oluşan,iyon kanalları ve iyon pompaları oynar. İyon kanalları iyonların geçebileceği küçük geçitler açar ve çoğu durumda bu geçitler sadece belirli iyonları geçirir (kimi zaman iyonların yönleri de bu durumu etkiler). İyon pompaları ise -taşıyıcı proteinler olarak da bilinir- aktif olarak bazı spesifik iyonları taşır. Bazı durumlarda metabolik süreçle üretilen enerjiyi de kullanır.
İyon pompaları[değiştir | kaynağı değiştir]
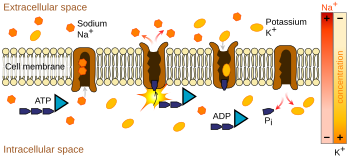
İyon pompaları aktif taşıma yapan -iyon pompalamak için ATP (hücresel enerji) kullanmak gibi- integral proteinleridir.[8] Bu iyon pompaları içerideki ve dışarıdaki yoğunluğu değiştirerek işini yapar. Aksiyon potansiyeliyle en çok ilgisi olan iyon pompası dışarı üç sodyum iyonu bırakıp içeri iki potasyum iyonu alarak çalışan sodyum-potasyum pompasıdır.[9] Bunun sonucunda, nöronun içindeki potasyum K+ iyonlarının yoğunluğu dışarıdaki yoğunluğun 20 katına ulaşırken dışarıdaki sodyum yoğunluğu da içerinin 9 katına yaklaşır.[10][11] Benzer biçimde, kalsiyum, klorür ve magnezyum gibi diğer iyonlar da nöronun içinde ve dışında farklı yoğunluklara sahip olur.[11]
İyon pompası aksiyon potansiyelini sadece hücre içinde ve dışında yakın yoğunluk yaratarak etkiler. Aksiyon potansiyeli iyon pompasından daha çok iyon kanallarının açılıp kapanmasında yer alır. Eğer iyon pompasının enerji kaynağı biterse ya da ok zehri (ouabain) gibi bir inhibitörle (engelleyici) karşılaşırsa, aksonlar genlikleri çok çok azalıncaya kadar binlerce aksiyon potansiyeli ateşlemeye devam edebilirler.[8] Bilhassa, aksiyon potansiyelinden sonra iyon pompalarının pek hücre zarının kutuplaşmasında pek bir önemi kalmıyor.[3]
Membran potansiyelinin üretimindeki en büyük pay sodyum-potasyum pompasına aittir. Bu mekanizma membran içinde bulunan ve zardan sodyum ve potasyum geçişini sağlamak için ATP'den enerji üreten bir protein kompleksidir. Her bir döngüde içerideki üç sodyum iyonu dışarıdaki iki potasyum iyonuyla değiştirir. Eğer iki iyonun da sayıları aynıysa, pompa elektriksel olarak nötrdür ama değişim üçe iki olduğundan, her döngüde içeriden dışarıya bir tane pozitif yük verilir ve böylelikle pozitif voltaj farkı yaratılır. Pompanın üç etkisi vardır: (1) dışarıdaki sodyum yoğunluğunu arttırıp, içeridekini düşürür; (2) içerideki potasyum yoğunluğunu arttırıp, dışarıdakini düşürür; (3) içerideki voltajı dışarıya göre negatif hale getirir.
Sodyum-potasyum pompası işlem sırasında göreceli olarak yavaştır. Eğer başlangıçta hücrenin her yerindeki potasyum ve sodyum yoğunluğu aynıysa pompanın denge durumuna getirmesi saatler alır. Sodyum-potasyum pompası devamlı çalışır ama pompalanabilen sodyum ve potasyum sayısı azaldıkça etkisi zamanla azalmaya başlar.
Fonksiyonel olarak önemli olan diğer iyon pompası ise sodyum-kalsiyum pompasıdır. Dışarıdan üç sodyum iyonu alıp dışarıya bir tane kalsiyum iyonu vermesi dışında çalışma yöntemi sodyum-potasyum pompasıyla aynıdır. Net yük akışı içeriye doğru olduğu için pompa inişli çalışır ve bu yüzden membran voltajı dışında herhangi bir enerji kaynağı gerektirmez. Sodyum-kalsiyum pompasının en önemli etkisi kalsiyumu dışarı pompalanmasıdır. Kalsiyum ve sodyumun yoğunluk farkı çok olduğu için dışarıdaki sodyumların kendiliğinden akışı sağlanır ama sodyum-potasyum pompasında bu etki diğerine göre yok sayılacak kadar azdır. Sodyum-kalsiyum pompasının çalışması sonucu hücre içindeki kalsiyum yoğunluğu çok düşer ve hücre dingin duruma ulaşır.
İyon kanalları[değiştir | kaynağı değiştir]

İyon kanalları iyonların hücre dışından içine doğru ilerleyebilmesini sağlayan porlu integral zar proteinleridir. Çoğu kanal spesifik bir iyonu geçirmek için özelleşmiştir. Mesela potasyum kanalları, aynı yüke sahip olup sadece biraz çap farkı olan sodyum ve potasyumu ayırıp potasyumu geçirir. Kanal porları iyonları sadece tekli sıra halinde geçirecek kadar küçüktür.[13] Birçok kanal çeşitli alt iletkenlik seviyesine sahip olmasına rağmen, iyon geçişine kapalı da olabilir açık da. Bir kanal açıkken, yoğunluk farkından dolayı iyonlar porlardan geçip hücrenin içine sızar. İyonik akım oranı -mesela tek kanallı akım genliği- maksimum kanal iletkenliği ve membran potansiyeliyle geri dönüm potansiyeli arasındaki farktan oluşan elektrokimyasal kuvvet tarafından belirlenir.[14]
Kanallar proteinlerin farklı yapılarına göre farklı durumlarda olabilir ama her halukarda açık ya da kapalıdırlar. Genellikle, kapalı durumda porlar büzüşür ve iyon geçişine müsaade etmez ya da proteinin bazı kısımları poru tıkar. Örneğin, voltaja bağlı kanallarda protein parçası porun içine girip açıklığı kapatır ve kanalı inaktive eder.[15] Bu inaktivasyon sodyum akışını durdurur ve aksiyon potansiyelinde büyük rol oynar.
İyon kanalları çevresel faktörlere verdikleri tepkilerle sınıflandırılabilir.[16] Örneğin, aksiyon potansiyelinde yer alan voltaja bağlı iyon kanalları zardan geçen voltaja göre açılıp kapanır. Liganda bağlı kanallar ise nörotransmitter gibi ligand moleküllerinin bağlanmasına bağlı olarak açılıp kapanır. Diğer kanal türlerinin bazılar mekanik kuvvetlerle açılıp kapanır, bazıları ise (sensör nöronları gibi) ışık, sıcaklık ve basınçla açılıp kapanır.
Sızıntı kanalları[değiştir | kaynağı değiştir]
Sızıntı kanalları iyon kanallarının en basit türüdür. Geçirgenlikleri aşağı yukarı sabittir. Bu tür kanallar, özellikle potasyum ve klorür kanalları, nöronlar için çok önemlidir. Yine de özelliklerinin tamamen sabit olmaması dikkate alınmalıdır. Birçoğu iyi bir şekilde temas ettiğinde voltaja bağlı hale gelir diğer bir deyişle doğrultuculardır. Ayrıca bazıları liganda bağlı olmamalarına rağmen ligand tarafından kapatılabilirler.
Liganda duyarlı kanallar[değiştir | kaynağı değiştir]
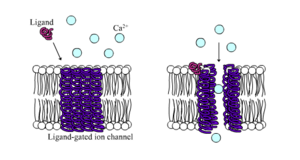
Liganda duyarlı iyon kanalları (kimyasal kapılı iyon kanalları) bir ligand türü proteinin yapısına bağlandığında geçirgenlikleri oldukça artan kanallardır. Hayvan hücrelerinde bunlardan yüzlerce bulunur. Nörotransmitter reseptörler (postsinaptik bölgelerde oluşur) gibi geniş fonksiyon alt kümeleri ve onlara kapı olan kimyasal ligandlar presinaptik akson terminallerinden salınır. Bu türün bir örneği AMPA reseptörleridir. Bu reseptörler aktive edildiklerinde sodyum ve potasyum geçişini sağlayan nörotransmitter glutamik asitler için çalışır. Diğer bir örnek ise aktive edildiğinde klorür geçişini sağlayan GABA nörotransmitteri için çalışan GABA reseptörleridir.
Nörotransmitter reseptörler hücre dışında beliren ligandlar tarafından aktive edilir ama hücre içindeki etkileşimlerle kontrol edilen ligand duyarlı kanallar da vardır.
Voltaja duyarlı kanallar[değiştir | kaynağı değiştir]
Voltaj-Kapılı iyon kanalları, ya da diğer bir deyişle voltaja duyarlı kanallar, geçirgenliği membran potansiyelinden etkilenen kanallardır. Her bir üyesi farklı bir iyon ve farklı bir voltaj değeri için özelleştiğinden büyük bir grup oluştururlar. Ayrıca birçoğu zamana da bağlıdır. Yani voltaj değişimine hemen tepki vermez biraz süre geçmesini beklerler.
Bu grubun en önemli üyelerinden biri aksiyon potansiyelinin altında yatan voltaja duyarlı sodyum kanallarıdır (bu kanallar aksiyon potansiyelinin fizyolojisini betimleyen Hodgkin-Huxley modeli ile Nobel Fizyoloji veya Tıp Ödülü kazanan Alan Lloyd Hodgkin ve Andrew Huxley tarafından sınıflandırılmış oldukları için Hodgkin-Huxley sodyum kanalları olarak da bilinir). Bu kanal dingin potansiyel durumunda kapalıdır ama voltaj belli bir eşiği geçer geçmez açılır ve membran potansiyelinde ani değişime sebep olan hızlı bir sodyum iyonu akışı başlar. Aksiyon potansiyelinden kurtulmak kısmen dingin voltaj durumunda kapalı olan voltaj duyarlı kanallara bağlıdır ama kanallar aksiyon potansiyeli yüzünden meydana gelen büyük voltaj değişimi sonucu açılmış olur.
Ters potansiyel[değiştir | kaynağı değiştir]
Denge potansiyeli olarak da bilinen ters potansiyel difüzyon ve elektrik kuvvetinin dengede olduğu ve hiçbir net iyon akışının olmadığı durumlarda zar içindeki voltajın değeridir. Yani zar içindeki voltaj iyonun difüzyonunun kuvvetine tamamen zıttır. Öyle ki, zardan iyon geçişi sıfırdır ve değişmezdir. Ters potansiyel çok önemlidir çünkü o iyonun geçebileceği kanallara etki eden voltajı verir. Diğer bir deyişle, pil gibi davrandığında iyon yoğunluğunun eğiminin ürettiği voltajı verir.
Bir iyonun ters potansiyeli genellikle Eiyon ile gösterilir. Herhangi bir iyonun sahip olduğu ters potansiyel Nernst eşitliği kullanılarak hesaplanabilir.[17] Örneğin, potasyum iyonları için ters potansiyel aşağıdaki eşitlikle hesaplanabilir:
burada
- Eeq,K+ potasyumun volt olarak ölçülen ters potansiyeli
- R evrensel gaz sabiti, 8.314 joule·K−1·mol-1 değerine eşittir.
- T Kelvin ( K = Santigrat derece + 273.15) olarak ölçülen mutlak sıcaklıktır
- z sayısı soruda yer alan iyonun temel yükü
- F Faraday sabiti, 96,485 coulomb·mol−1 ya da J·V−1·mol-1 değerine eşittir
- [K+]o potasyumun hücre dışı konsantrasyonu, mol·m- 3 veya mg·l-1
- [K+]i potasyumun hücre içi konsantrasyonu
İki farklı iyon aynı yüke sahip olsalar bile (mesela, K+ ve Na+), içerideki ve dışarıdaki yoğunluk farkından dolayı hala çok farklı denge potansiyellerine sahip olabilirler. Örneğin, nöronlardaki potasyum ve sodyumun denge potansiyellerini ele alalım. Potasyum denge potansiyeli dışarıda 5 mM potasyum ve içeride 140 mM potasyum varken (EK) -84 mV olarak hesaplanır . Diğer taraftan, sodyum denge potansiyeli, ENa, içeride 12 mM ve dışarıda 140 mM sodyum varken yaklaşık olarak +40 mV değerini verir.[note 1]
Eşdeğer devre[değiştir | kaynağı değiştir]
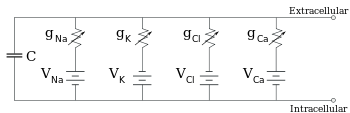
Elektrofizyolojistler iyonik yoğunluk farkının etkilerini, iyon kanalları ve membran kapasitesini eşdeğer devre üzerinden modeller. Bu devre sayesinde bir zar parçasının elektriksel özelliklerini ortaya koyabilirler. Eşdeğer devre her biri seri pil içeren dört paralel yol ve bir kapasitör bulundurur. Kapasite lipit katmanının özelliğine göre belirlenir ve sabit kabul edilir. Her dört paralel yol sodyum, potasyum, klorür ve kalsiyum iyonlarından gelir. Voltaj ise her bir iyonun yoğunluklarına göre belirlenir (yukarıdaki ters potansiyele bakın). Her bir iyonik yolun iletkenliği ise iyon kanallarının geçirgenlik durumuna göre belirlenir.
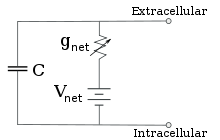
Sabit iyon konsantrasyonu ve kanal iletkenliğinin sabit değerleri için, eşdeğer devre daha da azaltılabilir. Aşağıda anlatıldığı gibi, paralel pil ve kapasitör bulunduran bir devre için Goldman denklemi kullanılır. Elektrik açısından, bu bir tür RC devresidir (direnç-kapasitans devresi) ve elektrik özellikleri ise çok basittir. Herhangi bir ilk durumdan başlayan akım, bir zaman sabiti olan τ = RC ile üstel zaman fonksiyonuyla azalır, burada C zar parçasının kapasitansı ve R = 1/gnet ise net direnç. Gerçekçi durumlar için, zaman sabiti genellikle 1-100 milisaniye aralığında yatar. Çoğu durumda, iyon kanallarının iletkenlik değişimi çok daha hızlı olur bu yüzden RC devresi iyi bir yaklaşım değildir ama yine de zar parçasını modellemek için kullanılan diferansiyel denklemi RC devrelerinin modifiye edilmiş halidir.
Dingin potansiyel[değiştir | kaynağı değiştir]
Membran potansiyeli uzun periyodlar boyunca kayda değer bir değişim göstermediği zaman, bu duruma dingin potansiyel ya da dinlenme potansiyeli denir. Bu terim genellikle uyarılamayan hücreler için kullanılsa da uyarımı olmayan uyarılabilir hücreler için de kullanılabilir. Uyarılabilen hücrelerde, diğer olası durumlar kademeli membran potansiyeli ve büyük aksiyon potansiyelidir. Belli bir zamanı takip eden membran potansiyeli ya hep, ya hiç prensibine göre hareket eder. Uyarılabilen hücrelerden bazıları nöronlar, kas hücreleri ve salgı bezlerinde bulunan salgı hücreleridir. Diğer hücre tiplerinde de membran voltajı hücre içi durum ya da çevresel faktörler tarafından uyarılıp değişikliğe uğrayabilir. Örneğin, hücre zarının depolarizasyonu kontrollü hücre ölümlerinde oldukça önemli bir aşamadır.[18]
Dingin potansiyele sebep olan etkileşimler Goldman denklemleri tarafından modellenmiştir.[19] Bu da sorudaki iyonların yüklerini ve iç-dış yoğunluk farkını temel alan ve yukarıda gösterilen Nernst denklemine benzer bir formdur. Ayrıca, sorudaki her bir iyonun göreceli geçirgenliğini ayrı ayrı ele alır.
Bu soruda yer alan üç iyon potasyum (K+), sodyum (Na+) ve klorürdür (Cl−). Kalsiyum bu sorudaki rolü göz ardı edilebilir olduğu için atlanmıştır ama daha önemli olduğu sorularda eklenebilir.[20] Klorür bir anyon olduğu için katyonlardan daha farklı ele alınır. Normalde payda hücre dışı yoğunlukları ve payda da hücre içi yoğunlukları yazılırken, klorürün tam tersi şekilde paya hücre içi paydaya ise hücre dışı yoğunlukları yazılır. P harfi iyonların geçirgenliğini temsil eder.
Özünde, Goldman formülü membran potansiyelini her bir hücrenin ters potansiyelinin ağırlıklı ortalaması olarak ifade eder. (Gerçi membran potansiyeli aksiyon potansiyeli boyunca 100 mV civarında değişse de hücre içindeki ve dışındaki yoğunluklarda kayda değer bir değişim olmaz. Hücre zarı dingin potansiyeldeyken kendi yoğunluklarına sadık kalırlar.) Çoğu hayvan hücresinde, dinginlik durumundaki potasyum geçirgenliği sodyum geçirgenliğinden çok daha yüksek. Bunun sonucunda, dinlenme potansiyeli genellikle potasyum ters potansiyeline yakın olur.[21][22] Klorür geçirgenliği oldukça yüksek olabilir ama diğer iyonların tersine klorür aktif olarak pompalanmaz. Bu yüzden ters potansiyelin denge durumu diğer iyonlar tarafından belirlenen dingin potansiyele oldukça yakın olur.
Çoğu hayvan hücrelerinde membran potansiyeli dinginlik değerleri genellikle Potasyum ters potansiyel değeri (yaklaşık olarak -80 mV) ve -40 mV arasında değişir. Uyarılabilir hücrelerdeki dinginlik potasiyeli (aksiyon potansiyeli üretmeye elverişlidir) genellikle -60 mV civarındadır. Daha fazla depolarize olmuş voltajlar spontane aksiyon potansiyeli üretimine sebep olabilir.[23] Böyle hücrelerde, dinginlik potansiyel değer diferansiyelin derecesinden bağımsızdır. Bazı durumlarda hücreler herhangi bir zar içi voltaj farklılığı göstermeyebilir.
Dinlenme potansiyelinin sürdürülebilirliği, aktif pompalamanın sızıntı kanallarından sızan iyonların yerini tamamlaması gerektiği için hücreye metabolik olarak pahalıya patlayabilir. En çok efor gerektiren durum ise hücre fonksiyonunun depolarize olmuş membran potansiyeli gerektirdiği durumdur. Örneğin, kurt sineğinin (Calliphora vicina) gün ışığındaki dinlenme potansiyeline adapte olmuş ışık alıcıları -30 mV gibi yüksek bir değere sahip olabilir.[24] Bu yüksek membran potansiyeli değeri hücrenin seri bir şekilde görsel girdilerle cevap vermesini sağlar. Bu dinginlik potansiyelinin sürüdürülmesi içi hücrenin bütün ATPsinin %20 sini sadece bunun için kullanması gerekir..[25]
Öte yandan, farklılaşmamış hücrelerde yüksek dinginlik potansiyeli metabolik bir avantaj olabilir. Bu belirgin paradoks dinginlik potansiyelinin kökeninin incelenmesiyle çözülebildi. Az farklılaşmış hücreler çok az sızıntı kanalı bulundurarak, çok yüksek girdi dirençleriyle karakterize olmuşlardır.[23] Gayet açık olan sonuca göre, potasyum geçirgenliği dinginlik ve ters potansiyel arasında yer alan sodyum geçirgenliğine çok benzer bir hal alır. Azalan sızıntı akımı sayesinde aktif pompalamaya olan ihtiyaç azalır ve metabolik gereksinimler düşer.
Dereceli potansiyel[değiştir | kaynağı değiştir]
Yukarıda açıklandığı gibi, bir hücre zarı içinde herhangi bir noktada potansiyel hücre içi ve hücre dışı alan arasındaki yoğunluk farkıyla ve hücre zarının geçirgenliğiyle belirlenir. İyon konsantrasyonu normalde çok hızlı bir şekilde değişmez (kalsiyum temel hücre içi yoğunluğu çok az olduğundan dolayı istisnadır, hızlı değişebilir), ama liganda duyarlı iyon kanallarının aktive edilmesiyle iyon geçirgenliği milisaniyenin çok küçük bir kısmında değişebilir. Değişim iyon kanallarının sayısı ve türüne bağlı olarak küçük de olabilir büyük de. Bu tür değişiklikler sabit genlik ve zamanı olan aksiyon potansiyelinin tersine dereceli potansiyel olarak adlandırılır.
Yukarıda verilen Goldman denkleminden de türetilebileceği gibi, belli bir iyon için artmakta olan geçirgenliğin etkisi o iyonun membran potansiyelini ters potansiyele dönüştürebilir. Böylece, Na+ kanallarının açılması membran potansiyelini genellikle +100 mV civarında olan Na+ ters potansiyeline doğru çeker. Aynı şekilde, K+ kanallarının açılması membran potansiyelini -90 mV civarına çeker ve Cl− kanallarının açılması da yaklaşık -70 mV civarına çeker (birçok zarın dinginlik potansiyelidir). Membran potansiyelinin çalışma aralığı -90 mV ile +100 mV aralığında olduğundan, olan Na+ kanallarının etkisi membran potansiyeli her zaman yukarı çekmek, K+ kanallarının etkisi aşağı çekmek çekmek ve Cl− kanallarını etkisi dinlenme potansiyeline doğru çekmektir.
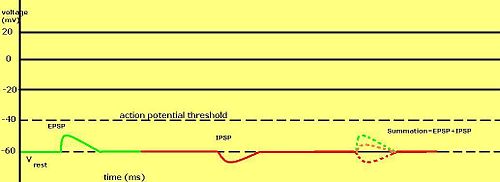
Kademeli membran potansiyelleri özellikle sinapslarda üretilen nöronlar için önemlidir—tek kademeli aksiyon potansiyeli tarafından aktive edilen sinaps tarafından üretilen membran potansiyelinin geçici değişimleri postsinaptik potansiyel olarak adlandırılır. Nörotransmitterler Na+ kanallarını açarak membran potansiyelinin daha pozitif hale gelmesini sağlarken, genellikle K+ kanallarını açarak daha negatif hale gelmesini sağlar.
Postsinaptik potansiyel iyon akımının ters potansiyeline bağlı olarak uyarıcı ya da engelleyici (inhibitör) olabilir ve bir hücrenin aksiyon potansiyeli ateşleme eşiği -50 mV civarındadır. Tipik sodyum akımlarında olduğu gibi eşiğin üstünde olan bir ters potansiyel ve postsinaptik potansiyel uyarıcı olarak kabul edilir ama bu postsinaptik potansiyel potasyum ve klorür akımlarında olduğu gibi eşiğin altında bir ters potansiyelle kombinlenirse inhibitör olarak kabul edilir. Bunun nedeni çoklu postsinaptik potansiyelin ortalama dışında bir etkisi olmamasıdır. Yani dingin potansiyelin üzerinde ama eşiğin altında olan ters potansiyelli akım eşiğe ulaşamaz. Bu yüzden, nörotransmitterler uyarıcı postsinaptik potansiyel (EPSP) üretmesi için Na+ kanallarını açarken, engelleyici postsinaptik potansiyel (IPSP) üretmesi için K+ veya Cl− kanallarını açar. Birden fazla tür kana aynı zaman diliminde açılırsa, kendi postsinaptik potansiyelleri doğrusal olmayan şekilde toplanır (birbirine eklenir).
Diğer değerler[değiştir | kaynağı değiştir]
Biyofiziğin bakış açısından, dinginlik potansiyeli yalnızca dinlenme durumundaki hücreyi domine eden membran potansiyelidir. Yukarıda verilen denklemler her zaman kullanılabilir ama aşağıdaki yaklaşım daha kolay görselleştirilmesini sağlayabilir. Verilen bir zamanda, iyonun üzerindeki membran potansiyelinden nasıl etkileneceğini belirleyen iki faktör vardır:
- İyonun itici kuvveti
- İyonun geçirgenliği
Eğer itici kuvvet yüksek ise, iyon hücre zarından itilir. Eğer geçirgenliği yüksek ise, iyonun zardan difüzyonla geçmesi daha kolay olacak.
- İtici kuvvet iyonu hücre zarı boyunca hareket ettiren net elektrik kuvvetidir. Bu kuvvet iyonun içinde olmak istediği potansiyel (kendi denge potansiyeli) ve gerçek zar potansiyeli (Em) arasındaki farktan hesaplanabilir.. Yani, iyonun itici kuvveti = E -m - E- iyon
- Örneğin, daha önce hesaplanan dinginlik potansiyeli 73 mV, potasyum üzerindeki itici kuvvet 7 mV ise : (73 mV) − (-80 mV) = 7 mV. Sodyum üzerindeki itici kuvvet (73 mV) − (60 mV) = -133 mV olurdu.
- Geçirgenlik bir iyonun zardan ne kadar kolay geçebileceğinin ölçüsüdür. Genellikle (elektrik) iletkenlik olarak, siemens birimine karşılık gelen 1 C·s−1·V−1, yani saniyede volt başına 1 coulomb şeklinde ölçülür.
Yani, dinlenme durumundaki bir membranda, potasyum için itici kuvvet düşükken, geçirgenliği çok yüksektir. Sodyum çok büyük bir itici kuvvete sahiptir ama neredeyse hiç dinginlik geçirgenliği yoktur. Bu durumda, potasyum sodyumdan yaklaşık 20 kat daha fazla akım taşır ve Em üzerinde sodyuma göre 20 kat daha etkilidir.
Ancak, aksiyon potansiyelinin pik seviyesi gibi bir başka durumu düşünürsek, burada Na geçirgenliği yüksek ve K geçirgenliği göreceli olarak düşük olacak. Böylece, membran ENa yakınlarına doğru hareket eder ve EK dan uzaklaşır.
Daha fazla iyon geçirgenliği, tahmin etmesi daha zor membran potansiyeli anlamına gelir. Bu ancak Goldman-Hodgkin-Katz denklemi çözülerek bulunabilir. Anlık bir zamandaki yoğunluk eğimi ve iyonun geçirgenliği kullanılarak o andaki membran potansiyeli belirlenebilir. GHK denklemi aslında herhangi bir zamandaki membran potansiyelinin, iyonların eşdeğerlik potansiyelinin ağırlıklı ortalaması olacağını ortaya koyar. "Ağırlık" kısmı iyonların göreceli geçirgenliğidir.
Etkileri[değiştir | kaynağı değiştir]
Hücreler enerjilerini iyon taşımak ve zarlar arası potansiyel üretmek için kullandıklarında, bu potansiyeli diğer iyonları ve şeker gibi metaboliterleri taşımak için kullanır. Mitokondrinin zarlar arası potansiyeli biyolojinin genel enerji kaynağı olan ATP üretimini tetikler.
Hücreler dingin durumlarında depoladıkları enerjiyi aksiyon potansiyeli üretmek ya da başka uyarımları tetiklemek için kullanabilir. Zar içindeki bu değişiklikler diğer hücrelerle olan iletişimi sağlar (aksiyon potansiyeliyle) ya da sperm tarafından döllenmiş bir yumurtada olduğu gibi bazı hücre içi değişiklikleri başlatabilir.
Nöron hücrelerinde, aksiyon potansiyeli sodyum iyonlarının sodyum kanalından hücre içine akmasıyla başlar ve depolarizasyona sebep olur. Bu akıma pasif difüzyon denir.
Ayrıca bakınız[değiştir | kaynağı değiştir]
Notlar[değiştir | kaynağı değiştir]
- ^ Note that the signs of ENa and EK are opposite.
Kaynakça[değiştir | kaynağı değiştir]
- ^ Campbell Biology, 6th edition
- ^ Johnston and Wu, p. 9.
- ^ a b Bullock, Orkand, and Grinnell, pp. 140–41.
- ^ Bullock, Orkand, and Grinnell, pp. 153–54.
- ^ Mummert H, Gradmann D (1991). "Action potentials in Acetabularia: measurement and simulation of voltage-gated fluxes". Journal of Membrane Biology. 124 (3). ss. 265-73. doi:10.1007/BF01994359. PMID 1664861.
- ^ Schmidt-Nielsen, p. 483.
- ^ Lieb WR, Stein WD (1986). "Chapter 2. Simple Diffusion across the Membrane Barrier". Transport and Diffusion across Cell Membranes. San Diego: Academic Press. ss. 69-112. ISBN 0-12-664661-9.
- ^ a b Hodgkin AL, Keynes RD (1955). "Active transport of cations in giant axons from Sepia and Loligo". J. Physiol. 128 (1). ss. 28-60. doi:10.1113/jphysiol.1955.sp005290. PMC 1365754 $2. PMID 14368574.
- ^ Caldwell PC, Hodgkin AL, Keynes RD, Shaw TI (1960). "The effects of injecting energy-rich phosphate compounds on the active transport of ions in the giant axons of Loligo". J. Physiol. 152 (3). ss. 561-90. PMC 1363339 $2. PMID 13806926.
- ^ Steinbach HB, Spiegelman S (1943). "The sodium and potassium balance in squid nerve axoplasm". J. Cell. Comp. Physiol. 22 (2). ss. 187-96. doi:10.1002/jcp.1030220209.
- ^ a b Hodgkin AL (1951). "The ionic basis of electrical activity in nerve and muscle". Biol. Rev. 26 (4). ss. 339-409. doi:10.1111/j.1469-185X.1951.tb01204.x.
- ^ CRC Handbook of Chemistry and Physics, 83rd edition, ISBN 0-8493-0483-0, pp. 12–14 to 12–16.
- ^ Eisenman G (1961). "On the elementary atomic origin of equilibrium ionic specificity". A Kleinzeller, A Kotyk, eds. (Ed.). Symposium on Membrane Transport and Metabolism. New York: Academic Press. ss. 163-79.
- ^ Junge, pp. 33–37.
- ^ Cai SQ, Li W, Sesti F (2007). "Multiple modes of a-type potassium current regulation". Curr. Pharm. Des. 13 (31). ss. 3178-84. doi:10.2174/138161207782341286. PMID 18045167.
- ^ Goldin AL (2007). "Neuronal Channels and Receptors". Waxman SG (Ed.). Molecular Neurology. Burlington, MA: Elsevier Academic Press. ss. 43-58. ISBN 978-0-12-369509-3.
- ^ Purves et al., pp. 28–32; Bullock, Orkand, and Grinnell, pp. 133–134; Schmidt-Nielsen, pp. 478–480, 596–597; Junge, pp. 33–35
- ^ Franco R, Bortner CD, Cidlowski JA (Ocak 2006). "Potential roles of electrogenic ion transport and plasma membrane depolarization in apoptosis". J. Membr. Biol. 209 (1). ss. 43-58. doi:10.1007/s00232-005-0837-5. PMID 16685600.
- ^ Purves et al., pp. 32–33; Bullock, Orkand, and Grinnell, pp. 138–140; Schmidt-Nielsen, pp. 480; Junge, pp. 35–37
- ^ Spangler SG (1972). "Expansion of the constant field equation to include both divalent and monovalent ions". Ala J Med Sci. 9 (2). ss. 218-23. PMID 5045041.
- ^ Purves et al., p. 34; Bullock, Orkand, and Grinnell, p. 134; Schmidt-Nielsen, pp. 478–480.
- ^ Purves et al., pp. 33–36; Bullock, Orkand, and Grinnell, p. 131.
- ^ a b Magnuson DS, Morassutti DJ, Staines WA, McBurney MW, Marshall KC. (14 Ocak 1995). "In vivo electrophysiological maturation of neurons derived from a multipotent precursor (embryonal carcinoma) cell line". Brain Res Dev Brain Res. 84 (1). ss. 130-41. doi:10.1016/0165-3806(94)00166-W. PMID 7720212.
- ^ Juusola M, Kouvalainen E, Järvilehto M, Weckström M. (Sep 1994). "Contrast gain, signal-to-noise ratio, and linearity in light-adapted blowfly photoreceptors". J Gen Physiol. 104 (3). ss. 593-621. doi:10.1085/jgp.104.3.593. PMC 2229225 $2. PMID 7807062.
- ^ Laughlin SB, de Ruyter van Steveninck RR, Anderson JC (Mayıs 1998). "The metabolic cost of neural information". Nat Neurosci. 1 (1). ss. 36-41. doi:10.1038/236. PMID 10195106.
Konuyla ilgili yayınlar[değiştir | kaynağı değiştir]
- Alberts ve ark. Moleküler Biyoloji Hücre. Garland Yayıncılık; 4. Bk&Cdr baskı (Mart 2002). ISBN 0-8153-3218-1. Lisans düzeyinde.
- Guyton, Arthur C., John E. Hall. Ders Kitabı tıbbi Fizyoloji. W. B. Saunders Company; 10th edition (15 Ağustos 2000). ISBN 0-7216-8677-X. Lisans düzeyinde.
- Hille, B. İyonik Kanal Uyarılabilir Membranlar Sinauer Associates, Sunderland, MA, USA, 1. Baskı, 1984. ISBN 0-87893-322-0
- Nicholls, J. G., Martin, A. R. ve Wallace, B. G. Dan Nöron Beyin Sinauer Associates, Inc. Sunderland, MA, USA 3rd Edition, 1992. ISBN 0-87893-580-0
- Ove-Sten Knudsen. Biyolojik Membranlar: Teori Taşıma, Potansiyelleri ve Elektrik Darbeleri. Cambridge University Press (26 Eylül 2002). ISBN 0-521-81018-3. Üniversite düzeyinde.
- Bağımsız Çalışma ulusal Sağlık Serisi. Fizyoloji. Lippincott Williams & Wilkins. Philadelphia, PE, ABD 4. Baskı, 2001. ISBN 0-683-30603-0
Dış bağlantılar[değiştir | kaynağı değiştir]
- Nernst/Goldman Denklemi Simülatörü
- Nernst Denklemi Hesap Makinesi 4 Haziran 2016 tarihinde Wayback Machine sitesinde arşivlendi.
- Goldman-Hodgkin-Katz Denklemi Hesap Makinesi 5 Haziran 2016 tarihinde Wayback Machine sitesinde arşivlendi.
- Elektrokimyasal İtici Güç Hesap Makinesi 26 Mayıs 2016 tarihinde Wayback Machine sitesinde arşivlendi.
- Kökeni İstirahat Membran Potansiyeli 13 Mayıs 2016 tarihinde Wayback Machine sitesinde arşivlendi. - Çevrimiçi etkileşimli öğretici (Flash)

![{\displaystyle E_{eq,K^{+}}={\frac {RT}{zF}}\ln {\frac {[K^{+}]_{o}}{[K^{+}]_{i}}},}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b7eb1afcc5d7a5032ff24be5c403b43b1307b01e)
![{\displaystyle E_{m}={\frac {RT}{F}}\ln {\left({\frac {P_{\mathrm {K} }[\mathrm {K} ^{+}]_{\mathrm {out} }+P_{\mathrm {Na} }[\mathrm {Na} ^{+}]_{\mathrm {out} }+P_{\mathrm {Cl} }[\mathrm {Cl} ^{-}]_{\mathrm {in} }}{P_{\mathrm {K} }[\mathrm {K} ^{+}]_{\mathrm {in} }+P_{\mathrm {Na} }[\mathrm {Na} ^{+}]_{\mathrm {in} }+P_{\mathrm {Cl} }[\mathrm {Cl} ^{-}]_{\mathrm {out} }}}\right)}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/4b29151571b6fb807674bf342d01f178908a1a98)