Diazinon

| |
| |
| Adlandırmalar | |
|---|---|
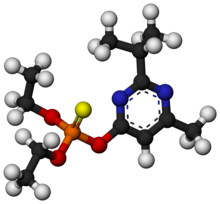
O,O-Diethyl O-[4-methyl-6-(propan-2-yl)pyrimidin-2-yl] phosphorothioate | |
Diğer adlar Dietoksi-[(2-izopropil-6-metil-4-pirimidinil)oksi]-tiyoksofosforan Basudin Diazide Spectracide | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA InfoCard | 100.005.795 |
| KEGG | |
PubChem CID
|
|
| UNII | |
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Kimyasal formül | C12H21N2O3PS |
| Molekül kütlesi | 304,35 g mol−1 |
| Görünüm | Koyu kahveden renksize kadar değişebilir |
| Koku | zayıf, ester gibi |
| Yoğunluk | 1.116-1.118 g/cm3 20 °C'de[1] |
| Kaynama noktası | bozunur[4] |
| Çözünürlük (su içinde) | 40 mg/L[2] |
| log P | 3.81 (oktanol/su)[3] |
| Farmakoloji | |
| P53AF03 (WHO) | |
| Tehlikeler | |
| Parlama noktası | 180°C [4] |
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz)
|
• 214 mg•kg−1 (insan, oral, TDLo) (2,3) • 66 mg•kg−1 (sıçan, oral, LD50) (2,4) |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | yok[4] IDLH = N.D.[4] REL = TWA 0.1 mg/m3 [deri][4] |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Diazinon, 1952'de bir İsviçreli kimya şirketi olan Ciba-Geigy(daha sonra Novartis ve Syngenta) tarafından geliştirilen koyu kahverengi bir tiyofosforik asit esterdir. Eskiden, hamamböceği, gümüş balığı, karıncalar ve pireleri konutlar ve binalarda kontrol etmek için kullanılan bir sistemik organofosfat insektisitidir. Diazinon, 1970'lerde ve 1980'lerin başında, genel amaçlı bahçe uygulamalarında ve iç mekan zararlısı kontrolünde yoğun bir şekilde kullanılmıştır. Batı ABD'de eşekarılarını kontrol etmek için yem formu kullanılmıştır. Avustralya ve Yeni Zelanda'da evcil hayvanlar için pire öldürücü olarak diazinon kullanılmıştır. Diazinon'un konut kullanımları 2004 yılında ABD'de yasaklanmıştır ancak tarımsal kullanımı için hala bir yasak yoktur. Acil durum antidotu atropindir.[5]
Tarihi[değiştir | kaynağı değiştir]
Diazinon, 1952 yılında İsviçre'deki Ciba-Geigy firması tarafından keşfedildi. Piyasada baskın olan DDT'nin yerini aldı. 1939'da, Geigy firmasından kimyacı Paul Hermann Müller, DDT'nin sıtma yayan böceklere karşı etkili olduğunu keşfetmişti. Bu yetenek DDT'nin, Müller'in 1948 Nobel Tıp Ödülü'nü almasına yetecek kadar önemli olduğunu göstermiştir.
Ancak, ödülü takip eden on yıllar geçtikçe, DDT'nin, gelişmiş ülkeler ve nihayetinde dünya çapındaki kuruluşlarca, çevresel bir tehlike olduğu bulunmuştur ve vektör böceklerle mücadele dışındaki tüm alternatif uygulamalarda insektisit olarak kullanımı yasaklanmıştır. Bu nedenle Ciba-Geigy firması alternatiflerini araştırmaya başlamıştır.
DDT üretimi düşerken Diazinon 1955'te kitlesel kullanım için uygun hale geldi. 1970'ten önce, diazinon çözeltilerinde kirleticilerle ilgili sorunlar vardı; ancak 1970'lerde, istenmeyen materyalleri azaltmak için alternatif arıtma yöntemleri kullanıldı.
Bu işlemden sonra, diazinon, çok amaçlı, iç ve dış mekan, ticari haşere kontrol ürünü haline geldi. 2004 yılında, ABD diazinonun konutlarda kullanımını yasakladı.
Yapı ve reaktivitesi[değiştir | kaynağı değiştir]
Diazononun yapısı bir tiyofosforik ester içerir. Fosfor merkezi, kimyasalın reaktif bölgesidir. Bununla birlikte, şu anda bilinen hiçbir mekanizma mevcut değildir. Sülfürün, bir hidroksit grubunu fosfor merkezine ileten ve kolayca reaksiyona girebilen bir hidronyum iyonu yoluyla sülfürün asidik ortamda protonlanmasını öneren yeni bir mekanizma vardır.
Diazinonun formları tozlar, granüller, sıvılar, konsantreler, mikrokapsüllemeler, ıslatılabilir tozlar ve tohum sargılarında olabileceği gibi geniş çapta değişir. Görünüşü, koyu kahverengiden (endüstriyel sınıf), renksiz bir sıvıya (saf) kadar, saflığa bağlı olarak değişir.
Diazinon, standart ortam sıcaklığı ve basıncı altında nispeten stabildir, ancak ısıtıldığında toksik fosfin gazı oluşturmaya yatkındır. Ayrıca, güçlü bir oksitleyici ajan varlığında diazinon toksik fosfor oksitlere oksitlenebilir.
Metabolizma ve etki mekanizması[değiştir | kaynağı değiştir]
Diazinon, bir asetilkolinesteraz enzimi inhibitörü olarak işlev görür. Bu enzim, nörotransmitter asetilkolini, kolin ve bir asetat grubuna ayırır. (1) Asetilkolinesteraz enzimi inhibisyonu sinaptik yarıkta anormal bir asetilkolin birikimine neden olur.
Diazinon vücuda girdiğinde, diazinondan çok daha zehirli olan ve esas olarak Asetilkolinesteraz enziminin inhibe edilmesine neden olan bir organofosfat bileşiği olan diazoksona oksidatif olarak dejenere olur. (6) Diazinonun aktivasyonu(reaksiyon 1) karaciğer mikrozomal enzim sisteminde olur ve O2 ve NADPH gerektirir. Ek olarak, mikrozomal enzim sisteminde oksidasyon yoluyla dejenere olabilir (Reaksiyon 2). Her iki reaksiyon da mümkündür ve muhtemelen aynı anda spesifik olmayan şekilde katalize edilir. Oluşturulduktan sonra diazokson, dejenere olduğu için tekrar biyotransformasyona uğrar.
Diazoxon, karaciğerdeki mikrozomal ve diğer alt hücresel gruplardaki çok etkili hidrolizatlara bağlı olarak dejenere olur (Reaksiyon 3). Memeli türleri, diazoksonu çok daha yavaş bir oranda (2 ila 6 haftalık bir yarı ömür ile) dejenere eder. Böcekler zehirli formların hızla birikmesine izin veren bu hidroliz aşamasından yoksundur. Diazozonun detoksifikasyonu, mirosomal karışık fonksiyon oksidaz sistemi ile işlenir. Tam olarak bilinmemekle birlikte, bunun, diazinonun böceklere karşı seçiciliğinin sebebi olduğuna inanılmaktadır. Hidroliz veya oksidasyondan sonra diazinon daha fazla dejenere olur (Reaksiyon 4).

Toksisite ve hayvanlar üzerindeki etkileri[değiştir | kaynağı değiştir]
Diazinon, omurgalılar için nispeten yüksek toksik olarak kabul edilir. İnhalasyonu mümkün olsa da, diazinonun zehirlenmesine yönelik yaygın yol emilimdir. Gözlemlenen toksikasyon semptomları diğer asetilkolinesteraz inhibitörlerine uygundur. Belirtiler aşağıdaki gibidir:
- Kolik(bağırsaklarda ağrı)
- İshal ve / veya kusma
- Baş dönmesi
- Baş ağrısı
- Miosis
- Bradikardi
- Kan basıncında ani düşüş
- Çırpınma
- Apne
| Lethal Doz | Gözlemler |
|---|---|
| LD50 |
|
İnsanlarda belirtileri[değiştir | kaynağı değiştir]
- Gözler, kulaklar, burun ve boğaz:
- Küçük gözbebekleri(ışığa karşı tepki vermez)
- Kardiyovasküler:
- Düşük veya yüksek tansiyon
- Yavaş veya hızlı kalp atış hızı
- Solunum:
- Solunum güçlüğü
- Göğüste sıkışma
- Sinir sistemi:
- Kaygı
- Konvülsiyon
- Koma
- Baş dönmesi
- Heyecanlanma
- Baş ağrısı
- Zayıflık
- Titreme
- Seğirme
- Cilt
- Tahriş
- Kızarıklık
- Terleme
- Mide-bağırsak sistemi
- Karın krampları
- İshal
- İştah kaybı
- Mide bulantısı
- Kusma
Tipik olarak tedaviler, maruz kalmaya veya toksinin verilme yöntemine bağlı olarak değişecektir. Hastayı detoks ederken idrar örnekleri, kan içeriği ve kalp hızları gibi kritik biyobelirteçler ölçülür. Diazinon zehirlenmesinden muzdarip hastalar için yaygın tedaviler şunlardır:
- Yardımlı Solunum
- İntravenöz sıvılar (IV)
- Cildin ve gözlerin yıkanması
- Tıbbi Tedaviler; antidotlar atropin ve oksim dahil.
- Gastrik Lavaj
İlk 4 ila 6 saatte (tıbbi tedaviden sonra) iyileşmeye devam eden hastalar genellikle iyileşir. Genellikle uzun süreli tedavi gereklidir. Bazı toksisiteler haftalar, aylar veya daha uzun süre devam edebilir.
Ayrıca bakınız[değiştir | kaynağı değiştir]
Kaynakça[değiştir | kaynağı değiştir]
- ^ Budavari, S., (Ed.) (1996). The Merck Index - An Encyclopedia of Chemicals, Drugs, and Biologicals. Whitehouse Station, NJ: Merck. s. 508.
- ^ Sharom, M.S.; Miles, J.R.W.; Harris, C.R.; McEwen, F.L. (1980). "Behaviour of 12 insecticides in soil and aqueous suspensions of soil and sediment". Water Research. 14 (8). ss. 1095-100. doi:10.1016/0043-1354(80)90158-X.
- ^ Hansch, Corwin; Leo, Albert; Hoekman, David (1995). Exploring QSAR: Volume 2: Hydrophobic, Electronic, and Steric Constants. Washington, DC: American Chemical Society. s. 106. ISBN 978-0-8412-2991-4.
- ^ a b c d e NIOSH Pocket Guide to Chemical Hazards. "#0181". National Institute for Occupational Safety and Health (NIOSH).
- ^ Geller, Robert J.; Lopez, Gaylord P.; Cutler, Stephen; Lin, Diana; Bachman, George F.; Gorman, Susan E. (2003). "Atropine availability as an antidote for nerve agent casualties: Validated rapid reformulation of high-concentration atropine from bulk powder". Annals of Emergency Medicine. 41 (4). ss. 453-6. doi:10.1067/mem.2003.103. PMID 12658242.
