DNA onarımı
Bu maddede kaynak listesi bulunmasına karşın metin içi kaynakların yetersizliği nedeniyle bazı bilgilerin hangi kaynaktan alındığı belirsizdir. (Haziran 2016) (Bu şablonun nasıl ve ne zaman kaldırılması gerektiğini öğrenin) |
DNA onarımı, DNA moleküllerindeki hataları onarım mekanizmalarını tanımlamaktadır. İnsan hücrelerinde metabolik aktiviteler ve çevresel faktörler (UV ışığı gibi) sonucu günde 1 milyon hücrenin zarar görmesi olasıdır. Bu etkenler, DNA'nın yapısını ve dahası diğer nesillere aktarılan genetik bilgiyi değiştirebilirler. Bu değişimler yararlı olabileceği gibi, ölümcül sonuçlara neden olabilecek kadar da zararlı olabilir. Bu yüzden, bütün canlı hücreleri, evrim süreçleri boyunca nesillere değişmeden aktarılması gereken DNA molekülünü koruma mekanizmaları geliştirmişlerdir.[1]
Küçük hasarlar çoğunlukla DNA onarım sistemleri tarafından onarılır. Yüksek düzeydeki hasarlar apoptozisi uyararak "hücre ölümüne" yol açar. Böylelikle organizma kendini korumuş olur. Orta derecedeki hasarların birikimi ise mutasyonlara neden olur.
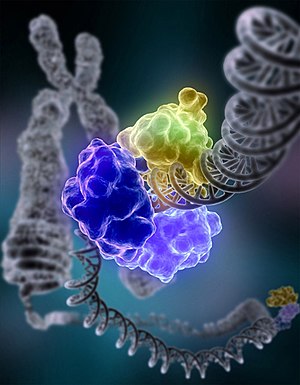
Hücre tüm bu DNA hasarlarına farklı metabolik yollar ile cevap verir. Ağır DNA hasarları hücrenin apoptozis yolunu aktive ederek hücreyi ölüme götürür. Hücre, DNA hasarlarını "DNA tamir mekanizmaları" ile tamir edebilir. DNA hasarı ikileşme sırasında tamir edilemezse mutasyona ve sonuç olarak genomik kararsızlığa, kanser ve yaşlanmaya neden olur.[2]
DNA tamir sisteminde 100’den fazla gen rol oynar ve bu genlerin kodladığı proteinler tamir mekanizmalarında görev alırlar. Her bir insan hücresinin DNA'sında günde yaklaşık olarak 104 adet kodlanmayan veya yanlış kodlamaya neden olan hasar meydana gelmektedir. Mitokondrial DNA'da nokta mutasyonlarının birikiminin yaşa bağlı olarak arttığı, bu nedenle özellikle mitokondrideki oksidalif DNA hasarının yaşlanma ile ilişkili olduğu düşünülmektedir. DNA tamir mekanizmaları genomik kararlılığın devamını sağlayan sistemlerdir.
2015 Nobel Kimya Ödülü DNA onarımı proseslerinin moleküler mekanikleri üzerine çalışmaları nedeniyle Tomas Lindahl, Paul Modrich ve Aziz Sancar'a verilmiştir.[3][4]
Direkt tamir mekanizmaları[değiştir | kaynağı değiştir]
Fotoreaktivasyon[değiştir | kaynağı değiştir]
UV ile meydana gelen mutasyonları içeren hücreler, mavi spektrum (300–500 nm) içeren görünür ışığa maruz bırakıldıklarında, geriye dönüşüm yapıp düzelir. Bu olaya fotoreaktivasyon denir. Evrimsel süreçte bu sistem korunarak gelmiştir. Işık (300–500 nm) ve iki kromoforu sayesinde 'DNA Fotoliaz' enzimi aktive olarak bu dönüşümü gerçekleştirir. Bu enzim hem prokaryotlarda hem de ökaryotlarda bulunur.
O6-Metilguanin Tamiri[değiştir | kaynağı değiştir]
O6-Metilguanin (mG) alkilleyici ajanlar varlığında oluşur ve yüksek oranda mutajeniktir. O6-Metilguanin-DNA metil transferaz enzimi, DNA’daki yanlış metillenen bazların CH3 gruplarını kendi sistein rezidülerine transfer ederek normal Guanin oluşumunu sağlar. Bunu yaparken enzim de geri dönüşümsüz olarak baskılanmış olur ve işlev dışı kalır. Böylece bu onarımda enzimin özgünlüğü kadar sayısı da önem kazanmaktadır.
Basit Tek Zincir Kırıklarının Ligasyonu[değiştir | kaynağı değiştir]
X-ışını ya da peroksitler gibi bazı ajanlar DNA zincirinde basit kırıklara neden olabilmektedir. Bir zincirde olan basit kırıklar DNA ligaz enzimi ile hemen tamir edilmektedir. DNA ligaz; enerji gerektiren bir reaksiyon ile 5' fosfat grubu ile 3'OH grubu arasındaki fosfodiester bağını oluşturur.
Kesip-Çıkarma Tamirleri(Ekzisyon)[değiştir | kaynağı değiştir]
Tüm prokaryot ve ökaryot organizmalarda bulunan bu tip tamir sistemi 3 temel basamak içerir:
- Hasar veya hata tanınır ve enzimatik olarak bir nükleaz tarafından kesip çıkarılır.
- DNA polimeraz oluşan boşlukları doldurur.
- DNA ligaz son bağı kurar ve boşluk tamamen kapanır.
Baz eksizyon tamiri (BER)[değiştir | kaynağı değiştir]
Baz Eksizyon Tamiri, DNA bazlarının doğal hidrolizi veya kimyasal ajanlar nedeni ile oluşan uygun olmayan bazların tamiri ile ilgilidir. BER’de görev alan enzim DNA glikozilazdır. Spontan veya kimyasallarla olan deaminasyon veya iyonize radyasyon ve oksidatif hasar sonucu oluşan baz değişikliklerine spesifiktir (urasil, hipoksantin, 3-metiladenin vb.). DNA glikozilaz, uygun olmayan bazı tanır. Deoksiriboz şeker ve baz arasındaki N-glikozidik bağın hidrolizi ile uzaklaştırır. Lezyona spesifik glikozilaz enzim formu kullanılır (Örn: Urasil-DNA glikozilaz). Abazik (apirimidinik ya da apürinik) bölge oluşur (AP bölge). AP bölgeyi spesifik AP endonükleaz enzimleri tanır ve bu zincirde bir çentik açar. Ekzonükleaz enzimi fosfat ve şekeri ayırır. Oluşan boşluk DNA polimeraz ile doldurulur ve ligaz ile fosfodiester bağlantı sağlanır (Glikozilaz, metillenmiş sitozinden amino grubunun uzaklaşmasıyla oluşan timini DNA’dan çıkartamaz, çünkü timin DNA için normal bir bazdır).
Nükleotid eksizyon tamiri (NER)[değiştir | kaynağı değiştir]
DNA'nın sarmal yapısında geniş bozulmalara neden olan DNA lezyonları NER sistemi ile onarılır. UV kaynaklı pirimidin dimerleri, sigara nedenli benzopiren-guanin gibi baz değişimleri, kemoterapötik ilaçlarla oluşan baz değişimleri BER’de bazlar tek olarak kesip çıkarılırken, NER’de hasarlı bazlar oligonükleotid parçaları olarak kesip çıkarılır. Prokaryotlarda anahtar enzimatik kompleks ABC ekzinükleazdır. 3 altünitesi vardır.:
- uvr A,
- uvr B,
- uvr C)
Sistem şu şekilde işler; uvr A - uvr B kompleksi DNA’yı tarar ve hasar bulunduğunda DNA’ya bağlanır. uvr A ayrılır, uvr C - uvr B kompleksi oluşur. uvr C; hasarın 3' ucuna 4–5 nükleotid, 5' ucuna 8 nükleotid uzaktan çentikler açar. DNA helikaz (uvr D) bu 12–13 nükleotidlik parçası uzaklaştırır. İnsanda NER mekanizması çok daha karmaşıktır.
Ekzinükleaz aktivitesi birçok gen tarafından kodlanan proteinlerce gerçekleştirilir. DNA’daki hasar XPA proteini ile tanınır ve diğer proteinlerin bu bölgeye gelmeleri sağlanır. [Transkripsiyon faktörü II H (TFIIH), XPA ve replikasyon proteini A (RPA)] TFIIH’nin alt birimlerinden XPB ve XPD’nin helikaz aktiviteleri ile DNA zincirinde 20 nükleotidlik bir bölge açılır (unwinding). XPG proteini 3' uç bölgesinde hasardan 6 nükleotid uzaktan, XPF/ERCC1 protein kompleksi ise 5' uç bölgesinde hasardan 22 nükleotid uzaktan DNA zincirini keser. Serbest kalan 27–29 nükleotidlik parça uzaklaştırılır.
Nükleotid eksizyon tamir genleri[değiştir | kaynağı değiştir]
Memelilerde eksizyon tamir yolunun moleküler mekanizmasını araştırmak amacıyla NER hasarı olan iki mutant hücre hattı kullanılmıştır: Laboratuvarda oluşturulan UV'ye duyarlı hamster hücre hatları ve doğal insan mutantları XP, CS ve TTD'nin hücre hatları. Hücre füzyon çalışmaları sonucunda XP'da XPA, XPB, XPC, XPD, XPE, XPF ve XPG olmak üzere 7; CS' de iki (CSA ve CSB); TTD' de ise üç (XPB, XPD ve TTD A) komplementasyon grubu tanımlanmıştır. Bu hasta gruplarının hücre hatlarına ek olarak, mutant hamster hücre hatları arasında 11 komplementasyon grubu tanımlanmıştır. Mutant hamster hücrelerinin insan genomik DNA ile transfeksiyonu sonucunda insan DNA’sı ile hamster hücrelerinin mutant fenotipi düzeltilmiş ve ERCC (excision repair cross complementing) genleri tanımlanmıştır. Komplementasyon analizleri ERCC2'nin XPD, ERCC3'ün XPB, ERCC5'in XPG ve ERCC6'nın CSB geni ile benzer olduğunu ortaya çıkarmıştır.
Nükleotid eksizyon tamir mekanizması[değiştir | kaynağı değiştir]
Son yıllarda yapılan araştırmalar, eşleşmeyen DNA zincirindeki DNA adüktlerinin XPC/hHR23B kompleksi ile tanındığını ortaya koymuştur. XPC/hHR23B kompleksinin hasara bağlanması DNA yapısının kısmen açılmasına neden olmakta ve tamir mekanizmasında görev alan diğer proteinlerin bu bölgeye toplanmasını ve bağlanmasını sağlamaktadır. DNA zincirindeki bu açılma, Transkripsiyon faktörü II H (TFIIH)'nin, XPA ve replikasyon proteini A (RPA)'nın, hasarlı bölgeye girerek açık DNA kompleksini meydana getirmesine neden olmaktadır. Transkripsiyonda ve DNA tamirinde görev alan TFIIH 9 alt biriminden meydana gelmektedir ve alt birimlerden XPB 3'→5' ve XPD 5'→3' helikaz aktivitelerine sahiptir. Helikaz aktiviteleri nedeniyle, TFIIH DNA zincirinin 20-30 nükleotidlik bir bölgenin açılmasını sağlar. Daha sonra, hasarlı zincir üzerinde sırayla kesim olayı gerçekleşir. XPG proteini 3' bölgesinde, hasardan 2-8 nükleotid uzaklıktan keser.
XPF/ERCC1 ise 5' bölgesinde hasardan 15-24 nükleotid uzaklıktan keser. Hasarlı bölgeyi içeren 24-32 nükleotidlik oligonükleotid serbest bırakılır. Serbest bırakılan bu oligonükleotid, hasarı tanıyan proteinlerden XPC/hHR23B proteinine bağlı olarak ortamdan uzaklaştırılır. DNA zincirindeki boşluk, DNA replikasyon faktörü C (RFC), prolifere edici hücre nükleer antijeni (PCNA) ve DNA polimerazlar δ ve ε ile doldurulur. PCNA, RFC ile birlikte DNA kalıbı üzerine DNA polimerazlar δ ve ε 'un yüklenmesini sağlar. NER mekanizmasındaki son basamak, PCNA proteininin ayrılması ve ligaz I enzimi ile yeni sentezlenen DNA zincirinin ligasyonudur.
Transkripsiyona kenetlenmiş tamir mekanizması[değiştir | kaynağı değiştir]
İnsan tamir genlerinin tanımlanması ve klonlanmasıyla DNA tamiri ve transkripsiyon arasındaki moleküler ilişki açıklık kazanmıştır. Yapılan araştırmalar, genlerin okunan zincirinin okunmayan zincirden daha hızlı bir şekilde NER yoluyla tamir edildiğini ortaya koymuştur. Transkripsiyon sırasında RNA polimeraz II, DNA zincirinde hasarla karşılaştığında RNA sentezi durur ve TCR yolu bu hasarın tamirinde rol oynar. TCR mekanizmasında, GGR yolundan farklı olarak hasarın tanınma basamağında XPC/hHR23B kompleksi yerine CSB proteini rol oynar. CSB proteini, RNA polimeraz II'yi ubiquitin ile birleştirerek parçalanmasını ve böylece TFIIH, XPA ve RPA proteinlerinin hasarlı bölgeye ulaşmasını sağlar. TCR yolundaki diğer basamaklar GGR yolundaki basamaklar ile aynıdır.
NER mekanizmasında rol alan proteinlerdeki bozukluklar sonucunda bazı nadir görülen hastalıklar tanımlanmıştır;
- Xeroderma pigmentosum (XP proteinleri)
- Cockayne sendromu (CSA-CSB)
- Trikotiyodistrofi (XP proteinleri)
Yanlış eşleşme eksizyon tamiri (MER)[değiştir | kaynağı değiştir]
DNA polimeraz, replikasyon sırasında prova okuması (proofreading) yeteneğine sahiptir. Mismatch eksizyon tamiri, hata okuma sonrası bile kalan yanlış eşleşmeleri tamir eden mekanizmadır.
Prokaryotlarda MutS yanlış eşleşmeyi algılar ve bölgeye bağlanır. MutL nin bağlanması ile kopmpleks kararlılık kazanır. MutS-MutL kompleksi MutH yi aktive eder. MutH yakın bölgedeki metil grubu ekler ve karşı zincirde kesik oluşturur. UvrD (Helicase II) proteini kesip-çıkarma işlemine yardımcı olur. DNA pol boşluğu doldurur ve DNA ligaz yapıştırır.
Rekombinasyonal tamir[değiştir | kaynağı değiştir]
DNA hasarı diğer tamir sistemleri ile tamir edilememişse, replikasyondan sonra aktif olan mekanizmadır. Bir lezyon bulunduran DNA replike olurken, DNA polimeraz önce lezyonda duraklar. Hasarlı bölgeyi de içine alacak şekilde boşluk bırakarak atlar ve senteze devam eder. Rec A proteini, rekombinasyonal bir değiş tokuş işlemi ile hasarsız komplementer zincirde bulunan sekansı transfer eder. Komplementer zincirde oluşan boşluk DNA polimeraz – DNA ligaz enzimleri sayesinde doldurulur. Halen bulunan lezyon diğer tamir sistemleri ile onarılır.

SOS tamiri[değiştir | kaynağı değiştir]
DNA hasarının yüksek oranda olduğu ve diğer tamir mekanizmalarının başarılı olamadığı durumlarda devreye giren acil cevap sistemidir. DNA sentezi sırasında, bir lezyonun üzerinden atlamak yerine, sistem, DNA polimerazın lezyon karşısında replikasyonu devam ettirmesini sağlar. Fakat replikasyonun doğruluğundan fedakârlık edilir. Bu nedenle hataya meyilli sistem de denir. SOS yanıtında görev alan birçok proteini kodlayan genler normalde Lex A proteini tarafından baskılanmış durumdadır. DNA hasarı ile karşılaşıldığında, Rec A proteini hasarlı tek zincire bağlanır ve Rec A-ssDNA kompleksi oluşur. Rec A, DNA’ya bağlandıktan sonra Lex A proteininin otoproteolitik yıkımını aktive eder. Rec A, DNA polimeraza bağlanır ve lezyonu da geçerek DNA’yı replike etmesini sağlar. umu C-umu D kompleksi etkisiyle ve Rec A’nın, polimerazın 3'→5' ekzonükleaz (hata okuma ve çıkarma) aktivitesini inhibe etmesiyle translezyon replikasyon gerçekleşir. Hataya meyilli tamir sistemidir.
Çift zincir kırıklarının tamiri[değiştir | kaynağı değiştir]
İyonize radyasyon, oksidatif hasar sonucu veya doğal oluşan DNA çift zincir kırıkları iki şekilde tamir edilir;
- Serbest uçların homolog olmayan şekilde bağlanması (non-homolog end joining) (NHEJ)
- Homolog rekombinasyon
Serbest uçların homolog olmayan bağlanması (NHEJ)[değiştir | kaynağı değiştir]
Hızlı ve hataya meyilli bir sistemdir. Ku 70-Ku 80 kompleksleri DNA kırık uçlarına bağlanırlar. Serbest iki DNA ucu tamir edilene kadar bir arada tutulurlar (sinapsis). DNA bağımlı protein kinaz aktive olarak diğer proteinlerin hasar bölgesine gelmelerini sağlar. Bu protein komplekslerinin formasyonu DNA ligaz IV-XRCC4 kompleksinin kırık uçları bağlamasını sağlar.
NHEJ tamir yolundaki hataların çeşitli kanserler ile ilişkili translokasyonlara neden olduğu gösterilmiştir. Burkitt lenfoma, kronik myeloid lösemideki Philadelphia kromozomu bunlardandır. Homolog rekombinasyonda görev alan BRCA1 ve BRCA2 genlerinde olan mutasyonlar ile meme ve rahim kanserleri arasında ilişki bulunmuştur.
Homolog rekombinasyon[değiştir | kaynağı değiştir]
RAD ve BRCA genleri tarafından yönlendirilir. MRE11-RAD50-NBS1 kompleksinin nükleaz aktivitesi ile kırık uçları degredasyona uğrar. RAD 52 proteini 3' uçlara bağlanır. RAD 51- BRCA 2 kompleksi, rekombinasyon oluşturmak üzere kardeş kromatid zincirinin hasar bölgesine invazyonunu sağlar. Bu zincir kalıp olarak kullanılarak sentez yapılır ve hasar onarılır (DNA polimeraz – DNA ligaz).
Kaynakça[değiştir | kaynağı değiştir]
Dış bağlantılar[değiştir | kaynağı değiştir]
- Roswell Park Cancer Institute DNA Repair Lectures
- A comprehensive list of Human DNA Repair Genes
- 3D structures of some DNA repair enzymes
- Human DNA repair diseases17 Temmuz 2012 tarihinde Wayback Machine sitesinde arşivlendi.
- DNA repair special interest group
- DNA Repair12 Şubat 2018 tarihinde Wayback Machine sitesinde arşivlendi.
- DNA Damage and DNA Repair25 Şubat 2010 tarihinde Wayback Machine sitesinde arşivlendi.
- Segmental Progeria25 Şubat 2010 tarihinde Wayback Machine sitesinde arşivlendi.
- DNA-damage repair; the good, the bad, and the ugly3 Mart 2016 tarihinde Wayback Machine sitesinde arşivlendi.
Kaynakça[değiştir | kaynağı değiştir]
* Türk Biyokimya Dergisi, 2000, Cilt:25, Sayı:2
- Türk Biyokimya Dergisi [Turkish Journal of Biochemistry - Turk J Biochem] 15 July, 2003; 28 (1); 20-24
- Balajee AS, Bohr VA. (2000) Genomic Heterogeneity of Nucleotide Excision Repair. Gene 250, 15-30
- Hoeijmakers JHJ. (1993) Nucleotide Excision Repair II: from E.coli to Yeast. Trends Genet 9, 211-217
- Friwdberg, EC, DNA Repair and Mutagenesis, ASM pr. Washington, DC, 1995
- Capy, P., A Plastic Genome, Nature, 396, 522-523, 1998
- Strauss,BS., Frameshift Mutation, Microsatellites and Mismatch Mepairs, Mutat Res., 437, 195-203, 1999
- Francino MP., Ochman H., Strand Asymmetries in DNA Evolution, TIG, 13(6), 240-245, 1997
- ^ The isolation and partial characterization of age-correlated oligo-deoxyribo-ribonucleotides with covalently linked aspartyl-glutamyl polypeptides" (1971). "5055816". Johns Hopkins medical journal. Supplement. 11 Mayıs 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Aralık 2017.
- ^ ""Nobel Prize in Chemistry Awarded to Tomas Lindahl, Paul Modrich and Aziz Sancar for DNA Studies"". 29 Temmuz 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 3 Aralık 2017.
- ^ Broad, William J. (7 Ekim 2015). "Nobel Prize in Chemistry Awarded to Tomas Lindahl, Paul Modrich and Aziz Sancar for DNA Studies". New York Times. 7 Ekim 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 7 Ekim 2015.
- ^ Staff (7 Ekim 2015). "THE NOBEL PRIZE IN CHEMISTRY 2015 - DNA repair – providing chemical stability for life" (PDF). Nobel Prize. 16 Haziran 2018 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 7 Ekim 2015.
