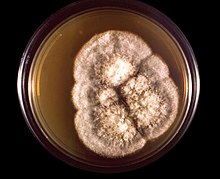
Coccidioides immitis
| Coccidioides immitis | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Biyolojik sınıflandırma | ||||||||||||
| ||||||||||||
Coccidioides immitis
G.W.Stiles (1896) | ||||||||||||
| Sinonimler [1] | ||||||||||||


Coccidioides immitis, güneybatı Amerika Birleşik Devletlerinin, kuzey Meksika'nın ve Batı yarımkürede başka birkaç bölgede toprakta bulunan patojenik bir mantardır.[2]
Epidemiyoloji
[değiştir | kaynağı değiştir]C. immitis'in C. posadasii ile akraba olmasının yanı sıra[3] bu tür en yaygın olarak Arizona, Kaliforniya, New Mexico, Nevada, Texas ve Utah'ın bazı alanları da içinde olmak üzere güneybatı ABD'nin çöl bölgelerinde ve Orta ve Güney Amerika'daki Arjantin, Brezilya, Kolombiya, Guatemala, Honduras, Meksika, Nikaragua, Paraguay ve Venezuela'da görülmektedir.[4]
Kesin konumları
[değiştir | kaynağı değiştir]C. immitis büyük ölçüde Kaliforniya'da bulunmayıp Baja California ve Arizona'da bulunurken, C. posadasii Teksas, kuzey Meksika ve Orta ve Güney Amerika'da kesintisiz bir biçimde bulunur. Arizona'da hem C. immitis, hem de C. posadasii bulunur.[5] C. immitis, Tehachapi dağlarının batısında daha yaygın iken, doğuda yaygın olan posadasii'dir.[6] Coccidioides türleri sıcak yazları ve yumuşak kışları olan ve yıllık yağış miktarı 10–50 cm arasında olan yarı çöl bölgelerden gelen alkali, kumlu topraklarda bulunur. Bu mantarlar genellikle yüzeyin 10 ila 30 santimetre altında bulunur.[7]
Klinik tablosu
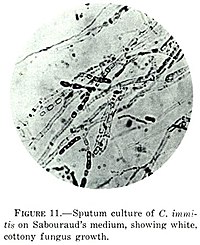
[değiştir | kaynağı değiştir]C. immitis, koksidiyoidomikoz (vadi ateşi) adı verilen bir hastalığa neden olabilir.[8][9][10] Kuluçka süresi 7 ila 21 gün arasında değişmektedir.[11] Koksidiyoidomikozun genellikle belirsiz ve özgül olmayan yaşamsal belirtiler ve semptomlar zemininde kolayca tanısı konulamaz. Göğüs röntgeniyle veya BT taramasıyla bile akciğer kanseri de içinde olmak üzere diğer akciğer hastalıklarından güvenilir bir biçimde ayrımı yapılamamaktadır. Coccidioides antijenlerini saptamayı amaçlayan kan veya idrar tahlilleri uygulanmaktadır. Bununla birlikte Coccidioides, akciğerdeki bir tümörü taklit edebilen bir kitle oluşturduğundan dolayı, doğru tanı için bir doku örneği (biyopsi) gerekebilir. Ayrıca Gomori'nin metenamin gümüş boyası ile Coccidioides organizmasının doku içinde özgül kürelerinin varlığını doğrulanabilir. C. immitis mantarının hastadan alınan örneklerden kültürü yapılabilir, ancak kültürün büyümesi haftalar alabilir ve laboratuvar çalışanının bir bölümü bunun üzerinde çalışırken özel önlemler alması gerekmektedir (vidalı kapaklı şişeler ve steril taşıma başlıkları önerilmektedir).[12] İki belgelenmiş ölümle birlikte laboratuvar koşullarında görülen en sık onuncu enfeksiyon olduğu bildirilmektedir.[2] Ekim 2012'ye kadar C. immitis, hem ABD Sağlık ve Sosyal Hizmetler Bakanlığı, hem de ABD Tarım Bakanlığı tarafından seçilmiş bir etken olarak listelenmişti ve 3. düzey biyogüvenlik patojeni olarak kabul edilmiştir.
Tedavi
[değiştir | kaynağı değiştir]- Çoğu Coccidioides enfeksiyonu bir ila dört hafta arasında bir kuluçka dönemine sahiptir[2] ve belirli bir tedavi olmadan düzelir; az sayıda klinik çalışmada az şiddetli hastalıktaki sonuçları değerlendirmiştir.
- Hastalığın şiddetini değerlendirmek için yaygın olarak kullanılan göstergeler şunları içermektedir:[13]
- 1 aydan uzun süren sürekli ateş
- %10'dan fazla vücut ağırlığı kaybı
- 3 haftadan fazla süren yoğun gece terlemeleri
- Bir akciğerin yarısından fazlasını veya her iki akciğerin bölümlerini içeren infiltratlar
- Belirgin veya kalıcı hiler adenopati
- 1:16 veya daha yüksek antikoksidiyoidal kompleman fiksasyonu IgG'si titreleri
- Koksidiyoidal antijenlere karşı deride aşırı duyarlılığın olmaması
- Çalışmaya karşı yetersizlik
- 2 aydan fazla süren semptomlar
- Yayılma için risk faktörleri (tedaviye başlanması için gereken):
- Sütçocukluğu (infantlık) döneminde birincil enfeksiyon
- Gebelik sırasında birincil enfeksiyon, özellikle de üçüncü trimesterde veya post partum'dan (doğum sonrasından) hemen sonra
- İmmünosüpresyon (örn., HIV/AIDS hastaları, transplant (nakil) alıcıları, yüksek doz kortikosteroid alan hastalar, anti-tümör nekroz faktörü ilaçları alanlar)
- Diyabetes mellitus veya önceden var olan kardiyopulmoner hastalık da içinde olmak üzere kronik zayıflama veya altta yatan hastalık
- Yüksek aşılamaya maruziyet
- Filipinler, Siyahlar veya İspanyollar gibi belirli etnik kökenler
- 55 yaşından yukarıda olmak
Azoller
[değiştir | kaynağı değiştir]Azollerin uygulanması, koksidiyoidomikoz için tedavide bir devrim yaratmıştır[14] ve bu etkenler, tedavinin genellikle ilk adımıdır. Bununla birlikte, bu azollerin hiçbiri gebelik ve emzirme döneminde güvenli değildir, çünkü hayvan çalışmalarında bunların teratojenliği gösterilmiştir.
Azollerden ketokonazol, ABD Gıda ve İlaç İdaresi (FDA) tarafından koksidiyoidomikoz tedavisi için onaylanan tek maddedir. Bununla birlikte, başlangıçta meningeal olmayan akciğer dışı hastalığın uzun süreli tedavisinde kullanılmasına karşın, daha güçlü, daha az toksik triazoller (flukonazol ve itrakonazol) yerini almıştır. İtrakonazol (400 mg/gün) meningeal olmayan enfeksiyonun tedavisinde flukonazolünkine eşit bir etkinliğe sahip olduğu ve tedavi kesildikten sonra aynı nüks oranına sahip olduğu görülmektedir. Bununla birlikte itrakonazol, iskelet lezyonlarında daha iyi performans gösterirken flukonazol, pulmoner ve yumuşak doku enfeksiyonunda daha iyi performans göstermektedir. İtrakonazolün serum düzeyleri genellikle uzun süreli tedavinin başlangıcında elde edilir, çünkü emilimi bazen düzensiz ve öngörülemezdir. Komplikasyonlar hepatik işlev bozukluğunu içerebilir.
Flukonazole yanıt vermeyen hastalar için seçenekler kısıtlıdır. Bazı olgu bildirileri, birinci basamak tedaviye cevap vermeyen hastalığın tedavisinde üç yeni antifungal etkenin etkinliğini araştırmıştır: Posakonazol ve vorikonazol (flukonazole benzer yapıda triazol bileşikleri) ve kaspofungin (ekinokandin yapı sınıfının glukan sentez inhibitörü). Bununla birlikte, bu ilaçlar FDA onaylı değildir ve klinik çalışmalar bulunmamaktadır. Bir bildiride Coccidioides türlerinin duyarlılık testi, bu yeni ilaçlar da içinde olmak üzere çoğu antifungal etkene karşı tekbiçimli duyarlılığı ortaya çıkarmıştır.
Çok ciddi olgularda, hiçbir çalışma yapılmamasına karşın, amfoterisin B ile bir azolün kombinasyonu tedavisi önerilmiştir. Kaskofungin, flukonazol ile kombinasyon halinde, 31 yaşında, koksidiyoidal pnömonili bir Asyalı hastanın olgu sunumunda yararlı olarak belirtilmiştir. HIV ve koksidiyoidal menenjitli 23 yaşında siyah bir erkeğin bir olgu sunumunda amfoterisin B ve posakonazolün kombinasyon tedavisi klinik iyileşme sağlamıştır.
Posakonazol, Avrupa Komisyonu tarafından tedaviye yanıt vermeyen koksidiyoidomikoz için kurtarma tedavisi olarak onaylanmıştır. Daha ileri değerlendirme için klinik denemeler sürmektedir. Vorikonazol ile ayrıca tedaviye yanıt vermeyen olgular için kurtarma tedavisinde de çalışılmaktadır. Bir olgu sunumu, yayılmış koksidiyoidomikoz için kurtarma tedavisi olarak amfoterisin B ile kombinasyon halinde vorikonazolün başarılı olduğunu göstermiştir.
Bazı olgu sunumları, farklı sonuçlarla birlikte kaspofungin üzerinde çalışmıştır. Transplantasyon geçirmiş akut pulmoner koksidiyoidomikozlu bir hastada amfoterisin B uygulanmasını takiben 50 mg/gün kaspofungin umut verici sonuçlar göstermiştir. Yaygın koksidiyoidomikozlu bir hastada, yalnızca amfoterisin B ve kaspofungin ile birinci basamak tedavi, bir yanıt ortaya koyamamıştır, ancak hastaya flukonazol ile kombine edilmiş kaspofungin verildiğinde iyi sonuçlar elde edilmiştir. Yayınlanmış bir bildiride flukonazol, vorikonazol ve amfoterisin B ile geleneksel tedavinin başarısız olduğu yaygın ve meningeal koksidiyoidomikozlu bir hasta tanımlanmış; intravenöz 70 mg'lık bir yükleme dozundan sonra 50 mg/gün kaspofungin de başarısız olmuştur.
Amfoterisin
[değiştir | kaynağı değiştir]1957'de tanıtılan amfoterisin B, ciddi enfeksiyonlar için tercih edilen tedavi olmayı sürdürmektedir. Genellikle kötüleşen hastalık veya omurga gibi yaşamsal organlarda bulunan lezyonlar için yer edinmiştir. Klasik amfoterisin B deoksikolat formülünde veya bir lipit formülü olarak uygulanabilir. Hiçbir çalışma amfoterisin B'yi azol tedavisi ile doğrudan karşılaştırmamıştır. Komplikasyonlar arasında böbrek toksisitesi, kemik iliği toksisitesi ve lokal sistemik etkiler (ateş, katılık) bulunur.
Tedavi süresi ve maliyetleri
[değiştir | kaynağı değiştir]Tedavinin amaçları enfeksiyonun giderilmesi, antikor titrelerinin azaltılması, ilgili organların işlevlerinin geri dönüşü ve tekrarın önlenmesidir. Tedavi süresi, hastalığın klinik seyri tarafınca belirlenir, ancak bütün hastalarda en az 6 ay ve diğerlerinde genellikle bir yıl veya daha uzun olmalıdır. Tedavi; semptomların giderilmesi, radyografik anormalliklerin gerilemesi ve serum fiksasyon IgG'si titrelerindeki değişikliklerin bir kombinasyonuna göre uyarlanmıştır. İmmün sistemi baskılanmış hastalar ve meningeal tutulum öyküsü olan hastalar için yaşam boyu tedavi gerekmektedir.
Antifungal tedavinin maliyeti yıllık 5.000 $ ila 20.000 $ arasında olup yüksektir. Yoğun bakım gereksinimi olan ciddi hastalar için bu maliyetler artar. Arizona'da, 1998-2001 yılları arasında koksidioidomikozlu hasta başına ortalama 33.762 dolar harcanmıştır.
Kaynakça
[değiştir | kaynağı değiştir]- ^ "GSD Species Synonymy: Coccidioides immitis G.W. Stiles". Species Fungorum. CAB International. 7 Şubat 2016 tarihinde kaynağından arşivlendi. Erişim tarihi: 6 Şubat 2016.
- ^ a b c "Infectious Disease Index: Coccidioides immitis". MDSC Online. Public Health Agency of Canada (PHAC). 13 Mayıs 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 16 Temmuz 2013.
- ^ "Coccidioides group database". Broad Institute. 14 Temmuz 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2013.
- ^ "Operational Guidelines (version 1.0) for Geological Fieldwork in Areas Endemic for Coccidioidomycosis (Valley Fever)" (PDF). U.S. Geological Survey Open-File Report 00-348 Version 1.0. U.S. Department of the Interior. 4 Mart 2013 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 12 Temmuz 2013.
- ^ Hospenthal, Duane R., and Michael G. Rinaldi. Diagnosis and Treatment of Human Mycoses. Totowa, N.J.: Humana Press, 2007, p. 296-297.
- ^ "Arşivlenmiş kopya". 6 Eylül 2017 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Mayıs 2020.
- ^ Garcia Garcia SC, Salas Alanis JC, Flores MG, Gonzalez Gonzalez SE, Vera Cabrera L, Ocampo Candiani J (2015). "Coccidioidomycosis and the skin: a comprehensive review". An Bras Dermatol. Cilt 90. ss. 610-9. doi:10.1590/abd1806-4841.20153805. PMC 4631225 $2. PMID 26560205.
- ^ "Arşivlenmiş kopya". 6 Haziran 2020 tarihinde kaynağından arşivlendi. Erişim tarihi: 14 Mayıs 2020.
- ^ "Coccidioidomycosis (Valley Fever)". Centers for Disease Control and Prevention (CDC). 9 Temmuz 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2013.
- ^ "Fungal pneumonia: a silent epidemic - Coccidioidomycosis (valley fever)" (PDF). Centers for Disease Control and Prevention (CDC). 19 Şubat 2014 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 11 Temmuz 2013.
- ^ "Infectious Diseases Related To Travel". Centers for Disease Control and Prevention (CDC). 13 Haziran 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 12 Temmuz 2013.
- ^ "Coccidioides immitis". Tom Volk's Fungus of the Month. Tom Volk's Fungi. 17 Ocak 2013 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2013.
- ^ "Symptoms of Coccidioidomycosis (Valley Fever)". Centers for Disease Control and Prevention (CDC). 29 Mayıs 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2013.
- ^ "Treatment and Outcomes for Coccidioidomycosis (Valley Fever)". Centers for Disease Control and Prevention (CDC). 29 Mayıs 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 11 Temmuz 2013.
Dış bağlantılar
[değiştir | kaynağı değiştir]- Coccidioides immitis ve Coccidioides posadasii'nin22 Ekim 2013 tarihinde Wayback Machine sitesinde arşivlendi. sunumu, Mikoloji ve Mikobakteriyoloji Laboratuvarları Direktörü ve Laboratuvar Kliniği ve Patoloji Bölümü Profesörü Mayo Clinic Klinik Mikrobiyoloji Anabilim Dalı Profesörü Nancy L Wengenack