Sodyum bikarbonat: Revizyonlar arasındaki fark
| [kontrol edilmiş revizyon] | [kontrol edilmiş revizyon] |
Inertia6084 (mesaj | katkılar) k (GR) File renamed: File:Sodium bicarbonate3D.png → File:Sodium-bicarbonate-3D-balls-ionic.png Criterion 3 (obvious error) · Thêm phần phụ |
Değişiklik özeti yok |
||
| 1. satır: | 1. satır: | ||
{{Kimya bilgi kutusu |
|||
[[Dosya:Sodium bicarbonate.png|thumb|250px|Sodyum bikarbonat Formülü]] |
|||
| ResimDosyası = Sodium bicarbonate.jpg |
|||
[[Dosya:Sodium-bicarbonate-3D-balls-ionic.png|thumb|250x250px|Sodyum bikarbonat 3D]] |
|||
| ResimAdı = Sodyum bikarbonat örneği |
|||
| ResimDosyası1 = SodiumBicarbonate.svg |
|||
| ResimBoyutu1 = 121 |
|||
| ResimDosyasıL1 = Sodium-3D.png |
|||
| ResimAdıL1 = Sodyum katyonunun top ve çubuk modeli |
|||
| ResimDosyasıR1 = Bicarbonate-ion-3D-balls-B.png |
|||
| ResimAdıR1 = Bikarbonat anyonunun top ve çubuk modeli |
|||
| IUPACAdı = Sodyum hidrojen karbonat |
|||
| DiğerAdlar = Yemek sodası, Cep sodası, Karbonat |
|||
|Kısım1={{Kimyakutu Tanımlayıcılar |
|||
| IUPHAR_ligand = 4507 |
|||
| CASNo = 144-55-8 |
|||
| CASNo_Ref = {{cascite|correct|CAS}} |
|||
| PubChem = 516892 |
|||
| ChemSpiderID = 8609 |
|||
| ChemSpiderID_Ref = {{chemspidercite|correct|chemspider}} |
|||
| UNII = 8MDF5V39QO |
|||
| UNII_Ref = {{fdacite|correct|FDA}} |
|||
| EINECS = 205-633-8 |
|||
| DrugBank_Ref = {{drugbankcite|correct|drugbank}} |
|||
| DrugBank = DB01390 |
|||
| KEGG_Ref = {{keggcite|correct|kegg}} |
|||
| KEGG = C12603 |
|||
| MeSHName = Sodium+bicarbonate |
|||
| ChEBI_Ref = {{ebicite|correct|EBI}} |
|||
| ChEBI = 32139 |
|||
| ChEMBL = 1353 |
|||
| ChEMBL_Ref = {{ebicite|correct|EBI}} |
|||
| RTECS = VZ0950000 |
|||
| Beilstein = 4153970 |
|||
| SMILES = [Na+].OC([O-])=O |
|||
| StdInChI = 1S/CH2O3.Na/c2-1(3)4;/h(H2,2,3,4);/q;+1/p-1 |
|||
| StdInChI_Ref = {{stdinchicite|correct|chemspider}} |
|||
| InChI = 1/CH2O3.Na/c2-1(3)4;/h(H2,2,3,4);/q;+1/p-1 |
|||
| StdInChIKey = UIIMBOGNXHQVGW-UHFFFAOYSA-M |
|||
| StdInChIKey_Ref = {{stdinchicite|correct|chemspider}} |
|||
| InChIKey = UIIMBOGNXHQVGW-REWHXWOFAQ |
|||
}} |
|||
|Kısım2={{Kimyakutu Özellikler |
|||
| Formül = NaHCO<sub>3</sub> |
|||
| MolarKütle = 84.0066 g mol<sup>−1</sup> |
|||
| Görünüm = Beyaz kristaller |
|||
| Koku = Kokusuz |
|||
| Yoğunluk = {{madde işaretsiz liste |
|||
| 2.20 g/cm<sup>3</sup><ref name=crc>Haynes, p. 4.90</ref> |
|||
}} |
|||
| ErimeNoktası = |
|||
| Erime_notları = (50 °C'den itibaren [[sodyum karbonat]]a bozunur;°C<ref name="crc"/><ref>{{cite journal |doi=10.1007/s10973-006-8182-1 |title=Thermal behaviour of diclofenac, diclofenac sodium and sodium bicarbonate compositions |journal=Journal of Thermal Analysis and Calorimetry |volume=90 |issue=3 |pages=903–907 |year=2007| vauthors = Pasquali I, Bettini R, Giordano F }}</ref>) |
|||
| Çözünürlük = {{madde işaretsiz liste |
|||
| 69 g/L (0 °C)<ref name=crc3>Haynes, p. 5.194</ref><ref name=UNEP>{{cite web|publisher=[[United Nations Environment Programme]]|url=http://www.chem.unep.ch/irptc/sids/oecdsids/Sodium%20bicarbonate.pdf|title=Sodium Bicarbonate|url-status=dead|archive-url=https://web.archive.org/web/20110516015331/http://www.chem.unep.ch/irptc/sids/oecdsids/Sodium%20bicarbonate.pdf|archive-date=2011-05-16}}</ref> |
|||
| 96 g/L (20 °C)<ref name=crc3/><ref name=UNEP/> |
|||
| 165 g/L (60 °C)<ref name=crc3/><ref name=UNEP/> |
|||
}} |
|||
| ÇözünürDiğer = %0.02 aseton, %2.13 metanol @22 °C.<ref>{{cite journal | title = Solubilities of Sodium Carbonate and Sodium Bicarbonate in Acetone-Water and Methanol-Water Mixtures | journal = J. Chem. Eng. Data | year = 1966 | volume = 11 | issue = 3 | pages = 323–324 | doi = 10.1021/je60030a009| vauthors = Ellingboe JL, Runnels JH }}</ref> [[etanol]]de çözünmez |
|||
| LogP = −0.82 |
|||
| pKa = {{madde işaretsiz liste |
|||
| 10.329<ref name=crc4>Haynes, p. 7.23</ref> |
|||
| 6.351 (karbonik asit)<ref name=crc4/> |
|||
}} |
|||
| RefractIndex = nα = 1.377 nβ = 1.501 nγ = 1.583 |
|||
}} |
|||
|Kısım3={{Kimyakutu Yapı |
|||
| KristalYapısı = Monoklinik |
|||
}} |
|||
|Kısım6={{Kimyakutu Farmakoloji |
|||
| ATCCode_prefix = B05 |
|||
| ATCCode_suffix = CB04 |
|||
| ATC_Supplemental = {{ATC|B05|XA02}}, {{ATCvet|G04|BQ01}} |
|||
| AdminRoutes = Damar içi, oral |
|||
}} |
|||
|Kısım5={{Kimyakutu Termokimya |
|||
| DeltaHf = −950.8 kJ/mol<ref name=crc2>Haynes, p. 5.19</ref> |
|||
| DeltaGf = −851.0 kJ/mol<ref name=crc2/> |
|||
| Entropi = 101.7 J/mol K<ref name=crc2/> |
|||
| IsıKapasitesi = 87.6 J/mol K<ref name=crc2/> |
|||
}} |
|||
|Kısım7={{Kimyakutu Tehlikeler |
|||
| DışSDS = [http://siri.org/msds/f2/bdm/bdmjw.html External MSDS]{{dead link|date=March 2020}} |
|||
| AnaTehlikeler = Ciddi göz tahrişine neden olur |
|||
| NFPA-H = 0 |
|||
| NFPA-F = 0 |
|||
| NFPA-R = 1 |
|||
| LD50 = 4220 mg/kg (sıçan, oral)<ref>{{cite web |url= https://chem.nlm.nih.gov/chemidplus/rn/144-55-8 | work = ChemIDplus | publisher = U.S. National Library of Medicine | title = Sodium bicarbonate [USP:JAN] | last = Chambers | first = Michael | name-list-format = vanc }}</ref> |
|||
| ParlamaNoktası = Yanmaz |
|||
}} |
|||
|Kısım8={{Kimyakutu Benzeyen |
|||
| DiğerAnyonlar = [[Sodyum karbonat]] |
|||
| DiğerKatyonlar = {{madde işaretsiz liste |
|||
| [[Amonyum bikarbonat]] |
|||
| [[Potasyum bikarbonat]] |
|||
}} |
|||
| DiğerBileşikler = {{madde işaretsiz liste |
|||
| [[Sodyum bisülfat]] |
|||
| [[Sodyum hidrojen fosfat]] |
|||
}} |
|||
}} |
|||
}} |
|||
[[File:Cupcake2020.jpg|thumb|Kabartma tozu olarak karbonat kullanılmış pişmiş kekler]] |
|||
'''Sodyum bikarbonat''' ya da '''soda''' kimyasal formulü NaHCO<sub>3</sub> olan bir kimyasal bileşiktir. [[Sodyum tuzları]]ndan birisidir. [[Antiasit]] özelliği vardır. Kabartma tozu olarak da kullanılır. Suda çözünür. Beyaz katı kristal tozdur. Sodyum karbonat'ı andıran hafif alkali tadı vardır. [[Salin]] solüsyonu bileşiminde de kullanılır.<ref>http://www.ichastaliklaridergisi.org/managete/fu_folder/2012-01/html/2012-19-1-023-027.htm</ref> |
'''Sodyum bikarbonat''' ya da '''soda''' kimyasal formulü NaHCO<sub>3</sub> olan bir kimyasal bileşiktir. [[Sodyum tuzları]]ndan birisidir. [[Antiasit]] özelliği vardır. Kabartma tozu olarak da kullanılır. Suda çözünür. Beyaz katı kristal tozdur. Sodyum karbonat'ı andıran hafif alkali tadı vardır. [[Salin]] solüsyonu bileşiminde de kullanılır.<ref>http://www.ichastaliklaridergisi.org/managete/fu_folder/2012-01/html/2012-19-1-023-027.htm</ref> |
||
| 44. satır: | 141. satır: | ||
[[Kategori:Ev kimyasalları]] |
[[Kategori:Ev kimyasalları]] |
||
[[Kategori:İlaçlara kıvam veren maddeler]] |
[[Kategori:İlaçlara kıvam veren maddeler]] |
||
[[Kategori:Bilgi kutusu bulunmayan kimyasal maddeler]] |
|||
Sayfanın 23.22, 13 Haziran 2020 tarihindeki hâli

| |||
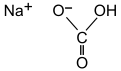
| |||
| |||
| Adlandırmalar | |||
|---|---|---|---|
Sodyum hidrojen karbonat | |||
Diğer adlar Yemek sodası, Cep sodası, Karbonat | |||
| Tanımlayıcılar | |||
3D model (JSmol)
|
|||
| 4153970 | |||
| ChEBI | |||
| ChEMBL | |||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.005.122 | ||
| EC Numarası |
| ||
| E numaraları | E500(ii) (asitliği düzenleyiciler, ...) | ||
| KEGG | |||
| MeSH | Sodium+bicarbonate | ||
PubChem CID
|
|||
| RTECS numarası |
| ||
| UNII | |||
CompTox Bilgi Panosu (EPA)
|
|||
| |||
| |||
| Özellikler | |||
| Molekül formülü | NaHCO3 | ||
| Molekül kütlesi | 84.0066 g mol−1 | ||
| Görünüm | Beyaz kristaller | ||
| Koku | Kokusuz | ||
| Yoğunluk |
| ||
| Erime noktası | (50 °C'den itibaren sodyum karbonata bozunur;°C[1][6]) | ||
| Çözünürlük (su içinde) | |||
| Çözünürlük | %0.02 aseton, %2.13 metanol @22 °C.[4] etanolde çözünmez | ||
| log P | −0.82 | ||
| Asitlik (pKa) | |||
| Kırınım dizimi (nD) | nα = 1.377 nβ = 1.501 nγ = 1.583 | ||
| Yapı | |||
| Monoklinik | |||
| Termokimya | |||
Isı sığası (C)
|
87.6 J/mol K[7] | ||
Standart molar entropi (S⦵298)
|
101.7 J/mol K[7] | ||
Standart formasyon entalpisi (ΔfH⦵298)
|
−950.8 kJ/mol[7] | ||
Gibbs serbest enerjisi (ΔfG⦵)
|
−851.0 kJ/mol[7] | ||
| Farmakoloji | |||
| B05CB04 (WHO) B05XA02 (DSÖ), QG04BQ01 | |||
| Damar içi, oral | |||
| Tehlikeler | |||
| İş sağlığı ve güvenliği (OHS/OSH): | |||
| Ana tehlikeler | Ciddi göz tahrişine neden olur | ||
| NFPA 704 (yangın karosu) |
|||
| Parlama noktası | Yanmaz | ||
| Öldürücü doz veya konsantrasyon (LD, LC): | |||
LD50 (medyan doz)
|
4220 mg/kg (sıçan, oral)[8] | ||
| Güvenlik bilgi formu (SDS) | External MSDS[ölü/kırık bağlantı] | ||
| Benzeyen bileşikler | |||
Diğer anyonlar
|
Sodyum karbonat | ||
Diğer katyonlar
|
|||
Benzeyen bileşikler
|
|||
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |||
| Bilgi kutusu kaynakları | |||

Sodyum bikarbonat ya da soda kimyasal formulü NaHCO3 olan bir kimyasal bileşiktir. Sodyum tuzlarından birisidir. Antiasit özelliği vardır. Kabartma tozu olarak da kullanılır. Suda çözünür. Beyaz katı kristal tozdur. Sodyum karbonat'ı andıran hafif alkali tadı vardır. Salin solüsyonu bileşiminde de kullanılır.[9]
Tarih
Eski Mısır’da doğal Natron çökeltileri,en çok sodyum karbonat dekahidrat ve sodyum bikarbonat içeren bir karışımdan oluşurdu.Natron hiyeroglif yazılar için boya olarak kullanılırdı.
1791 yılında fransız kimyager, Nicolas Leblanc soda olarak bilinen sodyum karbonatı üretti.1846 yılında New York’lu iki fırıncı,John Dwink ve Austin Church sodyum karbonat ve karbondioksit den kabartma tozu üreten ilk fabrikayı kurdu.
Bu bileşik 1800 lü yıllarda Roman kaptan, Rudyard Kipling tarafından balıkları taze tutmak amacıyla kullanılmış ve o günden sonra ‘saleratus’ olarak anılmıştır.
Üretim
Sodyum karbonat, sodyum hidroksitin sulu çözeltisi ile karbon dioksitin reaksiyonu ile elde edilebilir.
CO2 + 2 NaOH --> Na2CO3 + H2O
Sodyum bikarbonat ise yeterince yüksek yoğunlukta karbondioksit ve su tepkimesi ile elde edilebilir.Sodyum bikarbonat bu yöntemde katı olarak çökelir.Kabartma tozu ticari miktarda benzer bir yöntem ile üretilmektedir.
Na2CO3 + CO2 + H2O --> 2 NaHCO3
Fizyolojik ve farmakolojik özellikleri
Yüzde 1,3'lük çözeltisi izotonik özelliktedir.
Veteriner hekimlikte asidozis'in sağaltımında önem taşır.
Hiponatremi'nin sağaltımında kullanılır.
Kaynakça
- ^ a b Haynes, p. 4.90
- ^ a b c Haynes, p. 5.194
- ^ a b c "Sodium Bicarbonate" (PDF). United Nations Environment Programme. 2011-05-16 tarihinde kaynağından (PDF) arşivlendi.
- ^ Ellingboe JL, Runnels JH (1966). "Solubilities of Sodium Carbonate and Sodium Bicarbonate in Acetone-Water and Methanol-Water Mixtures". J. Chem. Eng. Data. 11 (3): 323–324. doi:10.1021/je60030a009.
- ^ a b Haynes, p. 7.23
- ^ Pasquali I, Bettini R, Giordano F (2007). "Thermal behaviour of diclofenac, diclofenac sodium and sodium bicarbonate compositions". Journal of Thermal Analysis and Calorimetry. 90 (3): 903–907. doi:10.1007/s10973-006-8182-1.
- ^ a b c d Haynes, p. 5.19
- ^ Chambers M. "Sodium bicarbonate [USP:JAN]". ChemIDplus. U.S. National Library of Medicine.
- ^ http://www.ichastaliklaridergisi.org/managete/fu_folder/2012-01/html/2012-19-1-023-027.htm
Dış bağlantılar
 Wikimedia Commons'ta Sodyum bikarbonat ile ilgili çoklu ortam belgeleri bulunur.
Wikimedia Commons'ta Sodyum bikarbonat ile ilgili çoklu ortam belgeleri bulunur.
| İnorganik kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |



