Homolog rekombinasyon

Homolog rekombinasyon (genel rekombinasyon olarak da bilinir), benzer veya aynı dizilere sahip DNA iplikleri arasında nükleotit dizilerinin birbiriyle yer değiştirdiği bir genetik rekombinasyon tipidir. Bu süreç sırasında DNA birkaç kere kesilir, sonra da birleştirilir. Homolog rekombinasyon, DNA'daki çift iplikli kırıkların hatasız tamirinde kullanılmanın yanı sıra, mayoz sırasında krosover yoluyla yeni DNA dizi bileşimlerinin (kombinezonlarının) oluşumunu da sağlar. DNA'daki yeni bileşimler genetik varyasyonlar oluşturur. Genetik varyasyonlar yeni, bir olasılıkla yararlı olabilecek alel kombinasyonlarıdır, bunların üreyen canlı topluluklarda oluşmaları, bu değişiklikleri taşıyan bireylerin değişen çevresel şartlara evrimsel adaptasyon göstermelerini sağlar.[1]
İki tip homolog rekombinasyon vardır, biri mitoz sırasında DNA tamirinde görülür, öbürü mayoz sırasında. Bunların aynı ilk adımları aynıdır: çift iplikli bir kırık meydana geldikten sonra, kırığın etrafındaki DNA'nın 5' ucundan bir kısım kesilp atılır (buna rezeksiyon denir). Bunu izleyen İşgal adımında, hasar görmüş kromozomun çıkıntı yapan 3' ucu, hasarsız homolog kromozomu "işgal" eder. İşgalin ardından iki kromozom arasında bir Holliday bağlantısı oluşur. DNA tamir yolağında, ikinci bir Holliday bağlantısı oluşur. Bu iki bağlantının nasıl ayrıştığına (yani kesildiğine) bağlı olarak, mayotik versiyonda kromozom krosoveri ya olur ya da olmaz.
Homolog rekombinasyonun, canlıların üç üst aleminde de korunmuş olması onun temel bir biyolojik mekanizma olduğunu düşündürür. Protistalarda homolog rekombinmasyon genlerinin keşfi, mayozun evrim tarihinde erken ökaryot kökenli olduğu şeklinde yorumlanmıştır. Bu genlerin bozulması ile birkaç tip kanser arasında ilişki bulunduğu için, homolog rekombinasyon proteinleri aktif bir araştırma konusudur. Homolog rekombinasyon, ayrıca moleküler biyolojide kullanılan bir tekniktir, hedef organizmalarda genetik değişiklikler meydana getirmek için kullanılır. Homolog rekombinasyon teknikleri kullanan gen hedefleme teknikleri 2007 Nobel Fizyoloji veya Tıp Ödülü'nün konusu olmuştur.
Bakterilerde[değiştir | kaynağı değiştir]

Homolog rekombinasyon bakterilerde önemli bir DNA tamir sürecidir. Bakteri topluluklarında genetik çeşitlilik oluşturmakta da önemlidir, ama bu süreç ökaryotik genomlarıa çeşitlilik getiren mayotik rekombinasyondan büyük farklılık gösterir. Homolog rekombinasyon Escherichia coli adlı bakteride ayrıntılı bir şekilde çalışılmıştır.[2] Bu yolağın iki versiyonu vardır, bunlar, çift iplikli kırıkların tamirini sağlayan RecBCD yolağı ve tek iplikli kırıkların tamirini sağlayan RecF yolağıdır.[3] RecBCD yolağı, bozulmuş veya duraksamış DNA ikileşme çatalını yeniden harekete geçirmeye, ayrıca transpozonlarda gen ifadesinin düzenlenmesinde kullanılır.

RecBCD yolağı[değiştir | kaynağı değiştir]
RecBCD yolağı, bakterilerde çift iplikli DNA kırıklarını onarmakta kullanılan ana rekombinasyon yolağıdır. Çift iplikli DNA'daki bir kırığın küt veya yaklaşık küt ucuna bağlanarak rekombinasyonu başlatır. RecBCD DNA'ya bağlanınca, RecB ve RecD altbirimleri, ATP hidrolizi ile yürüyen helikaz etkinliği sayesinde, birbirine sarılı DNA ikilisini çözmeye başlar. Bu iki altbirim sonra ayrılmış olan iplikleri endonükleotik olarak keser: RecB, 3' ucu, RecD'nin 5' ucu kesmesinden daha sık olarak keser. DNA'nın açılması ve kesilmesi RecBCD'nin Kay konumu (İng. Chi site) olarak adlandırılan spesifik bir nükleotit dizisine (5'-GCTGGTGG-3') varana kadar devam eder.[5]
Kay konumuna varınca RecBCD enziminin etkinliğinde dramatik bir değişiklik meydana gelir.[6] RecBCD birkaç saniye kadar duralar, sonra ilk hızının yarısı bir hızla ilerlemeye devam eder. RecD kesme hızını artırır ve 5' ipliği daha parçalanmış bir hale getirir, bu arada RecB altbirimi kesme etkinliğini durdurur. Kay konumunun tanınması RecBCD enzimini değiştirir, öyle ki 3'uzantıya birçok RecA proteinleri yüklemeye başlar. Meydana gelen, RecA kaplı nükleoprotein filaman, homolog kromozomda benzer diziler aramaya başlar. Başka bir DNA molekülünde benzer bir dizi bulunca RecA'lı iplik, iplik işgali denen bir süreç ile bu homolog DNA ikilisinin içine girer.[5]
İşgalci 3' çıkıntı içine girdiği DNA ikilisindeki iki iplikten birinin yerini alır. Sonuç, Holliday bağlantısı olarak adlandırılan, X-harfi şeklinde bir yapıdır. RuvA Holliday bağlantısına bağlanır ve RuvB'yi seferber eder. Holiday birleşiminin DNA üzerinde yürümesi dal ilerlemesi olarak adlandırılır ve heksamerik bir ATPaz olan RuvB tarafından katalizlenir. RuvC zayıf spesifiteli bir endonükleazdır, junction ayrışmadan önce onun bir miktar ilerlemesine izin verir.[7]
Rekombinasyon iki tip ürün verir, bunlar Holliday birleşiminin nasıl ayrıştığına bağlıdır bunlara uç birleştirme (İng. splice) veya yama (İng. patch) denir. Uç birleştirme ürünleri yarım krosover ürünleridir, bunun sonucu genler karılır. Buna karşın yama ayrışması krosover olmayan ürünler meydana getirir.[8]
RecF yolağı[değiştir | kaynağı değiştir]
Bakteriler DNA'daki tek iplikli kırıkları onarmak için homolog rekombinasyonun RecF yolağını (RecFOR yolağı olarak da adlandırılır) kullanırlar. RecBCD yolağı mutasyonlar sonucu çalışmaz hale gelince RecF yolağı çift iplikli kırıkların tamirinde onun yerini de alabilir. RecF yolağı hâlen RecBCD yolağından çok daha az anlaşılmış durumdadır. İki yolak da iplik işgali için RecA'ya gerek duyar, ayrıca dal ilerlerlesi (İng. branch migration) ve ayrışma evrelerinde benzeşirler.[9][10]
RecF yolağının başlangıcında, RecJ (tek iplikli DNA'yı 5' → 3i yönünde kesen bir eksonükleaz) DNA'daki tek iplikli bir kırıktaki 5' uca bağlanır, bu uçtan kırparak 3' doğrultuda ilerlemeye başlar. RecJ tek başına da çalışabilse de, tek iplik bağlayıcı protein (İngilizce single-strand binding protein veya SSBP) ve RecQ helikaz etkinliğinin mevcudiyeti 5' ucun ne kadar kırpıldığını (rezeksiyon miktarını) belirler. RecJ'nin 5' ucu kırpmasının ardından meydana gelen 3' çıkıntıya SSBP bağlanır.[10] Bu sayede tek iplikli 3' çıkıntının, komplementer diziler yüzünden kendi üzerine katlanmasının önüne geçilmiş olur.[11]
RecA'nın SSBP-kaplı 3' çıkıntıya yüklenmesi iki farklı yoldan olabilir, bunlardan biri RecFOR enzimini gerektirir, öbürü ise RecOR enzimini.[12] RecFOR yolağında, 3' uca sahip tek iplikli DNA'nın çift ipliklikçikli DNA ile birleştiği konumda RecFR kompleksi bağlanır. RecO sonra tek iplikli DNA üzerinden SSBP'nin yerini alır ama SSBP RecO'ya bağlı kalır. RecFOR sonra bu tek iplikli DNA/çift iplikli DNA birleşmesindeki (junction) içeri girinti 5' uca RecA'yı yükler. RecFR'de bulunan RecR altbirimi RecO ile etkileşerek RecFOR kompleksini oluşturur. Bunun sonucu RecR hem RecO'dan SSBP'yi ayrıştırır hem de 3' çıkıntıya RecA proteinleri yükler.[13]
RecOR tarafından RecA yüklemesi RecFOR yüklemesinden birkaç yönden farklıdır, özellikle moleküler etkileşim gereksinimleri ve ideal DNA substratı için.[12] RecFOR yolağında farklı olarak, RecOR yolağında RecO ile SSBP'nin C-ucu arasında etkileşim vardır. Ayrıca, RecOR yolağında 3' çıkıntıya RecA'yı bağlamak için tek iplikli DNA/çift iplikli DNA birleşmesine gerek yoktur, buna karşın verimli olması için RecFOR yolağında böyle bir gereksinim vardır. Bu yüzden recA yüklemesinde RecOR yolağı çoğu durumda RecFOR yolağından daha verimli çalışır.[12]
Dal ilerlemesi[değiştir | kaynağı değiştir]
İplik işgalinin hemen ardından, dal ilerlemesi olarak adlandırılan bir süreç ile, Holliday bağlantısı bağlanmış DNA üzerinde hareket eder. Holliday bağlantısının bu hareketi sırasında iki homolog DNA ikilileri arasında baz çiftleri birbiriyle yer değiştirir. Dal ilerlemesini katalizlemek için RuvA proteini Holliday bağlantısını önce tanır, sonra da ona bağlanır, ardından RuvB'yi de seferber ederek RuvAB kompleksini oluşturur. RuvB molekülü halkasal, altıgen şekillidir; iki RuvB molekülü Holliday bağlantısının iki tarafında yüklenirler ve dal ilerlemesine güç verecek birer pompa gibi çalışırlar. İki RuvA tetrameri Holliday bağlantısının kare-şekilli merkezinde yer alır ve DNA'yı sandviç gibi aralarına alırlar. Her bir DNA ikilisinin iplikleri RuvA'nın yüzeyinde çözülürler, protein onları bir ikiliden öbürüne yönlendirir.[14][15]
Ayrışma[değiştir | kaynağı değiştir]
Rekombinasyonun ayrışma (rezolüsyon) aşamasında, iplik işgal sürecinde oluşan Holliday bağlantıları kesilir, böylece tekrar iki ayrı DNA molekülü meydana gelir. Bu kesme işlemi, RuvC ile etkileşen RuvAB kompleksi beraberce oluşturduğu RuvABC kompleksi tarafından yapılır. RuvC bir endonükleazdır, 5'-(A/T)TT(G/C)-3' dizisini keser; bu dejenere kod, DNA'da sıkça bulunur (yaklaşık her 64 nükleotitte bir).[15] Kesmeden önce, RuvC Holliday bağlantısındaki iki RuvA tetramerinden birini yerinden çıkarıp oradaki DNA'ya temas eder.[14] RuvC'nin DNA'yı nasıl kestiğine bağlı olarak rekombinasyon ya "uç birleştirme" (İng. splice) ya da "yama" (İng. patch) ürünleriyle sonuçlanır.[15] Uçbirleştirme ürünleri krosover ürünleridir, rekombinasyon noktasının iki yanındaki genetik malzeme farklı şekilde bir araya gelir (asortisman olur). Yama ürünleri, buna karşın, krosover olmayan ürünlerdir, genetik malzemenin yeni bir bileşimi olmaz, rekombinasyon ürününde sadece hibrit DNA'dan oluşan bir "yama" vardır.[16]
Genetik transferin kolaylaştırılması[değiştir | kaynağı değiştir]
Yatay gen transferi, bir organizmanın, yavrusu olmadığı başka bir organizmaya ait yabancı DNA'yı edinme sürecidir. Yatay gen transferinde verici organizmanın DNA'sının alıcı organizmanın genomuna entegre olmasında homolog rekombinasyon önemli bir yoludur. Homolog rekombinasyon alınan DNA'nın konak genoma yüksek derecede benzer olmasını gerektirir ve bu yüzden yatay gen transferi genelde benzer bakterilerle sınırlıdır.[17] pek çok bakteri üzerinde yapılan çalışmalar göstermiştir ki, verici ve alıcı organizmaların DNA'ların dizi benzerliği arttıkça rekombinasyon sıklığı log-lineer bir azalma gösterir.[18][19][20]
Ökaryotlarda[değiştir | kaynağı değiştir]
Homolog rekombinasyonun olması çoğu ökaryotik hücrede mitoz ve mayoz için esastır. Mitoz sırasında homolog rekombinasyon, iyonlaştırıcı radyasyon veya DNA'ya hasar verici kimyasalların neden olduğu çift iplikli kırıkları tamir etmeye yarar.[21] Bunların tamir edilmemesi durumda somatik hücrelerde kromozom parçaları arasında büyük ölçekli yer değişimlerine (rearrangement) yol açar,[22] bu da kansere neden olabilir.
Mayozda homolog rekombinasyon, profaz I evresindeki kromozom krosoverini kolaylaştırır.[23] Mayotik homolog rekombinasyon Spo11 proteininin programlanmış olarak DNA'da çift iplikli bir kırık yapması ile başlar.[24] Bu kesilme yerleri öoğunlukla rekombinasyon "hotspotlarında" meydana gelir, bunlar kromozom üzerinde rekombinasyon sıklığını yüksek olduğu 1000-2000 baz çiftlik bölgelerdir. Aynı kromozomdaki iki gen arasında rekombinasyon hotspotunun olmazsa bu demektir ki bu iki gen gelecek kuşaklarda eşit oranda kalıtılacaktır, yani bu iki gen, bağımsız assorti olan genlerden beklenecek bağlantıdan daha yüksek bir bağlantıya sahip olacaktır.[25] Ebeveyn kromozomlarındaki genetik malzemenin karışması (karılması?) sonraki kuşaklardaki genetik çeşitliliğin önemli bir kaynağıdır.
Çift iplikli kırık tamiri[değiştir | kaynağı değiştir]
HR ve NHEJ arasında seçim[değiştir | kaynağı değiştir]
Çift iplikli kırıklar homolog rekombinasyon veya homolog olmayan (non-homolog) uç birleştirme (NHUB) ile tamir edilebilir. NHUB, homolog rekombinasyondan farklı olarak, onarıma kılavuzluk yapmak için uzun homolog bir diziye gerek göstermez. çift iplik kırıklarının tamiri için homolog rekombinasyon mu, NHUB mu kullanılacağı hücre döngüsünün evresine bağlıdır. Kardeş kromatitlere kolayca erişilebildiği hücre döngüsünün S ve G2 evrelerinde ve homolog rekombinasyon yukarı ayarlanır. Kardeş kromatitler birbirlerinin tam bir kopyası olduklarından homolog rekombinasyon için ideal birer substrattır, buna karşın homolog kromozomlar birbirlerine benzer olmakla beraber tıpatıp aynı değildirler. NHUB G1 evresinde hakimdir, ondan sonra aşağıa ayarlanır ama tüm hücre döngüsü boyunca bir miktar etkinliğini sürdürür. Homolog rekombinasyon ve NHUB'nin hücre döngüsüne dayalı düzenlenmeleri türlere göre çarklılık gösterir. Siklin-bağımlı kinazlar (CDK) tomurcuklanan mayalarda ve memelilerde homolog rekombinasyonun özellikle önemli düzenlenyicileridir, ama çalışma mekanizmaları bu iki taksada farklıdır.[26] Tomurcuklanan mayalarda, S evresine girince, Cdc28 adlı CDK, Sae2 proteinini fosforile ederek homolog rekombinasyonu başlatır.[27]
Modeller[değiştir | kaynağı değiştir]
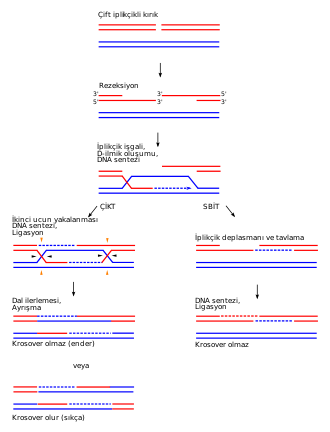
Homolog rekombinasyonun çift iplikli kırık tamirine nasıl yardım ettiği hakkında iki ana model, çift iplikli kırık tamir yolağı (çifte Holliday bağlantı modeli olarak da değinilir) ve sentez-bağımlı iplik tavlama (SBİT) yolağıdır.[28] Bu iki yolak ilk birkaç adımlarında benzerdirler. Çift iplikli bir kırık meydana geldikten sonra, MRX kompleks (insanlarda MRN kompleksi) olarak adlandırılan bir heterotrimerik potein, kırığın iki tarafındaki DNA'lara bağlanır. Sonra bir çift iplikli kırığın bir "rezeksiyon"u olur, yani her iki zincirde de kırığın hemen akış yukarısındaki (yani 5' ucu tarafındaki) DNA çıkartılır. Resekziyonun ilk adımında MRX kompleksi Sae2'yi seferber eder, bunlar beraberce kırığın iki tarafındaki 5' uçları kırparak tek iplikli kısa 3' çıkıntılar yaratırlar. İkinci adımda, üç diğer enzim ile 5'→3' rezeksiyon devam eder: Sgs1 helikaz (bakteriyel RecQ helikazın bir homoloğu, bkz. yukarıdaki bölüm), Exo1 ve Dna2 nükleazları.[27].
İkileşme proteini A (İng. Replication protein A veya RPA), tek iplikli DNA'ya yüksek afiniteli bir proteindir, ilk aşamada 3' çıkıntılara bağlanır.[29] Sonra, birkaç aracı proteinin de yardımıyla, Rad51 (ve mayoz sirasinda Dmc1) RPA ile kaplanmış tek iplikli DNA üzerinde bir nükleoprotein filaman oluşturur ve 3' çıkıntıya benzer diziye sahip DNA dizileri aramaya başlarlar. Böyle bir dizi bulunca, iplik işgali denen bir süreç başlar, tek iplikli nükleoprotein filaman, homolog kromozomun içine girer, onu "işgal" eder. İplik işgali sırasında, işgalci 3' çıkıntı ipliği ile homolog kromozom arasında bir deplasman (yerinden çıkma) ilmiği (İng. displacement loop veya D-ilmiği) oluşur. İplik işgalininin ardından, bir DNA polimeraz işgalci 3' ipliği uzatır ve D-ilmiğini, Holliday bağlantısı olarak adlandırılan, haç şekilli bir yapıya dönüştürür. Bunun ardından, işgalci iplik (yani orijinal 3' çıkıntılardan biri) üzerinde DNA sentezi olur, böylece iplik işgali sırasında yerinden çıkarılan iplik yerine yenisi getirilmiş olur.[28]
Çift ipliklikçikli kırık tamir yolağı[değiştir | kaynağı değiştir]
Rezeksiyon, iplik işgali ve DNA sentez aşamalarının ardından, ÇİKT ve SBİT yolakları ayrışırlar.[28] ÇİKT yolağının farklı olan yönü, ikinci 3' çıkıntının (iplik işgaline rol oynamayan çıkıntının) da homolog kromozom ile bir Holliday bağlantısı oluşturmasıdır. Çifte Holliday bağlantıları sonra kertici endonükleazlar (İng. nicking endonükleaz; DNA'nın tek ipliğini kesen (kerten) bir restriksiyon endonükleaz tipi) tarafından rekombinasyon ürünlerine dönüştürülür. ÇİKT yolağında rekombinasyon ürünü kromozomda krosover olma olasılığı olmama olasılığından çok daha yüksek olduğu bulunmuştur.[30] ÇİKT yolağı çoğu zaman kromozom krosoveri ile sonuçlandığı için, mayozda homolog rekombinasyonun nasıl olduğunun esas modelidir.
ÇİKT yolağında rekombinasyonun kromozomal krosoverine yol açması çifte Holliday bağlantısının nasıl çözüldüğüne bağlıdır. Eğer iki Holliday bağlantısı kesişen ipliklerde kesilirse (yandaki şekildeki siyah ok uçlarında), krosoversiz kromozomlar meydana gelir. Alternatif olarak, eğer bir Holliday bağlantısı kesişen iplikte kesilir, öbür bağlantı ise kesişmeyen iplikte kesilirse (yani şekilde görülen bir Holiday bağlantısındaki siyah okta ve öbüründeki turuncu okta), kromozomal krosover meydana gelir.[31]
SBİT yolağı[değiştir | kaynağı değiştir]
sentez-bağımlı iplik tavlama (SBİT) yolağı üzerinden homolog rekombinasyon mitozda olur ve krosoversiz ürünlerle ile sonuçlanır. Bu modelde, Holliday bağlantısının DNA ipliği üzerindeki hareketi (dal ilerlemesi, branch migration olarak adlandırılan bir süreç ile), uzatılmış işgalci ipliğin serbest bırakılması ile son bulur. İşgalci ipliğin yeni sentezlenmiş 3' ucu, zarar görmüş kromozomdaki öbür orijinal 3' ile komplementer baz eşleşmesi ile tavlanır. Tavlanmadan sonra 3' uçta kalan fazlalıklar çıkarılır, tek iplikli bölgeler tamir edilir ve SBİT tamamlanır.[32]
Tek iplik tavlama yolağı[değiştir | kaynağı değiştir]

Homolog rekombinasyonun tek iplik tavlama (TİT) yolağı, iki tekrar dizisi arasındaki çift iplikli kırıklar tamir edilir.[32][33] Kavram olarak bu yolak görece basittir: DNA ikilisinin iki ipliğinin 5'→3' rezeksiyonunun ardından, meydana gelen iki 3' çıkıntı hizalanır ve Rad50'nin yardımıyla birbirlerine tavlanırlar. Tavlanma tamamlanınca, 3' çıkıntıların homolog olmayan, artık uçları (Slx4 ve Saw1'in eşliğindeki) Rad1/10 nükleaz tarafından sindirilip yok edilir.[34] Kalan boşluklar yeni DNA sentezi ile doldurulur, ligasyon ile DNA ikilisindeki iplikler birleşir.[35] Tekrar dizileri arasındaki DNA dizisi ve tekrar dizilerinden biri bu süreç sonunda kaybolur. Genetik mazlemede delesyonlara neden olmasından dolayı TİT yolağı mutajenik sayılır.[32]
Kİİ yolağı[değiştir | kaynağı değiştir]
DNA ikileşmesi sırasında, DNA helikaz DNA'yı açarken bazen ikileşme çatalında çift iplikli kırıklara rastlanabilir. Bu bozukluklar homolog rekombinasyonun "kırık-indüklenmiş ikileşme" (İng. break-induced replication) (Kİİ) yolağı ile tamir edilir. Bu konuda önerilmiş üç model, iplik işgali ile başlar ama D-ilmiğinin ilerlemesi ve onu takip eden, post-sinaptik (Holliday bağlantısının ayrışması sonrası) evrelerde farklılık gösterirler.[36]
Kİİ yolağı, telomerazların yokluğunda (veya onların eşliğinde) telomerlerin uzunluğunu muhafaza etmeye yarayabilir (telomerler ökaryotik kromozomların uçlarındaki DNA bölgeleridir). Telomeraz enzimleri olmayınca telomerle her mitoz bölünmesinin ardından biraz kısalırlar, bu da nihayet hücre bölünmesini engeller ve yaşlanmaya neden olur. Mutasyonlar sonucu telomerazın etkinsizleştirildiği tomurcuklanan maya hücrelerinde, Kİİ yolağını kullanarak telomerlerini uzatan ve beklenenden daha geç yaşlanan iki tip hücre tipi bulunmuştur. Her iki tip hücre Rad52 proteinine gerek duyar, Tip I hücreler ayrıca Rad51'e gerek duyar, Tip II hücreler ise duymaz. Bu iki tip hücrenin spontan mutasyonlar ile ortaya çıkarlar, Tip I hücreler Tip II ücrelere kıyasla daha sık oluşurlar ama daha yavaş büyürler.[36]
Telomer uzunluğunun korunması, kanserin anahtar özelliklerinden biri olan hücre ölümsüzleşmesinde kritik bir öneme sahiptir. Çoğu kanser, telomerlerini korumak için telomerazları yukarı ayarlar. Ancak, bazı insan kanser tiplerinde, Kİİ-benzeri bir yolak, telomer muhafazası için alternatif bir mekanizma olarak çalışarak tümörlerin varlıklarını sürdürmelerini sağlar.[37] Rekombinasyona dayalı bir telomer muhafaza mekanizması yüzünden telomeraz inhibitörlerine dayanıklılık oluşabileceği hâlen araştırılmaktadır.[38]
İşlevsizliğin etkileri[değiştir | kaynağı değiştir]
Homolog rekombinasyonda yetersizlik insanlarda kanser oluşumu ile bağlantılı olduğu görülmüştür. Örneğin kanserle ilişikli Bloom sendromu, Werner sendromu ve Rothmund-Thomson sendromu, RecQ helikaz genlerinden birinin (sırasıyla BLM, WRN ve RECQ4) hatalı çalışmasından kaynaklanır.[39] BLM proteinin eksik olduğu Bloom sendrom hastalarında homolog rekombinasyon sıklığında bir artma vardır.[40] BLM'siz farelerde yapılan deneylerde, bu mutasyonun neden olduğu homolog rekombinasyon sonucu meydana gelen heterozigotluk kaybı kansere yol açmaktadır.[41]
Homolog rekombinasyon sıklığının azalması da kansere yol açabilir.[42] BRCA1 bunun bir örneğidir. Bir tümör baskılayıcı gen olan BRCA1'nın kötü çalışmasının göğüs ve yumurtalık kanserine yatkınlığını artırdığı gösterilmiştir. BRCA1 geni olmayan hücrelerde homolog rekombinasyon vakaları 5 kat daha azdır; iyonlaştırıcı radyasyona daha duyarlı olmaları DNA'da daha çok sayıda çift iplikli kırık hasarının meydana geldiğini gösteri.[42] BRCA1 ile yakın ilişkili bir gen olan BRCA2'nin tek bilinen işlevi homologrekombinasyonu kolaylaştırmaktır. Bu genin ürünü olan 3418 amino asit uzunluğundaki büyük protein, tek iplikli DNA'ya bağlanarak ve RAD51 uzamasi için bir platform sağlayarak homolog rekombinasyonu kolaylaştırır. Bu filaman homolog rekombinasyonun başlamasında önemli bir adımdır ve BRCA2 mutasyonları yüzünden bu süreci eksik olak hücrelerde BRCA1 mutanlarındakine benzer bir fenotip görülmüştür: azalmış homolog rekombinasyon ve radyasyona karşı artmış bir duyarlılık.[42]
Evrimsel köken[değiştir | kaynağı değiştir]
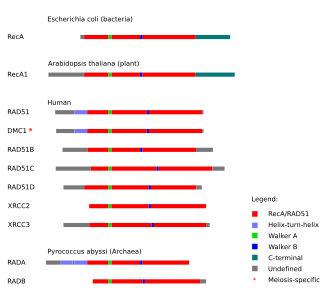
Amino asit dizilerindeki benzerliklere dayanarak homolog rekombinasyon (HR) ile ilişkili proteinlerin ortak evrimsel kökenlere sahip olduğu düşünülmektedir.[43] HR-ilişkili protein gruplarından biri RecA/Rad51 protein ailesidir, bunun içinde bakterilerdeki RecA proteini, arkelerdeki benzer proteinler (RadA ve RadB) ve ökaryotlardaki proteinler (Rad51, Rad51B, Rad51C, Rad51D, Dmc1, XRCC2 and XRCC3). Tüm bu proteinler, RecA/RAD51 olarak adlandırılan yaklaşık 230 amino asit uzunluğunda korunmuş bölgeye sahiptir. Bu protein bölgesi içinde iki dizi motifi vardır, Walker A ve Walker B, bunlar bu gen ailesinin protein ürünlerine ATP hidroliz etkinliği sağlar.[43]
Filogenetik ağaçlarda RadA, Rad51 ve Dmc1'in aynı monofiletik gruba ait olması, bu proteinlerin ortak bir ataya ait olduğunu ima eder. Bu protein ailesinde Rad51 ve Dmc1 beraberce gruplandırılır, RadA'dan ayrı bir klad olarak. Okaryotik bir RecA geninde kadim bir gen ikileşme olayının modern RAD51 ve DMC1 genlerinin kökeni olduğu öne sürülmüştür.[43] Bu üç proteinin beraberce gruplandırılma kıstaslarından biri, her birinin N-uçlarında bir sarmal-kıvrım-sarmal (helix-turn-helix) motifine sahip olmalarıdır, bu motif DNA'ya bağlanma özelliği sağlar.
Ökaryotlardan en erken ayrılan Protistalardan biri olan Giardia 'da Dmc1'in keşfedilmesi, mayotik homolog rekombinasyonun (ve mayozun kendisinin) ökaryotik evrimde erken ortaya çıkmış olabileceğini göstermektedir.[44]
Dmc1 üzerine yapılan araştırmalara ek olarak, Spo11 protein ve homologlarının moleküler ve filogenetik analizi de mayotik rekombinasyonun orijini hakkında bilgi vermektedir.[45] Spo11, mayozda homolog rekombinasyonu başlatmak için çift iplikli kırıkları katalizleyen bir tip II topoizomerazdır.[24] Hayvan, mantar, bazı bitkiler, protistalar ve arkelerde Spo11 protein dizilerine dayanarak inşa edilen filogenetik ağaçlar, ökaryotik Spo11'in ökaryot ve arkebakterilerin en osn ortak atasında ortaya çıktığını ine sürmektedir.[45]
Teknolojik uygulamalar[değiştir | kaynağı değiştir]
Gen hedeflemesi[değiştir | kaynağı değiştir]

Canlıların içine DNA dizileri sokup rekombinant DNA ve genetik değişime uğramış canlı üretmekte kullanılan pek çok yöntem homolog rekombinasyon sürecini kullanır.[46] Gen hedeflemesi olarak da adlandırılan bu yöntemler maya ve fare genetiğinde özellikle yaygın kullanılır. Nakavt farelerde kullanılan gen hedefleme tekniği, yapay genetik malzemenin aktarılması için fare embriyonik kök hücreleri kullanır. Homolog rekombinasyon yoluyla hedef genin yerine dışarıdan eklenen gen gelir. Dolayısıyla fare, belli bir memeli genin etkilerini anlamak için bir model olarak kullanılır. Homolog rekombinasyon kullanarak embriyonik kök hücreler farelerde nasıl genetik değişim yaratılabileceğini keşfettikleri için Mario Capecchi, Martin Evans ve Oliver Smithies 2007 Nobel Fizyoloji veya Tıp Ödülünü kazanmışlardır.[47]
Protein mühendisliği[değiştir | kaynağı değiştir]
Homolog rekombinasyon ile protein mühendisliğinde iki proteindeki parçalar yer değiştirerek kimera protein meydana getirir. Bu tekniklerde rekombinasyon kullanarak proteinin birincil dizisinde yüksek düzeyde çeşitlilik yaratılsa da proteinin katlanarak üçüncül yapısını oluşturma yeteneği korunur.[48] Buna karşın diğie rprotein mühendislik tekniklerinde, örneğin rassal noktasal mutagenezde, proteinin işlevinin muhafaz olasılığı, artan amino asit substitusyonlarında artmayla üssel olarak olarak azalır.[49] Rekombinasyon teknikleri ile üretilen kimeralar katlanma yeteneklerini muhafaza ederler çünkü yer değiştiren parçaları yapısal ve evrimsel olarak korunmuştur. Rekombinasyon yapabilen yapısal "bloklarda" amino asit kalıntıları arasındaki etkileşimler korunmuştur. SCHEMA gibi yöntemler ve istatistik bağlaşım analizi (statistical coupling analysis) rekombinasyona uygun yapısal birimlerin tespitini mümkün kılar.[50][51][52]
Homolog rekombinasyona dayana teknikler protein mühendisliğinde kullanılmıştır.[50] 2007'de yayımlanan bir çalışmada, isoprenoid bileşiklerin biyosenteziyle ilişkili iki enzimin kimeraları üretilmiştir. Ebeveyn proteinler isoprenoid biyosentezindeki gerekli bir adımı sentezleme yetneğine sahip değilken, kimerada bu yetenek bulunmuştur.[53] Recombinasyonlu protein mühendisliği ile üretilen sitokrom P450 proteinleri de ebeveyn proteinlerin kullanamadığı substratları kabul ettiği bulunmuş böylece tasarımlı kimeralarda önemli derecede işlevsel çeşitlilik olabildiği gösterilmiştir.[54]
Kaynakça[değiştir | kaynağı değiştir]
- ^ Alberts, B; ve diğerleri. (2002). "Chapter 5: DNA Replication, Repair, and Recombination". Molecular Biology of the Cell (4.4 yayımcı=Garland Science bas.). New York. s. 845. ISBN 0-8153-3218-1. OCLC 1132112794. 27 Şubat 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 31 Ekim 2009.
- ^ Kowalczykowski, SC; ve diğerleri. (Eylül 1994). "Biochemistry of homologous recombination in Escherichia coli". Microbiology and Molecular Biology Reviews. 58 (3). ss. 401-465. PMC 372975 $2. PMID 7968921.
- ^ Rocha, EPC; ve diğerleri. (Ağustos 2005). "Comparative and evolutionary analysis of the bacterial homologous recombination systems". PLoS Genetics. 1 (2). s. e15. doi:10.1371/journal.pgen.0010015. PMC 1193525 $2. PMID 16132081.
- ^ Singleton, MR; ve diğerleri. (Kasım 2004). "Crystal structure of RecBCD enzyme reveals a machine for processing DNA breaks" (PDF). Nature. Cilt 432. ss. 187-193. doi:10.1038/nature02988. PMID 15538360. 25 Mayıs 2004 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 31 Ekim 2009.
- ^ a b Dillingham, MS; Kowalczykowski, SC (Aralık 2008). "RecBCD enzyme and the repair of double-stranded DNA breaks". Microbiology and Molecular Biology Reviews. 72 (4). s. 642-671. doi:10.1128/MMBR.00020-08. PMC 2593567 $2. PMID 19052323.
- ^ Spies, M; ve diğerleri. (Eylül 2003). "A molecular throttle: the recombination hotspot chi controls DNA translocation by the RecBCD helicase". Cell. 114 (5). ss. 647-654. doi:10.1016/S0092-8674(03)00681-0. PMID 13678587.
- ^ Donaldson, JR; ve diğerleri. (2006). "RuvABC is required to resolve Holliday junctions that accumulate following replication on damaged templates in Escherichia coli". Journal of Biological Chemistry. 281 (39). ss. 28811-28821. doi:10.1074/jbc.M603933200. PMID 16895921. 23 Temmuz 2008 tarihinde kaynağından arşivlendi. Erişim tarihi: 31 Ekim 2009.
- ^ Gumbiner-Russo, LM; Rosenberg, SM (2007). "Physical analyses of E. coli heteroduplex recombination products in vivo: on the prevalence of 5′ and 3′ patches". PLoS One. 2 (11). s. e1242. doi:10.1371/journal.pone.0001242. PMC 2082072 $2. PMID 18043749.
- ^ Hiom, K (Temmuz 2009). "DNA Repair: Common Approaches to Fixing Double-Strand Breaks". Current Biology. 19 (13). ss. R523-R525. doi:10.1016/j.cub.2009.06.009.
- ^ a b Handa, N; ve diğerleri. (2009). "Reconstitution of initial steps of dsDNA break repair by the RecF pathway of E. coli". Genes and Development. Cilt 23. ss. 1234-1245. doi:10.1101/gad.1780709. PMC 2685532 $2. PMID 19451222.
- ^ Kowalczykowski, SC; ve diğerleri. (1987). "Effects of the Escherichia coli SSB protein on the binding of Escherichia coli RecA protein to single-stranded DNA. Demonstration of competitive binding and the lack of a specific protein-protein interaction". Journal of Biological Chemistry. 193 (1). ss. 81-95. doi:10.1016/0022-2836(87)90629-2. PMID 3295259.
- ^ a b c Sakai, A; Cox, MM (2009). "RecFOR and RecOR as distinct RecA loading pathways" (PDF). Journal of Biological Chemistry. 284 (5). ss. 3264-3272. doi:10.1074/jbc.M807220200. PMC 2631980 $2. PMID 18986990. 17 Haziran 2010 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 31 Ekim 2009.
- ^ Inoue, H; ve diğerleri. (Ocak 2008). "The process of displacing the single-stranded DNA-binding protein from single-stranded DNA by RecO and RecR proteins". Nucleic Acids Research. 36 (1). ss. 94-109. doi:10.1093/nar/gkm1004. PMC 2248737 $2. PMID 18000001.
- ^ a b West, SC (Temmuz 2003). "Molecular views of recombination proteins and their control". Nature Reviews Molecular Cell Biology. Cilt 4. ss. 435-437. doi:10.1038/nrm1127. PMID 12778123.
- ^ a b c Watson, JD; ve diğerleri. (2003). Molecular Biology of the Gene (5. bas.). Pearson/Benjamin Cummings. ss. 259-291. ISBN 978-0805346350.
- ^ Gumbiner-Russo, LM; Rosenberg, SM (Kasım 2007). "Physical analyses of E. coli heteroduplex recombination products in vivo: on the prevalence of 5′ and 3′ patches". PLoS One. 2 (11). s. e1242. doi:10.1371/journal.pone.0001242. PMC 2082072 $2. PMID 18043749.
- ^ Thomas, CM; Nielson, KM (Eylül 2005). "Mechanisms of, and barriers to, horizontal gene transfer between bacteria" (PDF). Nature Reviews Microbiology. 3 (9). ss. 711-721. doi:10.1038/nrmicro1234. PMID 16138099. 1 Haziran 2010 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 31 Ekim 2009.
- ^ Vulic, M; ve diğerleri. (Eylül 1997). "Molecular keys to speciation: DNA polymorphism and the control of genetic exchange in enterobacteria". Proceedings of the National Academy of Sciences USA. 94 (18). ss. 9763-9767. PMC 23264 $2. PMID 9275198.
- ^ Majewski, J; Cohan, FM (Ocak 1998). "The effect of mismatch repair and heteroduplex formation on sexual isolation in Bacillus". Genetics. 48 (1). ss. 13-18. PMC 1459767 $2. PMID 9475717.
- ^ Majewski, J; ve diğerleri. (Şubat 2000). "Barriers to genetic exchange between bacterial species: Streptococcus pneumoniae transformation". Journal of Bacteriology. Cilt 182. ss. 1016-1023. PMC 94378 $2. PMID 10648528.
- ^ Lodish H; ve diğerleri. (2000). "12.5: Recombination between Homologous DNA Sites: Double-Strand Breaks in DNA Initiate Recombination". Molecular Cell Biology (4. bas.). W. H. Freeman and Company. ISBN 0-7167-3136-3.
- ^ Griffiths, Anthony J.F.; ve diğerleri. (1999). "8: Chromosome Mutations: Chromosomal Rearrangements". Modern Genetic Analysis. W. H. Freeman and Company. ISBN 0-7167-3118-5. 27 Şubat 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 31 Ekim 2009.
- ^ Marcon, E; Moens, PB (Ağustos 2005). "The evolution of meiosis: recruitment and modification of somatic DNA-repair proteins". Bioessays. 27 (8). ss. 795-808. doi:10.1002/bies.20264. PMID 16015600.
- ^ a b Keeney, S; ve diğerleri. (Şubat 1997). "Meiosis-specific DNA double-strand breaks are catalyzed by Spo11, a member of a widely conserved protein family". Cell. 88 (3). ss. 375-384. doi:10.1016/S0092-8674(00)81876-0. PMID 9039264.
- ^ "A DNA recombination "hotspot" in humans is missing in chimps". PLoS Biology. 2 (6). Haziran 2004. s. e192. doi:10.1371/journal.pbio.0020192. PMC 423159 $2.
- ^ Shrivastav, M; ve diğerleri. (Ocak 2008). "Regulation of DNA double-strand break repair pathway choice". Cell Research. Cilt 18. ss. 134-147. doi:10.1038/cr.2007.111. PMID 18157161. 7 Eylül 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 31 Ekim 2009.
- ^ a b Mimitou, EP; Symington, LS (Mayıs 2009). "Nucleases and helicases take center stage in homologous recombination". Trends in Biochemical Science. 34 (5). ss. 264-272. doi:10.1016/j.tibs.2009.01.010. PMID 19375328.
- ^ a b c Sung, P; Klein, H (Ekim 2006). "Mechanism of homologous recombination: mediators and helicases take on regulatory functions". Nature Reviews Molecular Cell Biology. 7 (10). ss. 739-750. doi:10.1038/nrm2008. PMID 16926856.
- ^ Wold, MS (1997). "Replication protein A: heterotrimeric, single-stranded DNA-binding protein required for eukaryotic DNA metabolism". Annual Review of Biochemistry. Cilt 66. ss. 61-92. doi:10.1146/annurev.biochem.66.1.61. PMID 9242902.
- ^ McMahill, MS; ve diğerleri. (Kasım 2007). "Synthesis-dependent strand annealing in meiosis". PLoS Biology. 5 (11). s. e299. doi:10.1371/journal.pbio.0050299. PMC 2062477 $2. PMID 17988174.
- ^ Alberts B; ve diğerleri. (2008). Molecular Biology of the Cell (5. bas.). Garland Science. ss. 312-313. ISBN 978-0-8153-4105-5. 27 Şubat 2009 tarihinde kaynağından arşivlendi. Erişim tarihi: 31 Ekim 2009.
- ^ a b c Helleday, T; ve diğerleri. (Temmuz 2007). "DNA double-strand break repair: from mechanistic understanding to cancer treatment". DNA Repair (Amst.). 6 (7). ss. 923-935. doi:10.1016/j.dnarep.2007.02.006. PMID 17363343.
- ^ Haber lab. ""Single-strand annealing"". "Brandeis University". 19 Ocak 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 24 Ağustos 2009.
- ^ Mimitou, EP; Symington, LS (Eylül 2009). "DNA end resection: Many nucleases make light work". DNA repair. 8 (9). ss. 983-995. doi:10.1016/j.dnarep.2009.04.017.
- ^ Pâques, F; Haber, JE (Haziran 1999). "Multiple pathways of recombination induced by double-strand breaks in Saccharomyces cerevisiae". 63 (2). ss. 349-404. PMC 98970 $2. PMID 10357855.
- ^ a b McEachern, MJ; Haber, JE (2006). "Break-induced replication and recombinational telomere elongation in yeast". Annual Review of Biochemistry. Cilt 75. ss. 111-135. doi:10.1146/annurev.biochem.74.082803.133234. PMID 16756487.
- ^ Morrish, TA; Greider, CW (Ocak 2009). "Short telomeres initiate telomere recombination in primary and tumor cells". PLoS Genetics. 5 (1). s. e1000357. doi:10.1371/journal.pgen.1000357. PMC 2627939 $2. PMID 19180191.
- ^ Muntoni, RR; Reddel (Ekim 2005). "The first molecular details of ALT in human tumor cells". Human Molecular Genetics. 14 (Review Issue 2). ss. R191-R196. doi:10.1093/hmg/ddi266. PMID 16244317.
- ^ Cold Spring Harbor Laboratory (2007). "Human RecQ Helicases, Homologous Recombination And Genomic Instability". ScienceDaily. 10 Eylül 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 18 Aralık 2008.
- ^ Modesti, M; Kanaar, R (2001). "Homologous recombination: from model organisms to human disease". Genome Biology. 2 (5). s. REVIEWS1014. doi:10.1186/gb-2001-2-5-reviews1014. PMC 138934 $2. PMID 11387040.
- ^ Luo, G; ve diğerleri. (Aralık 2000). "Cancer predisposition caused by elevated mitotic recombination in Bloom mice". Nature Genetics. 26 (4). ss. 424-429. doi:10.1038/82548. PMID 11101838.
- ^ a b c Powell, SN; Kachnic, LA (Eylül 2003). "Roles of BRCA1 and BRCA2 in homologous recombination, DNA replication fidelity and the cellular response to ionizing radiation". Oncogene. 22 (37). ss. 5784-5791. doi:10.1038/sj.onc.1206678. PMID 12947386.
- ^ a b c Lin, Z; ve diğerleri. (2006). "Origins and evolution of the recA/Rad51 gene family: evidence for ancient gene duplication and endosymbiotic gene transfer". Proceedings of the National Academy of Sciences USA. 103 (27). ss. 10328-10333. doi:10.1073/pnas.0604232103. PMC 1502457 $2. PMID 16798872.
- ^ Ramesh, MA; ve diğerleri. (Ocak 2005). "A phylogenomic inventory of meiotic genes; evidence for sex in Giardia and an early eukaryotic origin of meiosis". Current Biology. 15 (2). ss. 185-191. doi:10.1016/j.cub.2005.01.003. PMID 15668177.
- ^ a b Malik, SB; ve diğerleri. (Aralık 2007). "Protist homologs of the meiotic Spo11 gene and topoisomerase VI reveal an evolutionary history of gene duplication and lineage-specific loss". Molecular Biology and Evolution. 24 (12). ss. 2827-2841. doi:10.1093/molbev/msm217. PMID 17921483.
- ^ Lodish H; ve diğerleri. (2000). "8.5:Gene Replacement and Transgenic Animals: DNA Is Transferred into Eukaryotic Cells in Various Ways". Molecular Cell Biology (4. bas.). W. H. Freeman and Company. ISBN 0-7167-3136-3.
- ^ "The Nobel Prize in Physiology or Medicine 2007". The Nobel Foundation. 8 Aralık 2015 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Aralık 2008.
- ^ Drummond, DA; ve diğerleri. (Nisan 2005). "On the conservative nature of intragenic recombination". Proceedings of the National Academy of Sciences USA. 102 (15). ss. 5380-5385. doi:10.1073/pnas.0500729102. PMC 556249 $2. PMID 15809422.
- ^ Bloom, JD; ve diğerleri. (Ocak 2005). "Thermodynamic prediction of protein neutrality". Proceedings of the National Academy of Sciences USA. 102 (3). ss. 606-611. doi:10.1073/pnas.0406744102. PMC 545518 $2. PMID 15644440.
- ^ a b Carbone, MN; Arnold, FH (Ağustos 2007). "Engineering by homologous recombination: exploring sequence and function within a conserved fold". Current Opinion in Structural Biology. 17 (4). ss. 454-459. doi:10.1016/j.sbi.2007.08.005. PMID 17884462.
- ^ Otey, CR; ve diğerleri. (Mayıs 2006). "Structure-guided recombination creates an artificial family of cytochromes P450". PLoS Biology. 4 (5). ss. e112. doi:10.1371/journal.pbio.0040112. PMC 1431580 $2. PMID 16594730.
- ^ Socolich, M; ve diğerleri. (Eylül 2005). "Evolutionary information for specifying a protein fold". Nature. Cilt 437. ss. 512-518. doi:10.1038/nature03991. PMID 16177782.
- ^ Thulasiram, HV; ve diğerleri. (Nisan 2007). "Chimeras of two isoprenoid synthases catalyze all four coupling reactions in isoprenoid biosynthesis". Science. 316 (5821). ss. 73-76. doi:10.1126/science.1137786. PMID 17412950.
- ^ Landwehr, M (Mart 2007). "Diversification of catalytic function in a synthetic family of chimeric cytochrome P450s". Chemistry and Biology. 14 (3). ss. 269-278. doi:10.1016/j.chembiol.2007.01.009. PMC 1991292 $2. PMID 17379142.
Ayrıca bakınız[değiştir | kaynağı değiştir]
Dış bağlantılar[değiştir | kaynağı değiştir]
- Animations - homologous recombination12 Aralık 2009 tarihinde Wayback Machine sitesinde arşivlendi.: Çeşitli homolog rekombinasyon modellerini gösteren animasyonlar
- Homologous recombination: Tempy & Trun8 Nisan 2007 tarihinde Wayback Machine sitesinde arşivlendi.: Homolog rekombinasyonun bakteriyel RecBCD yolağını gösteren animasyon
