Benzen: Revizyonlar arasındaki fark
| [kontrol edilmiş revizyon] | [kontrol edilmiş revizyon] |
k Kategori:Petrol ürünleri kaldırıldı; Kategori:Hidrokarbon çözücüler eklendi (HotCat) |
Khutuck Bot (mesaj | katkılar) k Bot: de:Benzol kaliteli maddedir |
||
| 36. satır: | 36. satır: | ||
{{Link SM|ro}} |
{{Link SM|ro}} |
||
{{Link SM|sl}} |
{{Link SM|sl}} |
||
{{Link GA|de}} |
|||
[[an:Benzén]] |
[[an:Benzén]] |
||
Sayfanın 00.32, 9 Şubat 2013 tarihindeki hâli

Benzen, aren veya aromatik hidrokarbonlar olarak adlandırılan organik bileşikler sınıfının en basit üyesidir. Renksiz, alevlenebilen, kaynama noktası 80,1 °C, erime noktası 5,5 °C olan bir sıvıdır. Moleküler formülü C6H6'dır. Benzen, endüstriyel bakımdan kıymetli olduğu gibi yapısı bakımından da kimya çalışmalarında önemlidir. Kan hücrelerini öldürme etkisi olduğundan kanser yapan bileşikler arasına girer. Eskiden balina yağının ısı etkisiyle bozunmasından elde edilen gaz, basınçla evlere gönderilir ve aydınlatmada kullanılırdı. Bu gazdan yağımsı bir kısım kalırdı. Benzen, 1825 yılında Michael Faraday tarafından bu yağımsı kısımda keşfedildi. Yaklaşık sekiz sene sonra başka araştırmacılar aynı maddeyi benzoik asidin kireçle oksidasyonundan elde ettiler. 1845'te August Wilhelm von Hofmann benzen diye adlandırdığı aynı maddeyi elde etmek için kömür katranı kullandı.

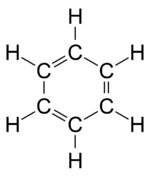
<ref> etiketinde geçersiz değişken (Bkz: Kaynak gösterme)Benzen, karbon atomlarının düzlemde düzgün altıgen şeklinde dizilmesinden meydana gelen bir yapıya sahiptir. Karbonlar arasında mesafe 1397 angströmdür. Köşelerde bulunan her karbon atomuna bir hidrojen atomu bağlıdır. Ayrıca değişik konformasyon yapılarında bulunabilir. Uzaysal olarak şekli düzlemsel şekline oranla oldukça farklıdır
Tepkime yeteneği
Benzenin yapısının kimyasal tepkimelere ne şekilde bir tepki gösterdiği üzerine yapılan çalışmaların, organik kimya teorilerinin gelişmesinde önemi büyük olmuştur. Hidrojen atomlarının karbon atomlarına oranının böyle düşük olduğu bir bileşikten umulan katılma tepkimeleri benzende olmaz. Benzenin gösterdiği tipik tepkimelerden biri, substitüsyon tepkimeleridir. Bu tepkime bir aktif grubun benzendeki bir hidrojeni çıkarıp onun yerine geçmesi şeklinde gerçekleşir. Bu davranışı izah etmek altı elektronun (benzende varmış gibi gösterilen 3 tane çifte bağdan ileri gelen) belli karbonlarda değil bütün benzen karbonlarına dağılmış olduğunu düşünmekle mümkün olur. Elektronların böyle dağılmış olması (belli karbonlarda olmaması) molekülün kararlı olmasını sağlar ve yine bu molekülün fiziksel ve kimyasal özelliklerini belirler.
Elde edilişi
Benzenin sübstitüsyon (yer değiştirme) tepkimeleri oldukça önemlidir. Çünkü, aromatik bileşiklerin pek çoğu bu tepkimelerle teşekkül ettirilir. İkinci Dünya Savaşı'ndan önce benzenin önemli kaynağı maden kömüründen elde edilen katran idi. İkinci Dünya Savaşı sırasında benzen ve bununla ilgili aromatik hidrokarbonlara (toluen, ksilen vb.) duyulan büyük ihtiyaç sebebiyle başka kaynaklar aranmaya başlandı. Bugün Amerika'da üretilen benzenin % 75'i petrolden olup, toluenin (C6H5-CH3) veya toluen ihtiva eden petrolün dealkilizasyonu işlemi ile yapılmaktadır. Bu işlem hidrojen kullanmayı, yüksek sıcaklığı, basıncı ve bir de katalizörü gerektirmektedir. İkinci bir metod naftence zengin petrolün yüksek sıcaklık ve basınçta dehidrojenlenmesidir. Benzen, fenol'ün indirgenmesiyle ve asetilenin trimerizasyonundan elde edilir.
Kullanılışı
Benzen, sanayide plastik imalinde kullanılan stiren ve fenolun sentezinde başlangıç maddesi olarak, naylon bileşenlerinde, sentetik deterjan imalinde kullanılır. Uçak benzinlerinde, boya yapmaya yarayan anilinin başlangıç maddesi ve böcek öldürücü olarak da benzen kullanılır. Benzen aynı zamanda iyi bir çözücüdür
Kaynak
Şablon:Link SM
Şablon:Link SM
Şablon:Link SM
Şablon:Link SM
Şablon:Link KM
Şablon:Link SM
Şablon:Link SM
Şablon:Link GA
