Kullanıcı:Efe7961/Çalışma2
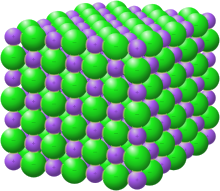
İyonik bileşik, iyonik bağ olarak adlandırılan elektrostatik kuvvetler tarafından bir arada tutulan iyonlardan oluşan kimyasal bir bileşiktir. Bileşik genel olarak nötrdür, ancak katyon adı verilen pozitif yüklü iyonlardan ve anyon adı verilen negatif yüklü iyonlardan oluşur. Bunlar sodyum klorürdeki sodyum (Na+) ve klorür (Cl-) gibi basit iyonlar veya amonyum (NH+4) ve karbonat (CO2-3) gibi çok atomlu türler olabilir.
Hidroksit (OH−) veya oksit (O2−) içeren iyonik bileşikler baz arak sınıflandırılır. Bu iyonları içermeyen iyonik bileşikler de tuzlar olarak adlandırılır ve asit-baz reaksiyonları ile oluşturulabilir. İyonik bileşikler ayrıca çözücülerinin buharlaşması, çökelme, donma, katı hal reaksiyonu veya reaktif metallerin halojen gazları gibi reaktif metal olmayanlarla elektron transfer reaksiyonu yoluyla kurucu iyonlarından üretilebilir.
İyonik bileşikler tipik olarak yüksek erime ve kaynama noktalarına sahiptir ve sert ve kırılgandır. Katı iyonlar normal şartlarda elektriği iletmezler ancak eritikldiklerinde veya suda çözündüklerinde, iyonlar harekete geçtiği için elektriksel olarak iletken olurlar ve elektriği iletirler.
Keşif tarihi[değiştir | kaynağı değiştir]
İyon kelimesi Grekçe: ἰόν, ion "gitmek" anlamına gelir. Bu terim, 1834'te fizikçi ve kimyager Michael Faraday tarafından, bir elektrottan diğerine sulu bir ortam aracılığıyla giden o zamanlar bilinmeyen türler için kullanıldı.[1][2]

1913'te sodyum klorürün kristal yapısı William Bragg ve Lawrence Bragg tarafından keşfedildi.[3][4][5] Yapılan çalışma, her atom için altı eşit uzaklıkta en yakın komşu olduğunu ortaya çıkardı, bu da bileşenlerin moleküller veya sonlu kümeler halinde değil, bunun yerine uzun menzilli kristal düzenine sahip bir ağ olarak düzenlendiğini gösterdi.[5] Diğer birçok inorganik bileşiğin de benzer yapısal özelliklere sahip olduğu bulundu.[5] Bu bileşiklerin kısa süre sonra nötr atomlardan ziyade iyonlardan oluştuğu ortaya çıktı, ancak bu hipotezin kanıtı, 1920'lerin ortalarına kadar, elektronların yoğunluğunu tespit eden X-ışını yansıma deneylerinin gerçekleştirildiği zamana kadar bulunamadı.[5][6]
İyonik kristal yapıların teorik bir tedavisinin geliştirilmesine başlıca katkıda bulunanlar Max Born, Fritz Haber, Alfred Landé, Erwin Madelung, Paul Peter Ewald ve Kasimir Fajans'dı.[7]
Oluşum[değiştir | kaynağı değiştir]

İyonik bileşikler, kendilerini oluşturan iyonlardan buharlaşma, çökeltme veya donma] yoluyla üretilebilir. Alkali metaller gibi reaktif metaller, iyonik bir ürün oluşturmak için yüksek elektronegatif halojen gazlarla doğrudan reaksiyona girebilir.[8] Katılar arasındaki yüksek sıcaklık reaksiyonunun ürünü olarak da sentezlenebilirler.[9]
Kaynakça[değiştir | kaynağı değiştir]
- ^ Michael Faraday (1791–1867). UK: BBC. 2016-08-25 tarihinde kaynağından arşivlendi.
- ^ "Online etymology dictionary". 2011-05-14 tarihinde kaynağından arşivlendi. Erişim tarihi: 2011-01-07.
- ^ Bragg, W. H.; Bragg, W. L. (1 July 1913). "The Reflection of X-rays by Crystals". Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. 88 (605): 428–438. Bibcode:1913RSPSA..88..428B. doi:10.1098/rspa.1913.0040.
- ^ Bragg, W. H. (22 September 1913). "The Reflection of X-rays by Crystals. (II.)". Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. 89 (610): 246–248. Bibcode:1913RSPSA..89..246B. doi:10.1098/rspa.1913.0082.
- ^ a b c d Sherman, Jack (August 1932). "Crystal Energies of Ionic Compounds and Thermochemical Applications". Chemical Reviews. 11 (1): 93–170. doi:10.1021/cr60038a002.
- ^ James, R. W.; Brindley, G. W. (1 November 1928). "A Quantitative Study of the Reflexion of X-Rays by Sylvine". Proceedings of the Royal Society A: Mathematical, Physical and Engineering Sciences. 121 (787): 155–171. Bibcode:1928RSPSA.121..155J. doi:10.1098/rspa.1928.0188.
- ^ Pauling 1960, s. 505.
- ^ Zumdahl 1989, s. 312.
- ^ Wold & Dwight 1993, s. 71.
