Sodyum hidroksit
| |

| |
| Adlandırmalar | |
|---|---|
Sodyum oksidanid[2] | |
| Tanımlayıcılar | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.013.805 |
| EC Numarası |
|
| E numaraları | E524 (asitliği düzenleyiciler, ...) |
| 68430 | |
| KEGG | |
| MeSH | Sodium+Hydroxide |
PubChem CID
|
|
| RTECS numarası |
|
| UNII | |
| UN numarası | 1824, 1823 |
CompTox Bilgi Panosu (EPA)
|
|
| |
| |
| Özellikler | |
| Molekül formülü | NaOH |
| Molekül kütlesi | 39.9971 g mol−1 |
| Görünüm | Beyaz, mumsu, opak kristaller |
| Koku | kokusuz |
| Yoğunluk | 2.13 g/cm3[5] |
| Erime noktası | 323 °C |
| Kaynama noktası | 1388 °C |
| Çözünürlük (su içinde) | 418 g/L (0 °C) 1000 g/L (25 °C)[5] 3370 g/L (100 °C) |
| Çözünürlük | gliserinde çözünür amonyakta çok az çözünür eterde çözünmez propilen glikolde yavaş çözünür |
| Çözünürlük (metanol içinde) | 238 g/L |
| Çözünürlük (etanol içinde) | <<139 g/L |
| Buhar basıncı | <2.4 kPa ( 20 °C) |
| Baziklik (pKb) | -0.56 (NaOH(aq) = Na+ + OH–)[6] |
| Yapı | |
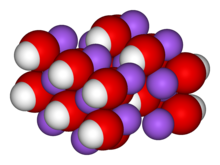
| Ortorombik, oS8=[7] | |
| Termokimya | |
Isı sığası (C)
|
59.5 J/mol K |
Standart molar entropi (S⦵298)
|
64.4 J•mol−1•K−1 |
Standart formasyon entalpisi (ΔfH⦵298)
|
−425.8 kJ•mol−1 |
Gibbs serbest enerjisi (ΔfG⦵)
|
-379.7 kJ/mol |
| Tehlikeler | |
| GHS etiketleme sistemi: | |
| Piktogramlar | 
|
| İşaret sözcüğü | Tehlike |
| Tehlike ifadeleri | H290, H314 |
| Önlem ifadeleri | P280, P305+P351+P338, P310 |
| NFPA 704 (yangın karosu) |
|
| Öldürücü doz veya konsantrasyon (LD, LC): | |
LD50 (medyan doz)
|
40 mg/kg (fare, intraperitoneal)[9] |
| NIOSH ABD maruz kalma limitleri: | |
| PEL (izin verilen) | TWA 2 mg/m3[8] |
| Güvenlik bilgi formu (SDS) | Dış SDS |
| Benzeyen bileşikler | |
Diğer anyonlar
|
Sodyum bisülfür Sodyum hidrür |
Diğer katyonlar
|
Sezyum hidroksit Lityum hidroksit Potasyum hidroksit |
| Aksi belirtilmediği sürece madde verileri, Standart sıcaklık ve basınç koşullarında belirtilir (25 °C [77 °F], 100 kPa).
| |
| Bilgi kutusu kaynakları | |
Kostik ve kostik soda olarak da bilinen sodyum hidroksit,[3][4] NaOH formülüne sahip bir inorganik bileşiktir. Sodyum katyonları Na+ ve hidroksit anyonları OH- içeren beyaz renkli katı bir iyonik bileşiktir.
Suda kolaylıkla çözünür ve yumuşak kaygan ve sabun hissi veren bir çözelti oluşturur. İnsan dokusuna kaşındırıcı bir etkisi vardır. Sodyum hidroksit (kostik soda veya sud kostik te denir), lâboratuvarda CO2 gibi asidik gazları yakalamak için kullanılır. Endüstride birçok kimyasal maddenin yapımında, yapay ipek, sabun, kâğıt, boya, deterjan endüstrisinde ve petrol rafinelerinde kullanılır. Ayrıca serigrafide pozitif20 ile beraber kullanılır. Bir bazdır. Su ile tepkimeye girdiğinde yaklaşık 5 dakika içinde sıcaklığı 50 Santigrat dereceye çıkar ve yaklaşık 15 dakika sıcak kalır.
Ayrıca bakınız
Kaynakça
- ^ a b "Sodium Hydroxide – Compound Summary". 1 Kasım 2012 tarihinde kaynağından arşivlendi. Erişim tarihi: 12 Haziran 2012.
- ^ "1310-73-2|Sodium hydroxide solution|Sigma Aldrich|sodium oxidanide" 27 Ocak 2018 tarihinde Wayback Machine sitesinde arşivlendi.. chembase.cn.
- ^ a b "Material Safety Datasheet" (PDF). certified-lye.com. 28 Şubat 2008 tarihinde kaynağından arşivlendi (PDF). Erişim tarihi: 7 Haziran 2020.
- ^ a b "Material Safety Datasheet 2" (PDF). hillbrothers.com. 3 Ağustos 2012 tarihinde kaynağından (PDF) arşivlendi. Erişim tarihi: 20 Mayıs 2012.
- ^ a b Haynes, p. 4.90
- ^ "Sortierte Liste: pKb-Werte, nach Ordnungszahl sortiert. – Das Periodensystem online". 16 Kasım 2018 tarihinde kaynağından arşivlendi. Erişim tarihi: 15 Ocak 2019.
- ^ Jacobs, H.; Kockelkorn, J. and Tacke, Th. (1985). "Hydroxide des Natriums, Kaliums und Rubidiums: Einkristallzüchtung und röntgenographische Strukturbestimmung an der bei Raumtemperatur stabilen Modifikation". Z. Anorg. Allg. Chem. 531: 119-124. doi:10.1002/zaac.19855311217.
- ^ NIOSH Pocket Guide to Chemical Hazards. "#0565". National Institute for Occupational Safety and Health (NIOSH).
- ^ Michael Chambers. "ChemIDplus – 1310-73-2 – HEMHJVSKTPXQMS-UHFFFAOYSA-M – Sodium hydroxide [NF] – Similar structures search, synonyms, formulas, resource links, and other chemical information.". nih.gov.
| İnorganik kimya ile ilgili bu madde taslak seviyesindedir. Madde içeriğini genişleterek Vikipedi'ye katkı sağlayabilirsiniz. |

