Sodyum bisülfat: Revizyonlar arasındaki fark
| [kontrol edilmiş revizyon] | [kontrol edilmiş revizyon] |
Değişiklik özeti yok |
Değişiklik özeti yok |
||
| 87. satır: | 87. satır: | ||
[[ar:بيكبريتات الصوديوم]] |
[[ar:بيكبريتات الصوديوم]] |
||
[[de:Natriumhydrogensulfat]] |
[[de:Natriumhydrogensulfat]] |
||
[[en:Sodium bisulfate]] |
|||
[[fr:Hydrogénosulfate de sodium]] |
[[fr:Hydrogénosulfate de sodium]] |
||
[[it:Idrogenosolfato di sodio]] |
[[it:Idrogenosolfato di sodio]] |
||
Sayfanın 21.49, 24 Ekim 2012 tarihindeki hâli
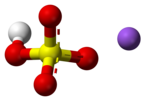
| Sodyum bisülfat | |
|---|---|
| |
| IUPAC Adı | Sodyum hidrojen sülfat |
| Diğer adlar | Sodyum asit sülfat |
| Tanımlamalar | |
| CAS No. | 7681-38-1 |
| RTECS | VZ1860000 |
| EC No. | 231-665-7 |
| Özellikleri | |
| Kimyasal formülü | NaHSO4 |
| Molekül ağırlığı | 120.06 gr./mol (susuz) 138.07 gr./mol (monohidrat) |
| Fiziksel görünüm | Beyaz kristal |
| Yoğunluk | 2.742 gr./cm3 (susuz) 1.8 gr./ cm3 (monohidrat) |
| Erime noktası | 58.5 °C (susuz) 315 °C (monohidrat) |
| Kaynama noktası | 315 °C (parçalanır) |
| Sudaki çözünürlüğü | 50 gr./100 mL (0 °C) 100 gr./100 mL (100 °C) |
| Çözünürlük | amonyak da çözünmez alkol de parçalanır. |
| Yapısı | |
| Kristal yapısı | Triklinik (susuz), Monoklinik (monohidrat) |
Sodyum bisülfat, diğer bir adı sodyum hidrojen sülfat (NaHSO4) olan bu kimyasal madde asit tuz karakterlidir. Kuru halde iken güvenli bir şekilde nakledilebilir ve depolanabilir. Susuz formu higroskopiktir. Sodyum bisülfat suda hidroliz olarak asidik çözelti verir. 1 Molarlık çözeltisinin pH değeri 1 den küçüktür . Sodyum bisülfat yavaşça ısıtılırsa suyunu kaybederek sodyum pirosülfata dönüşür.
- 2NaHSO4 → Na2S2O7 + H2O
Eğer ısıtma yüksek sıcaklıklarda yapılırsa sodyum sülfat ve kükürt trioksit oluşur.
- 2NaHSO4 → Na2SO4 + SO3 + H2O
Üretimi
Üretim yöntemlerinden ilki stokiyometrik miktardaki sodyum hidroksit ve sülfürik asit karışımının reaksiyonuna dayanır. İki eşdeğer asit ve bir eşdeğer baz kullanılması ile sodyum bisülfat ve su oluşur.
- NaOH + H2SO4 → NaHSO4 + H2O
İkinci bir üretim yöntemi ise sodyum klorür (tuz) ve sülfürik asit arasında gerçekleşen reaksiyondur. Yüksek sıcaklıkta gerçekleşen bu reaksiyon sonucunda sodyum bisülfat ve hidrojen klorür gazı oluşur.
- NaCl + H2SO4 → NaHSO4 + HCl
Sıcak ve derişik sodyum bisülfat çözeltisi püskürtmek suretiyle soğutulduğunda katı kristalleri oluşturur. Hidrojen klorür gazı ise reaksiyonun yan ürünü olarak hidroklorik asit üretmek için suda çözülür.
Kullanımı
Sodyum bisülfat başlıca pH düşürmek için kullanılır. Teknik olarak uygulamalarda metal parlatma, temizlik ürünleri ve yüzme havuzlarındaki klorlama işleminin etkinliğini artırmak için gerekli olan suyun pH derecesini düşürmek amacıyla kullanılır. Sodyum bisülfat kedilerde idrar yolları taşlarını azaltmak amacıyla kedi mamalarında yem katkı maddesi olarak kullanılır. Besin kalitesindeki sodyum bisülfat meşrubatlar da dahil olmak üzere çeşitli yiyecek ürünlerinde, mayonezler ve soslar da kullanılmaktadır. Ayrıca et ve kümes hayvanlarının işlenmesinde, kesilmiş taze etlerin kararmasını önlemek için oldukça sık kullanılır.
Kuyumculuk da da kendine kullanım yeri bulan sodyum bisülfat, ısıtılan yüzeylerde oluşan oksit tabakasını kaldırmak için kullanılan birçok çözeltilerde yüzey temizleme amacıyla bulunan başlıca maddedir.
